
【题目】下列转化过程中必须加入氧化剂的是
A.FeS→H2SB.KClO3→O2
C.I—→I2D.Fe3+→Fe2+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】钢铁厂在冷轧过程中会产生高浓度酸性含铁废水,主要含有H+、Cl﹣、Fe2+、Fe3+等,其处理的主要工艺流程如下:
请回答:
(1)废水未经处理直接排放的危害是(填字母).
a腐蚀水利设施 b影响水生生物的自然生长
(2)石灰乳用于中和含铁废水中的酸,写出石灰乳与盐酸反应的化学方程式: .
(3)过氧化氧的主要作用是(填字母).a还原剂 b氧化剂
(4)自来水厂常用漂白粉、液氯、二氧化氯、臭氧等作为消毒剂,杀灭水中的细菌.液氯注入水中后,能杀死水中细菌的物质是(填化学式).
(5)污水处理中的主要化学方法有中和法、、、 .
(6)某研究小组对钢铁厂高浓度酸性含铁废水进行监测时,取其样本稀释,测得有关数据如下:
离子 | H+ | Cl﹣ | Fe2+ | Fe3+ |
浓度(molL)﹣1 | 0.16 | 0.94 | 0.18 |
稀释后的溶液中c(Fe2+)=mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用铁粉制备摩尔盐的操作流程如下:
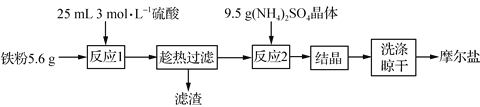
(1)流程中“趁热”过滤的原因是__________。
(2) 反应1制得硫酸亚铁的物质的量理论上应小于__________mol。
(3)为确定摩尔盐的化学式,进行如下实验:现称取4.704 g新制摩尔盐,溶于水配制成100.0 mL溶液,再将该溶液分成两等份。
向其中一份溶液中加入足量Ba(OH)2溶液,并微热,逸出能使湿润的红色石蕊试纸
变蓝的气体,同时生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色,用足量稀盐酸处理沉淀物,充分反应后过滤、洗涤和干燥,得白色固体2.796 g。
另一份溶液用0.050 0 mol·L-1 K2Cr2O7酸性溶液滴定,当Cr2O![]() 恰好完全被还原为Cr3+时,消耗K2Cr2O7溶液的体积为20.00 mL。
恰好完全被还原为Cr3+时,消耗K2Cr2O7溶液的体积为20.00 mL。
①25℃时,Ksp(BaSO4)=1.1×10-10,若要使溶液中SO![]() 离子沉淀完全(即该离子浓度须小于1×10-5 mol·L-1),则此时c[(Ba(OH)2]≥__________mol·L-1。
离子沉淀完全(即该离子浓度须小于1×10-5 mol·L-1),则此时c[(Ba(OH)2]≥__________mol·L-1。
②确定该摩尔盐的化学式(写出计算过程)。___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=12的氢氧化钠溶液和pH=4的醋酸溶液等体积混合后恰好中和,忽略混合后溶液体积的变化,下列说法中正确的是( )
A.混合后的溶液中c(Na+)=c(CH3COO-)
B.混合前的醋酸约1%发生电离
C.氢氧化钠和醋酸的浓度不相等
D.混合后的溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列反应在任何温度下均能自发进行的是( )
A.2N2(g)+O2(g)=2N2O(g) ΔH=+163 kJ·mol-1
B.Ag(s)+ ![]() Cl2(g)=AgCl(s) ΔH=-127 kJ·mol-1
Cl2(g)=AgCl(s) ΔH=-127 kJ·mol-1
C.H2O2(l)= ![]() O2(g)+H2O(l) ΔH=-98 kJ·mol-1
O2(g)+H2O(l) ΔH=-98 kJ·mol-1
D.HgO(s)=Hg(l)+ ![]() O2(g) ΔH=+91 kJ·mol-1
O2(g) ΔH=+91 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾(其中的PM2. 5,即大气中粒径小于或等于2.5 μm的颗粒物;1 μm=1x10-6m)中物质转化如下图所示。下列说法正确的是
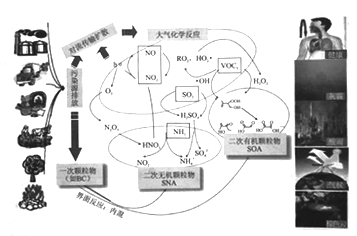
A. PM2.5属于胶体
B. 一次颗粒物(如BC)中不含碳元素
C. 二次无机颗粒物(SNA)主要成分为NH4NO3和( NH4)2SO4
D. 二次有机颗粒物(SOA)主要成分![]() 属于醇类
属于醇类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①离子化合物中可能含有共价键 ②构成晶体的粒子一定含有共价键 ③共价化合物中不可能含有离子键 ④晶体中含阳离子时一定含阴离子。
A. ①②
B. ①③
C. ②④
D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com