
【题目】下列叙述正确的是( )
①离子化合物中可能含有共价键 ②构成晶体的粒子一定含有共价键 ③共价化合物中不可能含有离子键 ④晶体中含阳离子时一定含阴离子。
A. ①②
B. ①③
C. ②④
D. ③④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
(1) H3BO3中B元素的化合价为______,其在元素周期表的位置是_________________。
(2)已知:A(OH)3+H2O![]() [Al(OH)4]-+H+,H3BO3的电离方程式为_______。酸性:H3BO3 _____(填*>”或“<”)Al(OH)3。
[Al(OH)4]-+H+,H3BO3的电离方程式为_______。酸性:H3BO3 _____(填*>”或“<”)Al(OH)3。
(3) H3BO3受热分解得到的B2O3和镁粉混合点燃可得单质B,生成单质B的化学方程式为________。
(4) H3BO3可用于生产储氢材料NaBH4。涉及的主要反应为:
I.H3BO3+3CH3OH→B(OCH3)3+3H2O
II.B(OCH3)3+4NaH→NaBH4+3CH3ONa
①“反应I”的类型为__________(填标号)。
A.取代反应 B.加成反应 C.加聚反应 D.氧化反应
②NaH的电子式为_______________。
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和Na[B(OH)4],其中H元素由-1价升高为+1价,该反应的离子方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关甲烷和乙烷的说法中,错误的是
A.互为同系物
B.均不能使高锰酸钾酸性溶液褪色
C.在核磁共振氢谱图(1H核磁共振谱图)中,均只有1个吸收峰
D.二氯取代物均为两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝(熔点660℃)是一种应用广泛的金属,工业上用Al2O3(熔点2045℃)和冰晶石(Na3AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)铝属于活泼金属却能在空气中稳定存在,原因是____(用化学用语及相关文字说明)。
(2)将0.1mo/LAlCl3溶液和10%NH4F溶液混合制取Na3AlF6。该实验所用试管及盛装NaF溶液的试剂瓶均为塑料材质,原因是____(用离子方程式表示)。
(3)下列关于氧化铝的叙述正确的是_____。
A.氧化铝可以治疗胃酸过多 B.氧化铝因为熔点高,可以作耐火材料
C.氧化铝是铝热剂的成分之一 D.氧化铝是天然蓝宝石的主要成分
(4)以Al 和NiO(OH)为电极,NaOH 溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是________。
(5)某工厂排放出有毒物质NOC1,它遇水就会生成NO3-。NOCl 分子中各原子均满足8电子稳定结构,则NOCl的电子式为____。水源中的NO3-对人类健康会产生危害,为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙烯![]() 可用于制作食品包装袋,在一定条件下可通过乙烯生成聚乙烯,下列说法中正确的是( )
可用于制作食品包装袋,在一定条件下可通过乙烯生成聚乙烯,下列说法中正确的是( )
A. 燃烧等质量的乙烯和聚乙烯时,聚乙烯消耗的氧气多
B. 乙烯比乙烷的含碳量高,燃烧时容易产生浓烟
C. 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
D. 乙烯和聚乙烯都能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水中的电离方程式是H2A = H+ + HA﹣ , HA﹣ ![]() H+ + A2﹣ . 回答下列问题:
H+ + A2﹣ . 回答下列问题:
(1)Na2A溶液显(填“酸性”、“中性”或“碱性”),理由是(用离子方程式或必要的文字说明).
(2)常温下,已知0.1molL﹣1NaHA溶液pH=2,则0.1molL﹣1H2A溶液中氢离子的物质的量浓度可能0.11molL﹣1(填“大于”、“等于”或“小于”),理由是 .
(3)0.1molL﹣1NaHA溶液中各种离子浓度由大到小的顺序是 .
(4)Na2A溶液中,下列表述正确的是_________.
A.c(Na+)+ c(H+)= c(HA﹣)+ 2c(A2﹣)+ c(OH﹣)
B.c(OH﹣)= c(HA﹣)+ c(H+)
C.c(OH﹣)= c(HA﹣)+ c(H+)+ 2c(H2A)
D.c (Na+)= 2[c(HA﹣)+ c(A2﹣) + c(H2A)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( ) 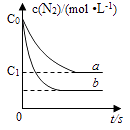
A.温度T下,该反应的平衡常数K= ![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)===2LiH(s) ΔH=-182 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1;
③4Li(s)+O2(g)===2Li2O(s) ΔH=-1196 kJ·mol-1。
试写出LiH在O2中燃烧的热化学方程式:__________________________________________。
(II)利用H2和CO2生产甲醇。某温度下,在容积为2L的密闭容器中充入1molCO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
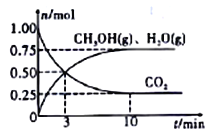
(1)从反应开始到3min时,氢气的平均反应速率v(H2)=____________。
(2)下列措施中一定能使CO2的转化率增大的是_______________(填序号)。
A.在原容器中再充入1mol CO2 B.在原容器中再充入1mol H2
C.在原容器中再充入1mol He D.使用更有效的催化剂
E. 缩小容器的容积 F. 将水蒸气从体系中分离出
(III)图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
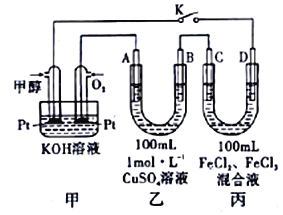
(1)甲中负极的电极反应式为_______________________________。
(2)乙中A极析出的气体在标准状况下的体积为_______________________。
(IV)已知常温下CN-的水解常数Kb=1.61×10-5。
(1)常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_________(填“酸”“碱”或“中”)性,c(CN-)_______(填“>”“<”或“=”)c(HCN)。
(2)常温下,若将c molL-1盐酸与0.61 molL-1KCN溶液等体积混合后恰好得到中性溶液,则c=________(小数点后保留4位数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com