
【题目】原子序数依次递增的甲、乙、丙、丁、戊是周期表中前30号元素,其中甲、乙、丙三元素的基态原子2p能级都有单电子,单电子个数分别是2、3、2;丁与戊原子序数相差18,戊元素是周期表中ds区的第一种元素。回答下列问题:
(1)甲能形成多种常见单质,在熔点很高的两种常见单质中,原子的杂化方式分别为______、__________。
(2)+1价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测丁元素的电离能突增应出现在第________电离能。
(3)戊的基态原子有________种形状不同的原子轨道;
(4)甲、乙分别都能与丙形成原子个数比为 1:3的微粒,则该两种微粒的空间构型分别为:_________________ ;__________________。
(5)丙和丁形成的一种离子化合物的晶胞结构如右图,该晶体中阳离子的配位数为_________ 。距一个阴离子周围最近的所有阳离子为顶点构成的几何体为_______________。已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,该化合物的相对分子质量为 M,则该晶胞中黑球的半径r =_____cm。(用含ρ、NA的计算式表示)

【答案】 sp2 sp3 二 3 平面三角形 平面三角形 8 正方体(立方体) 
【解析】甲、乙、丙原子序数依次递增,甲、乙、丙三元素的基态原子2p能级都有单电子,单电子个数分别是2、3、2,故甲、乙、丙分别是C、N、O,戊元素是周期表中ds区的第一种元素,所以戊为Cu,丁与戊原子序数相差18,则丁为Na,由分析知甲、乙、丙、丁、戊分别是C、N、O、Na、Cu元素,
(1)碳单质中熔点较高的有金刚石和石墨,金刚石中碳原子全部形成4个共价键,所以是sp3杂化,而石墨层状结构,碳原子形成3个共价键,所以是sp2杂化,故答案为:sp2;sp3;
(2)钠是第IA元素,最外层有1个电子,失去1个电子后,就达到稳定结构,再失电子会很困难,所以电离能突增应出现在第二电离能,故答案为:二;
(3)Cu是29号元素,原子核外电子数为29,基态原子核外电子排布式为:1s22s22p63s23p63d104s1,可以看出铜原子的基态原子轨道是s、p、d,所以有3种形状不同的原子轨道,故答案为:3;
(4)甲、乙都能和丙形成原子个数比为1:3的常见微粒分别是CO32-、NO3-,中心原子含σ键电子对数为3对,CO32-含有的电子对数=3+![]() =3,NO3-含有的电子对数=3+
=3,NO3-含有的电子对数=3+![]() =3,所以都是平面三角形结构,故答案为:平面三角形;平面三角形;
=3,所以都是平面三角形结构,故答案为:平面三角形;平面三角形;
(5)根据晶胞(Na2O)结构可知N(Na+):N(O2-)=2:1,根据晶胞结构,顶点和面心处微粒的数目为8×![]() +6×
+6×![]() =4,内部的微粒数目为8,所以顶点和面心处是阴离子,阳离子全部在晶胞内,所以与钠离子最近的阴离子是4个,即配位数是4.而距一个阴离子周围最近的所有阳离子为顶点构成的几何体是正方体.该晶胞中含有4个阴离子,所以有
=4,内部的微粒数目为8,所以顶点和面心处是阴离子,阳离子全部在晶胞内,所以与钠离子最近的阴离子是4个,即配位数是4.而距一个阴离子周围最近的所有阳离子为顶点构成的几何体是正方体.该晶胞中含有4个阴离子,所以有![]() =4,解得a=
=4,解得a=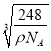 ,故答案为:8;正方体(立方体);
,故答案为:8;正方体(立方体); 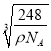 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知某溶液中含有下列8种离子中的5种(忽略水的电离及离子的水解):K+、Cu2+、Al3+、Fe2+、Cl﹣、CO32﹣、NO3﹣、SO42﹣ , 且5种离子的物质的量浓度相等.为了进一步探究该水溶液的组成,某同 学进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰.
②另取溶液加入足量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
③另取溶液加入BaCl2溶液,有白色沉淀生成.
根据上述实验,以下推测正确的是( )
A.无法确定溶液中是否存在Cu2+离子
B.原溶液中不含K+、Al3+、CO![]() 等离子
等离子
C.根据步骤②只能确定溶液中一定存在NO3﹣离子
D.步骤③所得到的白色沉淀共有2种钡盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酸的结构简式为CH2=CH—COOH,对其性质的描述不正确的是
A. 能与金属钠反应放出氢气B. 能与溴水发生加成反应而使溴水褪色
C. 能使酸性高锰酸钾溶液褪色D. 不能与新制氢氧化铜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】组成蛋白质的元素主要有C、H、O、N及S、P和少量的Zn、Cu等.
(1)N、P、S的第一电离能由小到大的顺序为 .
(2)组成蛋白质的最简单的氨基酸(HOOCCH2NH2)介子中,π键数目为 .
(3)Zn2+、Cu2+能与NH3、H2O、Cl﹣等形成配位数为4的配合物.①基态Zn2+的价电子(外围电子)排布式为 .
②[Zn(H2O)4]SO4中不存在的化学键类型有 . (填序号).
a.配位键 b.金属键 c.共价键 d.氢键 e.离子键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 .
a.平面正方形 b.正四面体 c.三角锥形 d.V形
(4)由上述几种元素组成的6一氨基青霉烷酸的结构如图,其中采用sp3杂化的原子除了S外,还有 .
(5)紫外光的光子所具有的能量约为399kJmol﹣根据下表有关蛋白质分子中主要化学键的键能信息,说明人体长时间照射紫外光后皮肤易受伤害的原因是(填序号).
共价键 | C﹣C | C﹣N | C﹣S |
键能/(kJmol﹣1) | 347 | 305 | 259 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于油脂的叙述不正确的是( )
A. 油脂是指油和脂肪,它们不属于酯类
B. 油脂没有固定的熔、沸点
C. 油脂是高级脂肪酸的甘油酯
D. 油脂是一种有机溶剂,可溶解多种维生素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH﹣+2HCO ![]() ═CaCO3↓+CO
═CaCO3↓+CO ![]() +2H2O
+2H2O
B.向NH4HSO4稀溶液中加入NaOH稀溶液少量:OH﹣+NH ![]() ═NH3?H2O
═NH3?H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
D.向淀粉KI溶液中滴加酸性H2O2溶液,溶液变蓝色:H2O2+2I﹣+2H+═I2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物M的结构简式如下: ![]() 下列有关M的叙述中正确的是( )
下列有关M的叙述中正确的是( )
A.M的分子式为:C12H15O5N2
B.M可以发生水解反应、中和反应、加成反应、消去反应
C.M的水解产物中一定含有醇类
D.1 molM最多可以与1L4mol/L的NaOH溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够鉴定氯乙烷中氯元素的存在的操作是( )
A.在氯乙烷中直接加入AgNO3溶液
B.加蒸馏水,充分搅拌后,加入AgNO3溶液
C.加入稀硝酸酸化,然后加入AgNO3溶液
D.加入NaOH的乙醇溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com