
【题目】下列有关物质的量浓度关系中,不正确的是:
A. 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B. 浓度相同的下列溶液: ①(NH4) 2 Fe(SO4)2 ②(NH4) 2 CO3 ③(NH4) 2SO4 ,NH4+浓度由大到小的顺序是:①>③>②
C. 浓度均为0.1 mol·L-1CH3COONa、NaHCO3、![]() -ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1
-ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1
D. NaHCO3溶液中:c(Na+)=c(H2CO3)+c(HCO3-)+2c(CO32-)
【答案】D
【解析】
A.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合,反应后的溶液溶质为等浓度的(NH4)2SO4和Na2SO4,NH4+水解,溶液呈酸性,则c(Na+)=c(SO42-)>c(NH4+),c(H+)>c(OH-),一般来说,单水解的程度较弱,则有c(NH4+)>c(H+),应有c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故A正确;B.硫酸亚铁铵中,亚铁离子对铵根离子的水解起到抑制作用;碳酸铵中,碳酸根对铵根离子的水解起到促进作用,硫酸根离子不影响铵根离子的水解,所以三种溶液中NH4+浓度大小为:①>③>②,故B正确;C.已知酸性:CH3COOH>H2CO3>![]() -OH,酸性越弱,对应的盐类水解程度越大,则浓度均为0.1 molL-1CH3COONa、NaHCO3、
-OH,酸性越弱,对应的盐类水解程度越大,则浓度均为0.1 molL-1CH3COONa、NaHCO3、![]() -ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1,故C正确;D.根据物料守恒可知,NaHCO3溶液中存在c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),故D错误;故选D。
-ONa溶液中:若c(OH-)分别为c1、c2、c3,则c3>c2>c1,故C正确;D.根据物料守恒可知,NaHCO3溶液中存在c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),故D错误;故选D。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】下列操作中最终可以得到Al(OH)3的是( )
A. Al2O3和水混合加热 B. Al和水反应
C. 过量的NaOH溶液加入到AlCl3溶液中 D. 过量的氨气通入到AlCl3溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人说:“Na2O2脾气火爆,一见二氧化碳就变脸, 遇见水就生气”。这种说法引起了某学习小组的兴趣,于是对Na2O2性质进行以下实验探究。
完成下列填空:
(1)实验装置如图所示。挤压胶头滴管,预期看到的实验现象________________、__________(写出2条主要现象)。
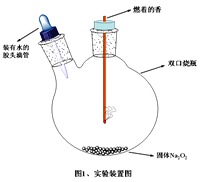
(2)写出Na2O2遇CO2“变脸”的化学方程式____________。若Na2O2长期露置于空气中,最终会转化为_________(填物质名称)。
(3)某同学发现Na2O2见水“生气”后所得溶液温度升高,滴加酚酞试液,酚酞先变红,但很快就褪色。对此设计实验进行探究:取两支试管分别加入少量Na2O2粉末,一支冰水浴,一支热水浴,两支试管里都滴加蒸馏水和酚酞。该实验的目的是__________________________。另一同学将实验改为:取两支试管,分别加入滴有酚酞的红色NaOH溶液,一支冰水浴,一支热水浴。你认为改后能否达到原实验目的____________,理由_______________________________。
(4)根据Na2O2的性质,指出它的一种用途_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低合金高强度钢是支撑"鸟巢"的铁骨钢筋,除含有铁元素外,还含有Mn(锰),Ti(钛),(铬),(铌)等合金元素,下列有关说法正确的是( )
A. Fe位于元素周期表的第四周期,第VIIIB族
B. 46TiO、 48TiO、50TiO互为同位素
C. Mn 2O7是酸性氧化物
D. ![]() 原子核内有个51个中子,核外有 41个电子
原子核内有个51个中子,核外有 41个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:![]() 下列叙述错误的是
下列叙述错误的是
A. 放电时正极附近溶液的碱性增强
B. 充电时锌极与外电源正极相连
C. 放电时每转移3 mol电子,正极有1mol K2FeO4被还原
D. 充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- FeO42- + 4 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯(![]() )是合成橡胶和塑料的重要单体,也是生产某些药物、农药的中间体。化合物E是一种昆虫信息素,可以通过以下流程制备。
)是合成橡胶和塑料的重要单体,也是生产某些药物、农药的中间体。化合物E是一种昆虫信息素,可以通过以下流程制备。

完成下列填空:
(1)反应②的反应类型__________;上述流程中的物质,与B互为同分异构体是__________。写出B的属于芳香烃的一种同分异构体的结构简式__________,该物质的名称为_________。
(2)反应①中,A和苯按摩尔比1:1完全反应,产物只有B。写出A的结构简式___________。
(3)写出反应③的化学方程式____________________________________。
(4)以B为原料制取C的反应是可逆反应,分离C、B混合物的实验操作为____________。
(5)苯乙烯露置于空气中可被氧化为苯甲醛和甲醛。设计实验方案检验苯乙烯样品是否被氧化变质______________________________________。
(6)参照上述合成路线的表示方法,设计以苯乙烯为原料经过三步反应制备新型高分子导电材料PPA(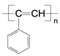 )的合成路线,并注明必要的反应条件。(无机物任选)_____________
)的合成路线,并注明必要的反应条件。(无机物任选)_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔生理学或医学奖。研究团队发现在温度较高时未能提取到青蒿素,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素。下面反应是青蒿素在一定条件下转化为双氢青蒿素:

以下说法不正确的是( )
A. 较高温度下未能提取到青蒿素的原因与分子中存在非极性的O—O键的不稳定性有关
B. 青蒿素和双氢青蒿素均能使湿润的淀粉-碘化钾试纸变蓝色
C. 双氢青蒿素比青蒿素的水溶性好,所以治疗疟疾的效果更好
D. 青蒿素属于酯类化合物,分子中碳原子采用sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As2O3在医药、电子等领域有重要应用。某含砷元素(As)的工业废水经如图1流程转化为粗产品。
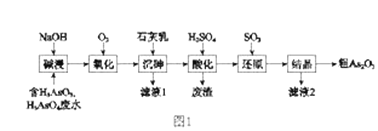
(1)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐。H3AsO4转化为Na3AsO4反应的化学方程式是_______________________________。
(2)“氧化”时,1molAsO33-转化为AsO43-至少需要O2______ mol。
(3)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有:
a.Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq) △H<0
Ca2+(aq)+2OH-(aq) △H<0
b.5Ca2++OH-+3AsO43-![]() Ca5(AsO4)3OH △H>0
Ca5(AsO4)3OH △H>0
研究表明:“沉砷”的最佳温度是85℃。 用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因是_____________________。
(4)“还原”过程中H3AsO4转化为H3AsO3,反应的化学方程式是_______________________。
(5)“还原”后加热溶液,H3AsO3分解为As2O3,同时结晶得到粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如图2所示。为了提高粗As2O3的沉淀率,“结晶”过程进行的操作是_______。
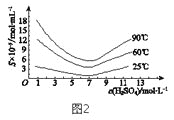
(6)下列说法中,正确的是 ______ (填字母)。
a.粗As2O3中含有CaSO4
b.工业生产中,滤液2可循环使用,提高砷的回收率
c.通过先“沉砷”后“酸化”的顺序,可以达到富集砷元素的目的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com