
【题目】化合物的知识贯穿整个高中学习,通过《化学反应原理》这本书的学习更是加深了对它们的认识。
(1)亚磷酸是二元弱酸。已知:
![]()
![]()
![]()
求![]()
![]()
![]() ______________
______________
(2)亚磷酸溶液与硝酸银溶液混合生成单质银和NO,写出该反应的离子方程式_________
(3)关于![]() 溶液,下列表达正确的是_____
溶液,下列表达正确的是_____
A.![]()
B.![]()
C.![]()
科目:高中化学 来源: 题型:
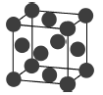
【题目】四种晶体的晶胞结构如图所示,下列有关说法正确的是( )
A.图甲所示晶体的化学式为A3B4C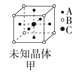
B.图乙所示晶体中阴阳离子个数比为1:1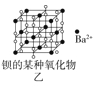
C.图丙所示CaF2晶体中Ca2+配位数为4,F-配位数为8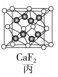
D.图丁所示晶体属于简单立方堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,[Cu(NH3) 4]( NO3) 2与液氨混合并加入Cu可制得一种黑绿色晶体。
(1)基态Cu2+核外电子排布式是______。
(2)黑绿色晶体的晶胞如图所示,写出该晶体的化学式:______。
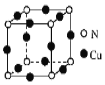
(3)[Cu(NH3)4]2+中配位体的空间结构结构为______
(4)![]() 中N原子轨道的杂化类型是______。与
中N原子轨道的杂化类型是______。与![]() 互为等电子体的一种分子为______(填化学式)。
互为等电子体的一种分子为______(填化学式)。
(5)氨极易溶于水的原因是______。
(6)金属铜的堆积方式如图所示:若该晶胞参数a=658pm,则该晶胞密度为________(列出计算表达式)g·cm-3。
 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应:2A(g)+2B(g)![]() C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是( )
C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,可以使正反应速率v正增大、D的物质的量浓度c(D)增大的是( )
A. 移走少量C B. 扩大容积,减小压强
C. 缩小容积,增大压强 D. 容积不变,充入“惰”气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2mol A和2mol B两种气体混合于2L密闭容器中,发生反应3A(g)+B(g)![]() 2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
(1)生成D的反应速率____________。
(2)B的平衡浓度为________。
(3)A的转化率为________。
(4)该温度下的平衡常数K=___。
(5)如果增大反应体系的压强,则平衡体系中C的转化率___。(填“增大”或“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀。用电离平衡原理解释上述现象。_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气净化中的一个反应如下:
NO(g)+CO(g)![]()
![]() N2(g)+CO2 (g) ΔH=-373.4 kJ·mol-1
N2(g)+CO2 (g) ΔH=-373.4 kJ·mol-1
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是( )
A.  B.
B. 
C.  D.
D. 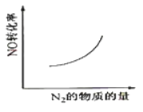
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国研制成功的全球唯一的治疗疟疾特效药——青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示。目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求。下列关于青蒿素的说法正确的是( )
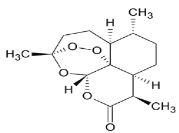
A.是一种烃
B.属于高分子化合物
C.属于芳香族化合物
D.分子式是C15H22O5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com