
【题目】中国研制成功的全球唯一的治疗疟疾特效药——青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示。目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求。下列关于青蒿素的说法正确的是( )
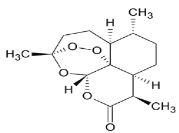
A.是一种烃
B.属于高分子化合物
C.属于芳香族化合物
D.分子式是C15H22O5
科目:高中化学 来源: 题型:
【题目】化合物的知识贯穿整个高中学习,通过《化学反应原理》这本书的学习更是加深了对它们的认识。
(1)亚磷酸是二元弱酸。已知:
![]()
![]()
![]()
求![]()
![]()
![]() ______________
______________
(2)亚磷酸溶液与硝酸银溶液混合生成单质银和NO,写出该反应的离子方程式_________
(3)关于![]() 溶液,下列表达正确的是_____
溶液,下列表达正确的是_____
A.![]()
B.![]()
C.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为VL的密闭容器中存在化学平衡:2NO2(g)![]() N2O4(g),ΔH<0。保持温度不变,将容器体积增大至2V后,下列说法不正确的是( )
N2O4(g),ΔH<0。保持温度不变,将容器体积增大至2V后,下列说法不正确的是( )
A.容器内气体颜色变深B.容器内N2O4分子数减小
C.混合气体的平均相对分子质量增大D.NO2的物质的量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
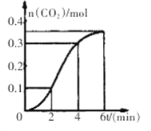
A.反应开始2分钟内平均反应速率最大
B.反应4分钟后平均反应速率最小
C.反应开始4分钟内温度对反应速率的影响比浓度大
D.反应4分钟后反应速率下降的原因是盐酸浓度逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4是一种黑色粉末,又称磁性氧化铁,它的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
Ⅰ.提出假设: 假设1.黑色粉末是CuO;假设2.黑色粉末是Fe3O4;
假设3.黑色粉未是CuO和Fe3O4的混合物
Ⅱ.设计探究实验:
方案一:取少量粉末加入足量稀硝酸,若假设2或假设3成立则实验现象是___________,相关反应的离子方程式为__________________________________。
方案二: 查阅资料: Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若产生___________现象,则假设2成立;若产生___________现象,则假设3成立。
方案三:
学生丙利用下图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:
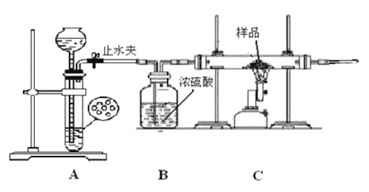
(1)下列实验步骤的先后顺序是___________(填序号)。
①打开止水夹;②关闭止水夹;③点燃C处的酒精喷灯;
④熄灭C处的酒精喷灯 ⑤收集氢气并验纯。
在点燃C处酒精喷灯前要进行的必要操作是__________________________。
(2)假设样品全部参加反应,若实验前样品的质量为4.7克,实验后称得装置C中固体的质量3.6克则假设___________(填“1”“2”或“3”) 正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,下列说法正确的是( )
A.向氨水中加入氯化铵固体,会使溶液的pH增大
B.常温时,向CaCO3的饱和溶液中加入Na2CO3固体,则CaCO3的溶度积常数增大
C.常温下,浓度均为0.1mol·L-1的①醋酸、②盐酸、③醋酸钠溶液,水的电离程度的顺序为③>①>②
D.NaHCO3饱和水溶液中c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验探究反应速率的测定和比较。
[实验步骤]
Ⅰ.取一套装置(装置如下图所示),加入40mL1mol/L的硫酸,测量收集10mLH2所需的时间。
Ⅱ.取另一套装置,加入40mL1mol/L的硫酸,测量收集10mLH2所需的时间。
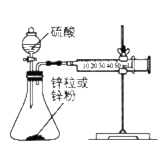
(1)[实验现象]
锌跟硫酸反应产生气泡,收集10mL气体, Ⅱ所用时间比Ⅰ所用时间_____。
(2)[实验结论]
4mol/L硫酸与锌反应比1mol/L硫酸与锌反应速率____。
(3)[注意事项]
a.锌粒的颗粒(即表面积)大小_____;
b.40mL硫酸要迅速加入;
c.装置____,且计时要迅速、准确;
d.气体收集可以用排水量气装置代替。
(4)实验讨论]除本实验测定反应速率的方法外,可行的方案还有(填两条):
a.________;b._______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如图所示:
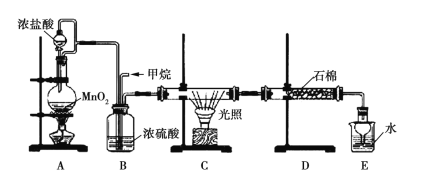
(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置的作用:①______;②______;③______。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_____(填序号)。
A.收集气体 B.吸收氯气 C.吸收氯化氢
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是重要的有机物,可由E和F在一定条件下合成(部分反应物或产物省略,另请注意箭头的指向方向):
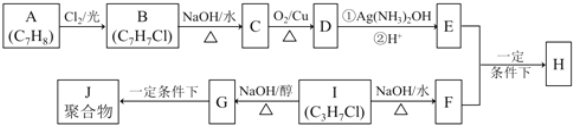
已知以下信息:
i.A属于芳香烃,H属于酯类化合物
ii.I的核磁共振氢谱为二组峰,且峰的面积比为6:1
回答下列问题:
(1) D的含氧官能团名称_________,B的结构简式_________
(2) B![]() C和G
C和G![]() J两步的反应类型________、_________
J两步的反应类型________、_________
(3)E+F![]() H的化学方程式______________
H的化学方程式______________
(4)I![]() G 的化学方程式_______________
G 的化学方程式_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com