
【题目】如图为相互串联的三个装置,试回答:
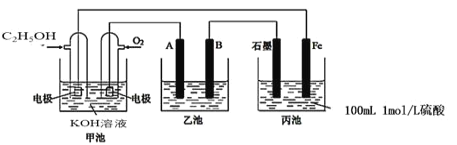
(1)写出甲池负极的电极反应式:________。
(2)若甲池消耗4.6gC2H5OH气体,则丙池中石墨极上生成气体的物质的量为______,反应一段时间后丙池溶液pH_______(填“增大”、“减小”、“不变”)。
(3)若利用乙池在铁片上镀银,则B是_______(填电极材料),电极反应式是______。
(4)若乙池中A、B为石墨电极,电解质溶液为CuCl2。当丙池共产生6.72L(标况)气体时,乙池A极产物_____mol,检验该产物的方法为:______(简述操作)。
【答案】C2H5OH-12e-+16OH-=2CO32-+11H2O 0.3mol 减小 Fe Ag++e-=Ag 0.2 用湿润的淀粉碘化钾试纸靠近A极,若变蓝,说明所产生气体为Cl2
【解析】
(1)在燃料电池中,通入燃料的电极为负极;
(2)与燃料电极连接的为阴极,与O2电极连接的为阳极,在丙池的石墨电极为阳极,溶液中OH-失去电子,发生氧化反应产生O2。先计算乙醇的物质的量,根据其失去电子,结合同一闭合回路中电子转移数目相等,可计算出反应产生氧气的物质的量,结合水的电离平衡判断溶液pH变化;
(3)在铁片上镀银,金属铁作阴极,金属银作阳极材料,选择硝酸银为电解质溶液;
(4)丙池实质是电解水,反应式为2H2O![]() 2H2↑+O2↑,根据气体的体积计算其物质的量,结合方程式确定转移电子数目,在乙池中A电极为阳极,在阳极上产生氯气,利用电子守恒解答,并根据氯气的强氧化性进行检验。
2H2↑+O2↑,根据气体的体积计算其物质的量,结合方程式确定转移电子数目,在乙池中A电极为阳极,在阳极上产生氯气,利用电子守恒解答,并根据氯气的强氧化性进行检验。
(1)在甲池中通入乙醇的电极为负极,乙醇失去电子,被氧化,与溶液中的OH-结合形成CO32-,所以负极的电极反应式为C2H5OH-12e-+16OH-=2CO32-+11H2O;
(2)在丙池中,石墨电极与燃料电池的正极连接,为阳极,Fe电极为阴极。在石墨电极上发生反应:4OH--4e-=2H2O+O2↑,n(C2H5OH)=4.6g÷46g/mol=0.1mol,根据负极的电极反应式C2H5OH-12e-+16OH-=2CO32-+11H2O可知:1mol乙醇反应失去12mol电子,则0.1mol乙醇反应失去1.2mol电子,由于在同一闭合回路中电子转移数目相等,所以丙池中石墨电极上反应产生O2的物质的量是n(O2)=1.2mol÷4=0.3mol;由于溶液中OH-不断放电产生O2,破坏了水的电离平衡,促进了水的电离,使溶液中c(H+)增大,溶液的酸性会逐渐增强,因此反应一段时间后丙池溶液pH减小;
(3)若利用乙池在铁片上镀银,则金属铁是阴极材料,与电源的负极连接,金属银是阳极材料,与电源的正极连接,选择硝酸银为电解质溶液。在甲池中,通氧气的电极是正极,所以乙池中A是阳极,材料是银,B是阴极,材料是铁片,在B电极上发生的电极反应:Ag++e-=Ag;
(4)乙池中A是阳极,发生反应:2Cl- -2e-=Cl2↑,B是阴极,Cu2+获得电子变为单质Cu。丙池共产生标况6.72L气体时,n(气体)=6.72L÷22.4L/mol=0.3mol,在丙池中实质是电解水,方程式是:2H2O![]() 2H2↑+O2↑。根据方程式可知:每反应产生3mol气体,转移电子的物质的量是4mol,则反应产生0.3mol气体,转移电子的物质的量是0.4mol,则根据串联电路中电子转移数目相等,可知在乙池的A电极上反应得到的氯气的物质的量是0.4mol÷2=0.2mol。氯气具有强的氧化性,在溶液中可将I-氧化为I2,I2遇淀粉溶液变为蓝色,故检验氯气的方法是:用湿润的淀粉碘化钾试纸靠近A极,若变蓝,说明所产生气体为Cl2。
2H2↑+O2↑。根据方程式可知:每反应产生3mol气体,转移电子的物质的量是4mol,则反应产生0.3mol气体,转移电子的物质的量是0.4mol,则根据串联电路中电子转移数目相等,可知在乙池的A电极上反应得到的氯气的物质的量是0.4mol÷2=0.2mol。氯气具有强的氧化性,在溶液中可将I-氧化为I2,I2遇淀粉溶液变为蓝色,故检验氯气的方法是:用湿润的淀粉碘化钾试纸靠近A极,若变蓝,说明所产生气体为Cl2。


科目:高中化学 来源: 题型:
【题目】化合物的分子式为C5H11Cl,分析数据表明:分子中有两个—CH3、两个—CH2—、一个![]() 和一个—Cl,它的可能的结构有( )种
和一个—Cl,它的可能的结构有( )种
A.2B.3C.4D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性小组为了探究石蜡油分解产物,设计了如下实验方案。下列说法错误的是
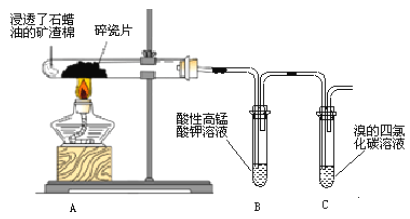
A. 碎瓷片有催化和积蓄热量的作用
B. 结束反应时,先撤出导管,再停止加热
C. 石蜡油是液态烷烃
D. B、C中溶液均褪色,反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4===2PbSO4+2H2O。负极电极反应式为___________________________________________。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu===2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为________,当线路中转移0.2 mol电子时,则被腐蚀铜的质量为________g。
(3)燃料电池是一种高效、环境友好的供电装置,以甲醇做燃料的电池,如下图所示,

①负极反应物是______________,H+从________极到________极(填a或b)。
②正极反应式为_________________,负极反应式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日本冈山大学教授滨田博喜和研究员富良德等通过实验发现,桉树叶子的培养细胞能够消除有害化学物质双酚A的毒性。双酚A的结构简式如下图所示,下列有关此物质的说法正确的是( )

A. 1 mol该物质与足量溴水反应消耗2 mol Br2
B. 该物质能与碳酸氢钠溶液反应放出CO2
C. 该物质的所有碳原子可能在同一平面
D. 该物质与足量氢气发生加成反应后所得物质的化学式为C15H28O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石中不含其他与CO反应的成分),并除去尾气。CO气体用H2C2O4![]() CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
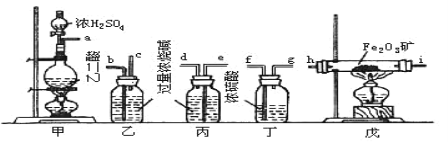
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a、b…表示) 接 , 接 , 接 , 接 。___________________
(2)装置乙的作用是___________________;装置丙的目的是____________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是____________________。
(4)实验前氧化铁矿粉末为xg,实验后测得乙、丙质量分别增加yg和zg,则氧化铁的质量分数为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学中的反应类型较多,请写出下列反应类型。
①苯与浓硝酸共热生成硝基苯__________
②乙醛和新制的银氨溶液反应__________
③乙烯使溴的四氯化碳溶液褪色________
④溴乙烷和氢氧化钠的乙醇溶液共热________
⑤由乙炔制备聚乙炔_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应3A(g)+B(g) ===2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(L·min)、②vC=0.5 mol/(L·min)、③vB=0.5 mol/(L·min),三种情况下该反应速率由大到小的关系是 。(用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
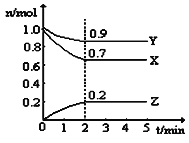
①该反应的化学方程式为__________________________。
②反应开始至2min,以气体Z表示的平均反应速率为 。
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时 (填“大”,“小”或“相等”,下同),混合气体密度比起始时 。
④上述反应,在第2min时,X的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为基本原料可制备X、Y、Z、W等物质,下列有关说法中正确的是( )
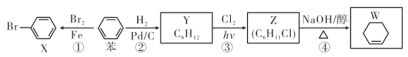
A. 反应①是苯与溴水的取代反应 B. 可用AgN03溶液检测W中是否混有Z
C. X、苯、Y分子中六个碳原子均共平面 D. 反应④中产物除W外还有H2O和NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com