
【题目】标准状况下,某气态烃A的密度是1.25g·L-1,取x L的A在足量的氧气中充分燃烧,生成的混合气体通入到50mLNaOH溶液,随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,产生的CO2气体体积与所加入的盐酸的体积之间的关系如图所示:
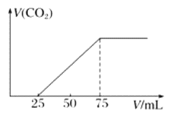
(1)A的摩尔质量为________________。
(2)请计算x的值(写出具体计算过程)。________________
【答案】28g·mol-1 该气态烃的摩尔质量为28g/mol,则该烃为乙烯C2H4,由图可知,当生成CO2气体时,发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,n(NaHCO3)=n(HCl)=0.05L×0.1mol·L-1=0.005mol,根据C元素守恒知,乙烯燃烧生成0.01mol CO2,则n(C2H4)=![]() n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
【解析】
(1)根据公式![]() 进行计算;
进行计算;
(2)先确定该气态烃的分子式,再根据所发生的反应,结合图像,利用元素守恒进行计算。
(1)标准状况下,某气态烃A的密度是1.25g·L-1,则A的摩尔质量为![]() ;
;
(2)该气态烃的摩尔质量为28g/mol,则该烃为乙烯C2H4;取x L乙烯在足量的氧气中充分燃烧,生成二氧化碳和水蒸气,将该混合气体通入到50mLNaOH溶液中,CO2与NaOH溶液反应;随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,生成CO2气体,当生成CO2气体时,应发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,由图可知,生成CO2气体至体积最大,消耗HCl为50mL,则n(NaHCO3)=n(HCl)=0.05L×0.1mol·L-1=0.005mol,根据C元素守恒知,乙烯燃烧生成0.01mol CO2,则n(C2H4)=![]() n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。
n(CO2)=0.005mol,则乙烯的体积为V=nVm=0.005mol×22.4L/mol=0.112L,即x=0.112L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下面的排序不正确的是( )
A.晶体沸点由低到高:CF4<CCl4<CBr4<CI4
B.晶格能由大到小:NaF>NaCl>NaBr
C.硬度由大到小:金刚石>碳化硅>晶体硅
D.熔点由高到低:Na>Mg>Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HA的电离常数Ka=1×10-6,向20 mL浓度为0.01 mol·L-1的HA溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液的pH与加入NaOH溶液的体积之间的关系如图所示,下列说法正确的是( )
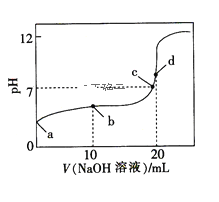
A.a点对应溶液的pH约为4,且溶液中只存在HA的电离平衡
B.b点对应溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-)
C.d点对应溶液中:c(OH-)-c(H+)=c(A-)
D.a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家目前开发出了一种新技术,将能放射出![]() 粒子的砹原子装入形状类似DNA螺旋结构的碳纳米管中,这种肉眼看不见的微型“核弹”可以搜索、确认并定向摧毁身体任何部位的癌细胞.下列有关说法中正确的是( )
粒子的砹原子装入形状类似DNA螺旋结构的碳纳米管中,这种肉眼看不见的微型“核弹”可以搜索、确认并定向摧毁身体任何部位的癌细胞.下列有关说法中正确的是( )
A.放射性At原子中,核外电子与核内中子数之差为133
B.根据元素周期律推知:砹单质是![]() 种有色固体,AgAt是一种不溶于水的固体
种有色固体,AgAt是一种不溶于水的固体
C.类似DNA螺旋结构的碳纳米管是一种高分子化合物
D.构成碳纳米管的微粒直径在![]() 之间,它实际上是一种胶体
之间,它实际上是一种胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值。则下列有关叙述正确的共有
A.1.4g乙烯与丙烯的混合气体含有NA个碳原子
B.精炼铜,若阳极失去2NA个电子,则阴极增重64g
C.在1L 0.1mol/L的Na2CO3溶液中,阴离子总数小于0.1NA
D.将1L 2mol/L的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、Q、T的原子序数与其常见化合价关系如图所示。下列说法正确的是( )
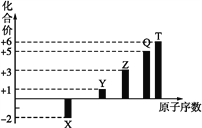
A. 1 mol TX2与足量X2反应生成TX3的分子数目为NA
B. Z元素形成的可溶性盐溶液可能显碱性
C. 1 mol Y2X2与足量H2O反应转移的电子数目为2NA
D. 0.1 mol Q元素的含氧酸在水中电离出的H+数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.![]() 称为拟卤素,性质与卤素相似.下列说法不正确的是( )
称为拟卤素,性质与卤素相似.下列说法不正确的是( )
M | N | ||
X | Y |
A.X位于三周期IIA,其单质可采用电解熔融![]() 制备
制备
B.元素最高价氧化物的水化物中,酸性最强的是![]()
C.气体分子![]() 的电子式为
的电子式为![]()
D.![]() 其与氢氧化钠溶液反应的化学方程式为
其与氢氧化钠溶液反应的化学方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用麻醉药苄佐卡因E和食品防腐剂J的合成路线如下:
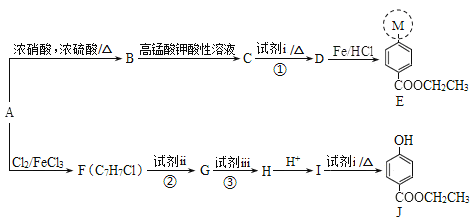
已知:I.M代表E分子结构中的一部分
II.![]()
请回答下列问题:
(1)E中含氧官能团的名称是___。
(2)A属于芳香烃,其结构简式是___。
(3)C能与NaHCO3溶液反应,反应①的化学方程式是___。
(4)反应②、③中试剂ii和试剂iii依次是____。(填序号)
a.高锰酸钾酸性溶液、氢氧化钠溶液 b.氢氧化钠溶液、高锰酸钾酸性溶液
(5)H的结构简式是___。
(6)J有多种同分异构体,其中符合下列条件的同分异构体有___种,写出其中任一种同分异构体的结构简式:___。
a.为苯的二元取代物,其中一个取代基为羟基
b.与J具有相同的官能团,且能发生银镜反应
(7)以A为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(![]() ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在![]() 时,碳酸钙在水中的沉淀溶解平衡曲线如图所示,已知
时,碳酸钙在水中的沉淀溶解平衡曲线如图所示,已知![]() 时硫酸钙的Ksp=9.1×10-6,下列说法正确的是( )
时硫酸钙的Ksp=9.1×10-6,下列说法正确的是( )
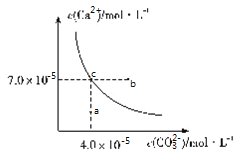
A.除去锅炉水垢中硫酸钙的办法是将其转化为碳酸钙,然后用酸去除
B.图中b点碳酸钙的结晶速率小于其溶解速率
C.通过蒸发,可使溶液由a点变化到c点
D.在25℃时,反应![]() 的平衡常数K=3500
的平衡常数K=3500
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com