
【题目】实验室用硫酸铝酸性溶液制备可溶性的碱式硫酸铝[Ala(SO4)b(OH)c],并用它对烟气进行脱硫处理的过程如图1: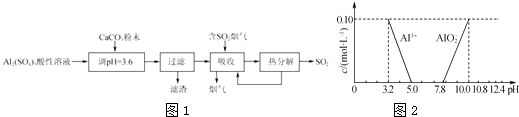
(1)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Ala(SO4)b(OH)c . 过滤时所用的玻璃仪器有、和烧杯,滤渣的主要成分为(填化学式).
(2)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将(填“增大”“减小”或“不变”).
(3)Ala(SO4)b(OH)c中a、b、c的代数关系式为 .
(4)已知在常温下溶液中Al3+、AlO2﹣的浓度与溶液pH的关系如图2所示.为确定碱式硫酸铝的组成,进行如下实验:
①取2.18g碱式硫酸铝样品在空气中灼烧至恒重,样品质量减少了0.36g.
②另取2.18g碱式硫酸铝溶于水,调节溶液的pH到5.0~7.8.
③将②产生的沉淀过滤、洗涤、灼烧至恒重,称量剩余固体为1.02g.
请计算样品中Al3+和SO42﹣的物质的量之比(写出计算过程).
【答案】
(1)漏斗,玻璃棒,CaSO4
(2)溶液中的部分SO32﹣ 被氧化成SO42﹣,减小
(3)3a=2b+c
(4)n(Al3+):n(SO42﹣)=0.02 mol:0.01mol=2:1
【解析】解:根据流程可知,Al2(SO4)3溶液中加入CaCO3调节溶液的pH至3.6,使Al2(SO4)3转化为CaSO4沉淀,过滤得滤渣为CaSO4,滤液中含有铝离子、硫酸根离子等,吸收含有二氧化硫的烟气,在溶液中生成亚硫酸根离子,部分亚硫根离子会被空气氧化成硫酸,将溶液再加热亚硫酸盐分解生成二氧化硫,所得溶液循环利用再用来吸收烟气,
(1)过滤时所用的玻璃仪器有漏斗、玻璃棒、烧杯,通过以上分析知,滤渣的成分是CaSO4;
(2)溶液吸收二氧化硫生成SO32﹣,在溶液中SO32﹣易被氧化生成SO42﹣,所以上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量;溶液中SO32﹣属于弱酸根离子被氧气氧化为转化为SO42﹣,SO42﹣为强酸根离子,则溶液酸性增强,pH减小;
(3)根据化合物中化合价代数和为零可知abc的关系为3a=2b+c;
(4)由步骤①可知n(H2O)=0.36 g/18 gmol﹣1=0.02 mol,所以n(OH﹣)=0.02 mol×2=0.04 mol,
由③可知1.02 g为Al2O3,则n(Al2O3)=1.02 g/102 gmol﹣1=0.01 mol,所以样品中n(Al3+)=0.02 mol 根据电荷守恒可知,样品中n(SO42﹣)=(0.02 mol×3﹣0.04 mol)/2=0.01 mol,所以n(Al3+):n(SO42﹣)=0.02 mol:0.01mol=2:1,
答:样品中Al3+和SO42﹣的物质的量之比为2:1.
故答案为:(1)漏斗、玻璃棒;CaSO4;(2)溶液中的部分SO32﹣ 被氧化成SO42﹣;减小;(3)3a=2b+c;(4)2:1
(1)过滤主要用于固液混合物的分离,所需仪器为铁架台、玻璃棒、烧杯、漏斗;
(2)SO2易溶于水形成H2SO3,而H2SO3易被空气中的氧气氧化成H2SO4;
(3)根据化合物中化合价代数和为0确定三者之间的关系;
(4)①样品减少的质量为H2O的质量;
②产生的沉淀为Al(OH)3;
③灼烧至恒重后,所得的固体为Al2O3。
明确各个数值所代表的物质,再结合相关元素守恒进行计算即可。


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
【题目】第四周期有18种元素,其相关化合物在化工、医药、材料等领域均有着广泛的应用。请回答下列问题:
(1)基态钙原子核外电子云形状为____________,电子占据的最高能层符号是____________。
(2)五氧化二钒(V2O5)是硫酸工业中重要的催化剂,基态钒原子的价电子排布式为____________。
(3)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验Fe2+的试剂,1molCN-中含π键的数目为____________,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是____________。
(4)镓、锗、砷、硒的第一电离能由大到小的顺序为____________(用元素符号表示);其中锗的化合物四氯化锗可用作光导纤维渗杂剂,其熔点为-49.5℃,沸点为83.1℃,则其晶体类型为____________,中心原子的杂化类型为____________;砷酸酸性弱于硒酸,从分子结构的角度解释原因____________;砷化硼是一种新型材料,或成为最好的热导体,其结构与金刚石相似,已知砷化硼晶胞参数为bpm,则该晶体的密度为____________ g ·cm-3。(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定铁铜合金的组成,将7.6g铁、铜合金加入100mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体2.24L(标准状况下),并测得溶液中H+的浓度为0.5molL﹣1 . 若反应前后溶液的体积变化忽略不计,则下列判断正确的是( )
A.上述反应中金属共失去电子0.1 mol
B.合金中,铜的质量为2.8 g
C.原硝酸的浓度:c(HNO3)=4.5 molL﹣1
D.要使溶液中的金属离子完全沉淀,需加5 molL﹣1的NaOH溶液60 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知部分弱酸的电离平衡常数如下表所示:
弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数Ka(25℃) | 1.75×10-5 | 2.98×10-8 | Ka1=4.3×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-7 Ka2=1.02×10-7 |
下列离子方程式正确的是
A. 少量的CO2通入NaClO溶液中:CO2+H2O+2C1O-==CO32-+2HClO
B. 少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-==SO32-+2HCO3-
C. 少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-==CaSO3↓+2HClO
D. 相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-==CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈是地壳中丰度最高的稀土元素,可用作催化剂、合金添加剂,也可用于医药、制革、玻璃、纺织等工业。氟碳铈矿的主要化学成分为CeFCO3,它是提取铈的重要矿物原料。氟碳铈矿的冶炼处理工艺已经发展到十数种,其中一种提取铈的工艺流程如下图所示。

已知:焙烧后烧渣中含+4价的铈及十3价的其他稀土氟化物和氧化物。
请回答下列问题:
(1)CeFCO3中Ce元素的化合价为______。
(2)“焙烧”前将矿石粉碎成细颗粒的目的是___________________________________________。
(3)“酸浸I”步骤中CeO2转化为Ce3+,且产生黄绿色气体,该过程的离子方程式为___________________。
(4)“酸浸1”步骤中CeF4转化为难溶物Ce(BF4)3,加入可溶性钾盐的目的是__________________。
(5)“操作I”后,向溶液中加入NaOH溶液,调节溶液pH可获得Ce(OH)3沉淀,利用pH试纸测定溶液pH值的实验操作是__________________________________。当溶液中离子浓度小于1×10-6mol/L时视为沉淀完全,常温下,加入NaOH调节溶液的pH应大于____[已知Ce(OH)3的Ksp=8.0×10-21,1g2=0.3]。
(6)写出“氧化”步骤的化学方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素组成的单质及化合物间能发生如下图所示的转化,其中甲、乙为单质,A、B、C、D为化合物,B为气体,C为白色沉淀。回答下列问题:

(1)若B为常见的碱性气体,C不溶于NaOH溶液。
①甲的电子式为________________。②写出A→B+C的化学方程式_____________________。
(2)若B为具有臭鸡蛋气味的气体,乙与Fe2O3反应可用于焊接钢轨。
①工业上制取乙的化学方程式为_____________________。
②写出D溶液与过量氨水反应的离子方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素是指每种质量不到体重的万分之一,质量总和不到人体质量的千分之一的近二十种元素,这些元素对人体正常代谢和健康起着重要作用.下列元素不是微量元素的是( )
A.I
B.H
C.Zn
D.Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com