
����Ŀ��һ�������������Ժ�CO2������ӦFe(s)��CO2(g)![]() FeO(s)��CO(g) �÷�ӦΪ���ȷ�Ӧ��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
FeO(s)��CO(g) �÷�ӦΪ���ȷ�Ӧ��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��

(1)t1ʱ�������淴Ӧ���ʵĴ�С��ϵΪ����______����(����>����<������=��)��
(2)4�����ڣ�CO2��ת����Ϊ__________��CO��ƽ����Ӧ����v(CO)��_________��
(3)���������ĸı��ܼ����䷴Ӧ���ʵ���______________(ѡ�����)
�ٽ����¶� �ڼ������۵�����
�۱���ѹǿ���䣬����Heʹ�������������
�ܱ���������䣬����Heʹ��ϵѹǿ����
(4)����������˵��������Ӧ�Ѵ�ƽ�����__________________(ѡ�����)
��v(CO2)��v(CO)
�ڵ�λʱ��������n molCO2��ͬʱ����n mol CO
�� ����������ѹǿ����ʱ����仯
�������������ƽ������������ʱ����仯
���𰸡�> 71.4�� 0.125mol��L-1��min-1 �٢� �ڢ�
��������
(1)t1��CO��CO2Ũ�ȱ仯�ص��ж������淴Ӧ���ʵĴ�С��
(2)����ת����=![]() ��100%����CO2��ƽ��ת���ʣ��������ʶ���ʽ����v(CO)��
��100%����CO2��ƽ��ת���ʣ��������ʶ���ʽ����v(CO)��
(3)����Ӱ�컯ѧ��Ӧ���ʵ�������Ũ�ȡ��¶ȡ�ѹǿ������������������С�ȷ�����
(4)���淴Ӧ�ﵽƽ��ʱ���κ�һ��ֵ����ʵ�����Ũ�Ȳ��䣬���ʵĺ������䣬��Ӧ���ʲ��䣬�ݴ˷������
(1)�ؼ�ͼ���֪����t1��COŨ������CO2Ũ�ȼ�С��˵����Ӧδ�ﵽƽ�⣬������У����V��>V����
(2)����ͼ���֪���ڷ�Ӧ��ʼʱ������CO2Ũ����0.7mol/L��ƽ��ʱCO2Ũ����0.2mol/L����Ӧת����Ũ����0.5mol/L������CO2��4�����ڣ��ﵽƽ��ʱ��ת����Ϊ![]() ��100%=
��100%=![]() ��100%=71.4�������ݻ�ѧ��Ӧ���ʵĶ���ʽ��֪��4������CO��ƽ����Ӧ����v(CO)=
��100%=71.4�������ݻ�ѧ��Ӧ���ʵĶ���ʽ��֪��4������CO��ƽ����Ӧ����v(CO)=![]() =0.125mol��L-1��min-1��
=0.125mol��L-1��min-1��
(3)�ٽ����¶ȣ����ʵ����ܽ��ͣ����������С����Ч��ײ�������٣���ѧ��Ӧ���ʽ��ͣ��ٷ������⣻
�����ڹ����Ũ�Ȳ��䣬���Լ������۵����������ʵķ�Ӧ���ʲ��䣬�ڲ��������⣻
�۱���ѹǿ���䣬����Heʹ�������������Ӧ��ϵ������Ũ�Ƚ��ͣ���λ����ڻ���������٣���Ч��ײ�������٣���ѧ��Ӧ���ʽ��ͣ��۷������⣻
�ܱ���������䣬����Heʹ��ϵѹǿ����������ϵ�ڵ�����Ũ�Ȳ��䣬���Ի�ѧ��Ӧ���ʲ��䣬�ܲ��������⣻
�ʺ���ѡ���Ǣ٢ۣ�
(4)��δָ����Ӧ��������������У���˲����ж��Ƿ�Ϊƽ��״̬���ٴ���
�ڵ�λʱ��������n molCO2��ͬʱ��Ȼ������nmolCO��������n mol CO����CO�����ʵ������䣬��Ӧ�ﵽƽ��״̬������ȷ��
�۸÷�Ӧ�Ƿ�Ӧǰ�������������ķ�Ӧ���κ���������ϵ��ѹǿ�����䣬��˲��ܾݴ��жϷ�Ӧ�Ƿ�Ϊƽ��״̬���۴���
�ܷ�Ӧǰ�������������䣬������������ᷢ���仯���������Ħ�������ᷢ���仯������Ħ����������g/molΪ��λʱ����ֵ�ϵ������ʵ���Է��������������������������ƽ������������ʱ����仯����Ӧ�ﵽƽ��״̬������ȷ��
�ʺ���ѡ���Ǣڢܡ�


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д� ��Ȥ����¹�֪��ϵ�д�
��Ȥ����¹�֪��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������£�0.5mol �״�(CH3OH)����������ȫȼ������CO2��Һ̬ˮ���ų��� ��363.3kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ_____________��
��2�������һ��ȼ�ϵ�أ��������ҺΪǿ����Һ��Pt ���缫���ڵ缫�Ϸֱ�ͨ��CO��������ͨ�� CO�ĵ缫ӦΪ_______��(����������������)���õ缫�Ϸ����ĵ缫��ӦʽΪ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������д��ڵ���ƽ�⣺H2S![]() H++HS-��HS-
H++HS-��HS-![]() H++S2-����֪��ʽ��NaHS��Һ�ʼ��ԣ�����10mlŨ��Ϊ0.1mol/L���������м����������ʣ������ж���ȷ����
H++S2-����֪��ʽ��NaHS��Һ�ʼ��ԣ�����10mlŨ��Ϊ0.1mol/L���������м����������ʣ������ж���ȷ����
A. ��ˮ����ʹƽ�������ƶ�����Һ��������Ũ������
B. ����20mlŨ��Ϊ0.1mol/L NaOH��Һ����c(Na+)=c(HS-)+c(H2S)+2c(S2-)
C. ͨ�����SO2���壬ƽ�������ƶ�����ҺpHֵʼ������
D. ����10mlŨ��Ϊ0.1mol/L NaOH��Һ����c(Na+)>c(HS-)>c(OH��)>c(H+)>c(S2-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����������21���͵���Դ��������Ҫ��������Ϊ�뵼����ϵĹ���̫���ܷ�������о�����Ҫ�����á����й��ڹ��˵���д������
A.��Ȼ���й�Ԫ�صĴ����ḻB.��Ȼ���д��ڴ����ĵ��ʹ�
C.�ߴ��ȵĹ豻���������оƬD.����H2�ڸ����»�ԭSiCl4�ķ����õ��ߴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦA2(g)��2B2(g)![]() 2AB2(g) ��H<0������˵����ȷ���ǣ� ��
2AB2(g) ��H<0������˵����ȷ���ǣ� ��
A. �ﵽƽ��������¶Ȼ�����ѹǿ�������ڸ÷�Ӧƽ�������ƶ�
B. �ﵽƽ������¶Ȼ��Сѹǿ�������ڸ÷�Ӧƽ�������ƶ�
C. �����¶������ڷ�Ӧ�������ӣ��Ӷ����̴ﵽƽ���ʱ��
D. �����¶ȣ�����Ӧ�������ӣ�����Ӧ���ʼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(NOCl���۵���-64.5 �棬�е���0.5 �棬�ж�)��������һ�ֻ�ɫ��������ˮ��ˮ�⡣�����ںϳ���������ý�����м���ȡ�ʵ���ҿ���������һ�������ڳ��³�ѹ�ºϳɣ�����Һ̬������

��1�������ͬѧ���Ʊ�ԭ����NO��Cl2����������ͼ�Ʊ�װ��:
��д��NOCl��NԪ�ػ��ϼۣ�_______
��Ϊ�Ʊ�����������������±���ȱ�ٵ�ҩƷ�ǣ���д�ں����ϣ�:
ʵ����Ŀ | װ���� | װ���� | |
�Ʊ������� | ��ƿ�� | ��Һ©���� | |
a .�Ʊ����������Cl2 | MnO2 | _______ | _______ |
b .�Ʊ����������NO | Cu | _______ | _______ |
��2������ͬѧ���ü����Ƶõ�NO��Cl2�Ʊ�NOCl��װ����ͼ��ʾ:
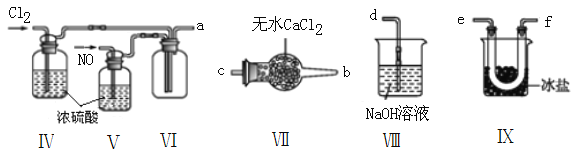
��װ������˳��Ϊa��____________________________(�������������ҷ�������Сд��ĸ��ʾ)��
��װ�����������ɽ�һ������NO��Cl2������һ��������______________________________��
��װ�â���ʵ����������װ��ǰ��Ӧ�������Ĵ�����_________________________��
��װ����������β��ʱ��NOCl�����ķ�������ԭ��Ӧ�Ļ�ѧ����ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������1LH2SO4��HNO3�Ļ����Һ����H2SO4��HNO3���ʵ���Ũ�ȴ������¹�ϵ��c(H2SO4)+c(HNO3)=1.2mol��L-1����������������ܽ�ͭ�����ʵ���Ϊ
A. 0.80mol 0.72molB. 0.45molC. 0.40mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ������������ַ�Ӧ�ϳɼ״���
��Ӧ��CO(g)+2H2(g) ![]() CH3OH(g)����H1
CH3OH(g)����H1
��Ӧ��C02(g)+3H2(g) ![]() CH30H(g)+ H2O(g)����H2
CH30H(g)+ H2O(g)����H2
�±����������Ƿ�ӦI�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
�¶� | 250�� | 300�� | 350�� |
K | 2.O | 0.27 | 0.012 |
��1���ɱ��������ж���H1_____0(�>������<����=��)��Ӧ��C02(g)+H2(g)![]() CO(g)+H20(g) ��H3=____(����H1����H2��ʾ)��
CO(g)+H20(g) ��H3=____(����H1����H2��ʾ)��
��2���������ݻ����䣬���д�ʩ����߷�Ӧ����COת���ʵ���_________(ѡ��ĸ)��
a������CO��ʹ��ϵ��ѹǿ����
b����CH3OH(g)����ϵ�з���
e������He��ʹ��ϵ��ѹǿ����
d��ʹ�ø�Ч����
��3��д����Ӧ��Ļ�ѧƽ�ⳣ������ʽ��K=_________�����ֺ��º��ݵ������½���Ӧ���ƽ����ϵ������Ũ�Ⱦ�����һ������ѧƽ��_________(�������������)�ƶ���ƽ�ⳣ��K____(��������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�±�ص�˵������ȷ����
A. ICl�ڷ�ӦICl+2NaOH![]() NaCl+NaIO+H2O����������
NaCl+NaIO+H2O����������
B. ��������������Ӧ�����Ȼ��ƺ���ṹ���ȶ�����ǿ����ϵ����������
C. ���۵⻯���ڿ����б�����������4I-+ O2 + 2H2O![]() 2I2 + 4OH-
2I2 + 4OH-
D. HF��HCl��HBr��HI�����ȶ������μ�������ԭ��������ǿ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com