
 ①上述合成甲醇的反应为
①上述合成甲醇的反应为| n |
| 1-n |
| 3 |
| 1 |
| 3 |
| 4 |
| 0.75 |
| 2×5 |
| 0.375×0.375 |
| 0.125×0.125 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、达平衡时,A的物质的量浓度2.0 mol/L |
| B、达平衡时,B的转化率20% |
| C、此5s内D的平均反应速率为0.2 mol?L-1?min-1 |
| D、x≥3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热、加压 |
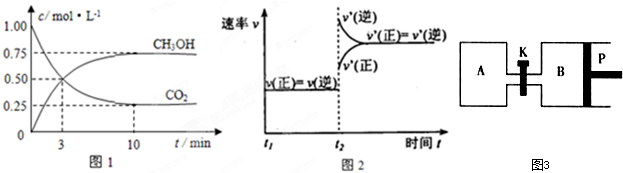
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
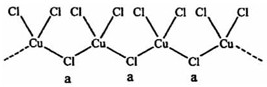
查看答案和解析>>
科目:高中化学 来源: 题型:
 按如图装置进行实验,并回答下列问题:
按如图装置进行实验,并回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com