
����Ŀ���ۺ��Ȼ���[Fe2(OH)nCl6-n]m���PFC����һ������Ч�����߷��Ӿ�ˮ������FeCl2��4H2OΪԭ�ϣ�����ϡ���Ტ����������NaNO2����������ˮ�⡢�ۺϵȲ��裬���Ʊ�PFC��
(1)��ϡ�����У�NaNO2����Fe2+��Ӧ����һ����ɫ����M������M�Ը÷�Ӧ�д����ã����ԭ����ͼ��ʾ�� M�Ļ�ѧʽΪ______�� Fe2+�����������±�O2���������ӷ���ʽΪ_______��

(2)�λ���[B��![]() �� 100%]�Ǻ�����ˮ�����ӵ�һ����Ҫָ�ꡣ�λ���ԽС����ˮ����ˮpH�仯��Ӱ��______��(����Խ��������ԽС��������Ӱ����)
�� 100%]�Ǻ�����ˮ�����ӵ�һ����Ҫָ�ꡣ�λ���ԽС����ˮ����ˮpH�仯��Ӱ��______��(����Խ��������ԽС��������Ӱ����)
(3)PFC��Ʒ���λ���(B)�IJⶨ��
��֪��PFC��Ʒ���ܶ��� = 1.40 g��mL1����Ʒ����������������(Fe) = 16%
����1��ȷ��ȡ1.00 mL PFC��Ʒ������ƿ�С�
����2������һ�����0.05000 mol��L1���������Һ�����¾��ú���һ������ķ�������Һ(��Fe3+��Ӧ������Fe3+��ʵ��ĸ���)���μ����η�̪��ָʾ����������0.05000 mol��L1�������Ʊ���Һ�ζ����յ㣬�����������Ʊ���Һ13.00 mL��
����3��ȷ��ȡ1.00 mL����ˮ��Ʒ������ƿ�У��ظ�����2�����������������Ʊ���Һ49.00 mL��
��������ʵ�����ݼ���PFC��Ʒ���λ���(B)(д���������)_______��
���𰸡�NO 4Fe2++ O2+ 4H+= 4Fe3++ 2H2O Խ�� ��Ʒ��OH�����ʵ���Ũ�ȣ� n(OH)�� n1(NaOH) n2(NaOH)�� 0.05000 mol��L1�� (49.00 13.00) �� 103L��1.8 �� 103mol��
c(OH)��![]() ��
�� ![]() ��1.8 �� 103mol��L1��
��1.8 �� 103mol��L1��
��Ʒ��Fe3+�����ʵ���Ũ�ȣ� c(Fe3+)��![]() ��
��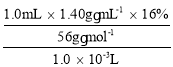 ��4.0 �� 103mol��L1��
��4.0 �� 103mol��L1��
B��![]() �� 100% ��
�� 100% ��![]() �� 100%�� 15%��
�� 100%�� 15%��
��������
(3)�õζ�ʵ��ʱ�ⶨPFC��Ʒ�е��λ��ȣ��λ���B��![]() �� 100%���ȸ�����Ʒ���ܶȡ�������������������ȡ��Ʒ��Fe3+��Ũ�ȣ�Ȼ�����һ��������������Һ��ַ�Ӧ������KF����Fe3+��ʵ��ĸ��ţ�֮�����������Ʊ�Һ�ζ�ʣ����������������������ˮ�ظ��������ζ�����������Һ��������������ȥʣ�������ɵõ���Ʒ�����������ĵ������������
�� 100%���ȸ�����Ʒ���ܶȡ�������������������ȡ��Ʒ��Fe3+��Ũ�ȣ�Ȼ�����һ��������������Һ��ַ�Ӧ������KF����Fe3+��ʵ��ĸ��ţ�֮�����������Ʊ�Һ�ζ�ʣ����������������������ˮ�ظ��������ζ�����������Һ��������������ȥʣ�������ɵõ���Ʒ�����������ĵ������������
(1)��ϡ�����У�NaNO2�ὫFe2+������Fe3+���ù�����NaNO2Ӧ��Ϊ����������ͼ��֪��M��Fe2+��������Fe(NO)2+����Ԫ�ػ��ϼ�û�б仯����NԪ�ػ��ϼ�Ҳ���䣬����MӦΪNO��Fe2+�����������±�O2������Ӧ����Fe3+�����ݵ����غ��Ԫ���غ�ɵ����ӷ���ʽӦΪ4Fe2++ O2+ 4H+= 4Fe3++ 2H2O��
(2)�λ���B��![]() �� 100%���λ���ԽС��[Fe2(OH)nCl6-n]m��n��ֵԽС����c(OH��)ԽС�����ɵ�Fe(OH)3�������Խ�٣���Һ��c(Fe3+)Խ��ˮ��Ч��Խǿ����ˮpH�仯��Ӱ��Խ��
�� 100%���λ���ԽС��[Fe2(OH)nCl6-n]m��n��ֵԽС����c(OH��)ԽС�����ɵ�Fe(OH)3�������Խ�٣���Һ��c(Fe3+)Խ��ˮ��Ч��Խǿ����ˮpH�仯��Ӱ��Խ��
(3)���ݷ�������Ʒ��OH�����ʵ���Ũ�ȣ� n(OH)�� n1(NaOH) n2(NaOH)�� 0.05000 mol��L1�� (49.00 13.00) �� 103L��1.8 �� 103mol��c(OH)��![]() ��
�� ![]() ��1.8 �� 103mol��L1��
��1.8 �� 103mol��L1��
��Ʒ��Fe3+�����ʵ���Ũ�ȣ�c(Fe3+)��![]() ��
��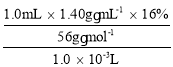 ��4.0 �� 103mol��L1��
��4.0 �� 103mol��L1��
B��![]() �� 100% ��
�� 100% ��![]() �� 100%��
�� 100%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ�����·�Ӧ�ɻ��������Դ������(![]() )������˵������ȷ����
)������˵������ȷ����
��![]()
![]()
��![]()
![]()
��![]()
![]()
��![]()
![]()
A. ��Ӧ�١���Ϊ��Ӧ���ṩԭ����
B. ��Ӧ��Ҳ��![]() ��Դ�����õķ���֮һ
��Դ�����õķ���֮һ
C. ��Ӧ![]() ��
��![]()
D. ��Ӧ![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���۶Ա��������Ҷ�����(PET)�׳Ƶ�����֬����һ����Ҫ���л��߷��Ӳ��ϡ���ṹΪ �������л���A�ϳ�PET��·������ͼ��ʾ:
�������л���A�ϳ�PET��·������ͼ��ʾ:

��֪:��![]() ����
���� ��
��
��������ش���������:
��1��A��������_______,C���������ŵ�������_______��
��2����1,3-����ϩ���Ʊ�˳ʽ��1,3-����ϩ��д��˳ʽ��l,3-����ϩ�Ľṹ��ʽ_______��
��3��A��D��B��C�ķ�Ӧ���ͷֱ�Ϊ_______ ��_______��
��4��д��C+F��PET�Ļ�ѧ��Ӧ����ʽ______________��
��5��G��F��ͬϵ�����Է���������F��28,G�ĺ˴Ź�������������壬�������Ϊ3:1:1,����ϸ�������G��ͬ���칹�干��_____�֡�
��6�����������ϳ�·�ߣ���1,3-����ϩΪԭ��(���Լ���ѡ)������Ʊ�������( )�ĺϳ�·��_______________��
)�ĺϳ�·��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������vtͼ������������ı�Կ��淴ӦA(g)��3B(g) ![]() 2C(g) ��H<0��Ӱ�졣�÷�Ӧ��������ʱ��Ĺ�ϵ��ͼ��ʾ��
2C(g) ��H<0��Ӱ�졣�÷�Ӧ��������ʱ��Ĺ�ϵ��ͼ��ʾ��

�ɼ���t1��t3��t5��t7ʱ��Ӧ���ﵽƽ�⣬���t2��t4��t6��t8ʱ��ֻ�ı���һ����Ӧ�����������ж�t2��t4��t6��t8ʱ�ı��������ж���ȷ����
A. ʹ���˴���������ѹǿ����С��Ӧ��Ũ�ȡ������¶�
B. �����¶ȡ���Сѹǿ����С��Ӧ��Ũ�ȡ�ʹ���˴���
C. ����Ӧ��Ũ�ȡ�ʹ���˴�������Сѹǿ�������¶�
D. �����¶ȡ���Сѹǿ������Ӧ��Ũ�ȡ�ʹ���˴���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫���巴Ӧ�������ڲⶨ�����ʵĺ�����˫���巴Ӧ��ԭ���ɱ�ʾ���£�

˫���� �Ϻ�ɫ������
(1)Cu2+�Ļ�̬��������Ų�ʽΪ_______��
(2)��H2O��Ϊ�ȵ������һ��������Ϊ_______(�ѧʽ)��
(3)˫��������е�ԭ�ӹ�����ӻ�������_______��1 mol˫��������к�����������ĿΪ_______��
(4)���Ϻ�ɫ�������е���λԭ��Ϊ_______��
(5)Cu3Au�ľ�������ͼ��ʾ��Cu3Au������ÿ��ͭԭ����Χ���������ͭԭ����ĿΪ_______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�������������Ũ����ķ�����ȡ������ʵ�飬��ʵ��װ������ͼ��
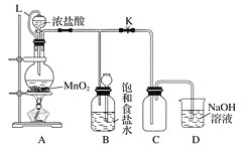
(1)д��Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽ��___________________________________��
(2)����������Ķ���������20 mL 12 mol��L��1�������ϼ��ȣ���ַ�Ӧ�����ɵ�������������0.06 mol������Ҫ��ԭ���Т�______________________����_________________��
(3)L��������____________________��B��������_________________��
(4)Ϊ�����Ũ����������ʣ����ʵ��Ľ�����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݺ����Ƽ�ԭ���Ʊ�����NaHCO3��ʵ�飬������ȡ��������ȡNaHCO3������NaHCO3������NaHCO3�ĸ����衣ͼʾװ�ú�ԭ������������
A.��ȡ����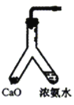 B.��ȡNaHCO3
B.��ȡNaHCO3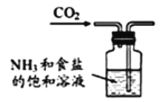
C.����NaHCO3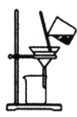 D.����NaHCO3
D.����NaHCO3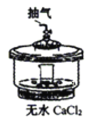
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ֱ��ʾ�йط�Ӧ�ķ�Ӧ�����������仯�Ĺ�ϵ���ݴ��ж�����˵����ȷ����
A. ʯīת��Ϊ���ʯ�ķ�Ӧ�����ȷ�Ӧ
B. ���ױȺ����ȶ�
C. S(g)��S(s)����H>0
D. H2(g)��I2(g)![]() 2HI(g)����H>0
2HI(g)����H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A.��״���£�22.4LNO��22.4LO2��Ϻ�ķ�������Ϊ2NA
B.0.1molL-1�İ�ˮ�У���Һ�и��������ʵ����������¹�ϵ��n(![]() )+n(NH3)+n(NHH2O)=0.1mol
)+n(NH3)+n(NHH2O)=0.1mol
C.��֪��������ֵΪ143kJg-1�����������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��H2(g)��![]() O2(g)=H2O(l) ��H��-286kJmol1
O2(g)=H2O(l) ��H��-286kJmol1
D.�����Ը��������Һ������ͷȼ�ղ�����SO2���壬��10mL0.1molL-1�����Ը��������Һ�պ���ɫʱ��ת�Ƶĵ�������Ϊ0.0025NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com