
【题目】回答下列问题:
(1)实验室在临时配制一些氯化铁溶液时,常将氯化铁固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,是为了_________________(填“促进”、“抑制”)水解。氯化铁水溶液呈______(填“酸”、“中”、“碱”)性,常温时的pH _____7(填“>”、“=”、“<”),原因是(用离子方程式表示):______________________________。
(2)常温下,pH=2的某酸HnA(A为酸根)与pH=12的某碱B(OH)m等体积混合,恰好反应生成正盐,混合溶液的pH=10.反应生成正盐的化学式为___________ ,该盐中___________(填离子符号)一定能水解,其水解的离子方程式为____________________.
【答案】抑制酸<Fe3++3H2O![]() Fe(OH)3+3H+BnAmAn-An- + H2O
Fe(OH)3+3H+BnAmAn-An- + H2O ![]() HA(n-1)— +OH--
HA(n-1)— +OH--
【解析】
(1)氯化铁为强酸弱碱盐,铁离子水解导致溶液呈酸性;
(2)pH=2的某酸HnA(A为酸根)与pH=12的某碱B(OH)m等体积混合生成正盐,说明酸中氢离子的总物质的量和碱中氢氧根离子的总物质的量相等,其盐溶液呈碱性,说明碱的电离程度大于酸的电离程度,根据化合物中化合价的代数和为0确定其化学式,根据酸碱的相对强弱确定水解的离子。
(1)氯化铁是弱酸强碱盐,铁离子易水解,为防止铁离子水解,配制氯化铁溶液时先将氯化铁固体先溶于较浓的盐酸中,抑制其水解,然后再用蒸馏水稀释到所需的浓度;
铁离子水解导致溶液呈酸性,pH <7,水解离子方程式为Fe3++3H2OFe(OH)3+3H+ ,
因此,本题正确答案是:抑制;酸;<;Fe3++3H2OFe(OH)3+3H+;
(2)HnA中A的化合价是-n价,B(OH)m中B的化合价是+m价,根据化合物中化合价的代数和为0知,二者的离子个数之比为n:m,则其化学式为:BnAm,
因此,本题正确答案是:BnAm;
根据题意知,其正盐溶液呈碱性,说明碱的电离程度大于酸的电离程度,生成的盐是强碱弱酸盐,则An-离子一定能水解,其水解方程式为:An- + H2O HA(n-1)— +OH--,
因此,本题正确答案是:An-;An- + H2O HA(n-1)— +OH--。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,一定体积的容器中发生反应:A(s)+3B(g)![]() 2C(g)+2D(g),下列描述中能说明该反应达到平衡的是
2C(g)+2D(g),下列描述中能说明该反应达到平衡的是
①A的质量不发生变化 ②单位时间内生成a mol A,同时消耗2a mol C
③容器中的压强不再变化 ④混合气体的密度不再变化
⑤n(A):n(B):n(C):n(D)=1:3:2:2 ⑥B的浓度不变
A. ②③⑤⑥ B. ①③④⑥ C. ②④⑤ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院深圳先进技术研究院成功研发了一种高效低成本储能电池——“铝一石墨”双离子电池,电池总反应为Al+xC+Li++PF6 -![]() AlLi+Cx PF6下列有关该电池的说法正确的是
AlLi+Cx PF6下列有关该电池的说法正确的是
A. 放电时,PF6-向正极移动
B. 放电时,负极反应为A1-3e-====Al3+
C. 充电时,两个电极增加的质量相等
D. 充电时,阳极反应为xC+PF6--e-==CxPF6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷(C8H8)其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是

A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氯代物1种、二氯代物有3种
C. 立方烷是苯(C6H6)的同系物,也是苯乙烯(C6H5-CH=CH2)的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴、镍具有相似的性质,在化学上称为铁系元素。回答下列问题:
(1)LiCoO2、 LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为_________,第四电离能I4(Co) _________I4(Fe)(填“>”或“<”),PO43-的空间构型为_________。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。
与CO互为等电子体的分子和离子分别为_________和_________(各举一种,填化学式);在CO分子中,键与π键数目之比为_________。
(3)铁与K2O、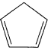 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为_________。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;从各种性质看,都表明它是典型的_________化合物。
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为_________。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;从各种性质看,都表明它是典型的_________化合物。
(4)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。
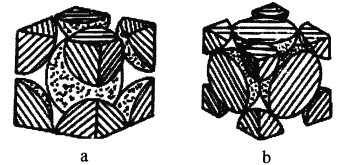
在图a所示堆积方式里铁原子的半径为rpm,则其晶胞棱长为_________cm。
在图b所示堆积方式里铁原子的总体积占晶体体积的比例为_________(用含圆周率π的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些芳香族化合物的分子式均为C7H8O,其中与FeCl3溶液混合后,显紫色和不显紫色的种类分别为( )
A.2种和1种B.2种和3种C.3种和2种D.3种和1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑.在b中小心加入4.0mL液态溴.向a中滴入几滴溴,有白雾产生,继续滴加至液溴滴完.装置c的作用是_________,三颈烧瓶中反应的化学方程式为_____________________;

(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.NaOH溶液洗涤的作用是__________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是_________;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为____________,要进一步提纯,下列操作中必须的是_________________;(填入正确选项前的字母)
A.结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是____________。(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应由两步反应A![]() B
B![]() C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)。下列有关叙述正确的是
C构成,反应过程中的能量变化曲线如图(E1、E3表示两反应的活化能)。下列有关叙述正确的是

A. 三种化合物的稳定性顺序:B﹤A﹤C
B. 两步反应均为放热反应
C. 加入催化剂不改变反应的焓变,但能提高产率
D. 整个反应的ΔH=E1-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期;C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙;A原子的最外层电子数比次外层电子数多3个;D周期序数等于D原子最外层电子数;E原子半径是同周期中最小的(除稀有气体外),根据以上信息回答下列问题:
(1)A元素在周期表中的位置__________________;
(2)乙物质中存在的化学键类型是______________;
(3)写出C与D的最高价氧化物对应的水化物相互间反应的离子方程式_____________;
(4)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的有效成分的电子式为_______________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com