
【题目】有一瓶澄清的溶液,其中可能含有 H+、NH4+、Na+、Al3+、Fe3+、I-、NO3- 、CO32-、SO42- 、AlO2-。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③该溶液的焰色反应没有黄色;
④当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。
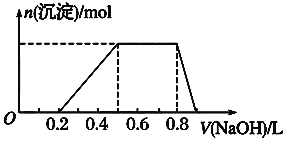
(1)该溶液中肯定含有的离子是_________________________,已确定阳离子的物质的量之比为_______________________。
(2)肯定不含的离子是_________________________________。
(3)不能确定的离子是_________,如何证明该离子是否存在?__________。
(4)请写出沉淀溶解过程的离子方程式____________________________。
【答案】H+、![]() 、Al3+、I-c(H+): c(
、Al3+、I-c(H+): c(![]() ) : c(Al3+)=2:3:1Na+、Fe3+、
) : c(Al3+)=2:3:1Na+、Fe3+、![]() 、
、![]() 、
、![]()
![]() 取溶液少量于试管中,向其中加入足量盐酸,无明显现象,再加几滴BaCl2溶液,产生白色沉淀,则证明含有
取溶液少量于试管中,向其中加入足量盐酸,无明显现象,再加几滴BaCl2溶液,产生白色沉淀,则证明含有![]() ,反之没有Al(OH)3+OH-=
,反之没有Al(OH)3+OH-= ![]() + 2H2O
+ 2H2O
【解析】
①.用pH试纸检测,溶液呈强酸性,说明溶液中存在H+,则一定不存在CO32-、AlO2-;②.取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色,说明溶液中一定含有I-,则一定不含有Fe3+、NO3-;③.该溶液的焰色反应没有黄色,则一定不含Na+;④.另取溶液适量,逐滴加入NaOH溶液,由图可知,先发生H++OH-=H2O,再发生Al3++3OH-= Al(OH)3↓,然后发生NH4++OH-=NH3·H2O,最后发生Al(OH)3+OH-=AlO2-+2H2O,则原溶液中含NH4+、Al3+。
(1).由上述分析可知,原溶液中一定含有H+、NH4+、Al3+、I,由H++OH-=H2O、Al3++3OH-= Al(OH)3↓、NH4++OH-=NH3·H2O并结合图象可知,消耗NaOH的体积分别为0.2L、0.3L、0.3L,阳离子的物质的量之比为c(H+):c(NH4+):c(Al3+)=2:3:1,故答案为:H+、NH4+、Al3+、I;c(H+):c(NH4+):c(Al3+)=2:3:1;
(2).由上述分析可知,溶液中肯定不含的离子是Na+、Fe3+、NO3、CO32、AlO2,故答案为:Na+、Fe3+、NO3、CO32、AlO2;
(3).根据上述分析,不能确定溶液中是否含SO42,证明该离子是否存在的实验方法为:取溶液少量于试管中,向其中加入足量盐酸,无明显现象,再加几滴BaCl2溶液,产生白色沉淀,则证明含有SO42,反之没有SO42,故答案为:SO42;取溶液少量于试管中,向其中加入足量盐酸,无明显现象,再加几滴BaCl2溶液,产生白色沉淀,则证明含有SO42,反之没有;
(4).沉淀溶解过程的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O。


科目:高中化学 来源: 题型:
【题目】在25℃、101kPa条件下,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.7 kJ·mol-1能自发进行的原因是( )
A. 该反应是吸热反应B. 该反应是放热反应
C. 该反应是熵减小的反应D. 该反应的熵增效应大于能量效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列叙述错误的是
A. 18g H2O中含的质子数为10NA
B. 12g 金刚石含有的共价键数为4NA
C. 28g N2中含有π键总数为2NA
D. 1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,该工艺流程如图所示,下列叙述不正确的是( )

A. 该过程中可得到化工产品H2SO4
B. 该过程中化合价发生改变的元素为Fe和S
C. 该工艺流程是除去煤燃烧时产生的SO2
D. 图中涉及的反应之一为Fe2(SO4)3+SO2 + 2H2O=2FeSO4+2H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”。下列错误的是( )
A. 煤、石油和天然气都属于碳素燃料B. 发展太阳能经济有助于减缓温室效应
C. 太阳能电池将太阳能直接转化为电能D. 菠菜蛋白质“发电”不属于“太阳能文明”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
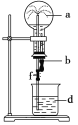
【题目】在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
a(干燥气体) | b(液体) | |
A | NO | 水 |
B | CO2 | 4 mol/L NaHCO3溶液 |
C | Cl2 | 饱和NaCl水溶液 |
D | NH3 | 1 mol/L盐酸 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修5:有机化学基础]扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F的路线如下:

(1)A可发生银镜反应,且具有酸性,A的结构简式为____________。B的分子式为C6H6O,则A与B所发生反应的类型为___________。
(2)C生成D的化学方程式为_____________________________。E是由2分子C生成的含有3个六元环的化合物,E的结构简式为______________。
(3)1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为_______mol。符合下列条件的F的同分异构体(不考虑立体异构)共有______种。
①苯环上只有2个取代基且处于对位,其中一个是羟基;
②在稀H2SO4中或NaOH溶液中加热均能发生水解反应;
③能发生银镜反应。
(4)已知:R—CH2—COOH![]()
![]() ,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
H2C===CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com