
【题目】下列物质转化在给定条件下能实现的是( )
①FeS2 ![]() SO3
SO3![]() H2SO4→CO2
H2SO4→CO2
②Al2O3![]() NaAlO2(aq)→Al(OH)3
NaAlO2(aq)→Al(OH)3
③NaCl(aq)![]() Na→NaOH(aq)
Na→NaOH(aq)
④Fe![]() FeSO4(aq)→Fe(OH)2
FeSO4(aq)→Fe(OH)2![]() Fe2O3
Fe2O3
⑤海水 ![]() 母液
母液 ![]() NaBrNaBrO3
NaBrNaBrO3![]() 粗溴
粗溴![]() Br2
Br2
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
科目:高中化学 来源: 题型:
【题目】利用下图流程可制备1,4-环己二醇,试回答:
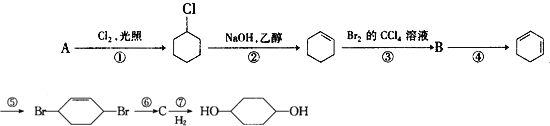
(1)反应①、②、③分别属于___、____、___。(填反应类型)
(2)化合物![]() 中所含官能团的名称为_______和________。
中所含官能团的名称为_______和________。
(3)写出下列化合物的结构简式:A_________,C________。
(4)反应④所用的试剂和条件为_________________。
(5)写出下列反应的化学方程式:反应①_____________;反应④_______________。
(6)请写出以CH3CH2Br为原料制备HOCH2CH2OH的合成路线流程图[无机试剂任用,合成路线流程图示例见本题]。________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是配制一定物质的量浓度溶液的过程示意图。下列说法中错误的是( )
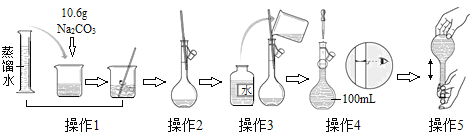
A.所配制的Na2CO3溶液的物质的量浓度为1.0 mol · L-1
B.操作2是将溶解并放置至室温的Na2CO3溶液转移到容量瓶中
C.操作4如果仰视,会使配得溶液的浓度偏低
D.操作5中,定容摇匀后发现液面低于刻度线,继续加水至液面与刻度线相切
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

下列说法正确的是
A.打浆步骤,将电石渣配制成溶液
B.氯化步骤,发生的主要反应2Ca(OH)2 + 2Cl2 = Ca(ClO)2 + CaCl2 +2H2O
C.氯化过程加快氯气的通入速率,有利于提高KClO3的产率
D.KClO3晶体中可能混有 KCl、KClO等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前海水提溴的最主要方法之一是空气吹出法,其部分流程图如下:
![]()
以下推断不合理的是( )
A. 热空气能吹出溴是利用溴易挥发的性质
B. SO2吸收溴的反应方程式:SO2+2H2O+Br2=H2SO4+2HBr
C. 流程中循环利用的物质有SO2、Br2、Cl2等
D. 没有采用直接蒸馏含Br2的海水得到单质溴主要是为了节能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:![]() (正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间t变化的关系如图所示。下列叙述中正确的是
(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间t变化的关系如图所示。下列叙述中正确的是
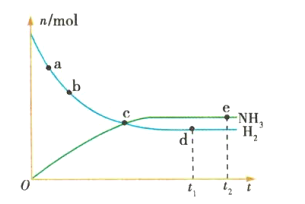
A.c点处正反应速率和逆反应速率相等
B.a点的正反应速率比b点的大
C.d点(t1时刻)和e点(t2时刻)处n(N2)不同
D.在t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的个数有( )
①氧原子的电子排布图:![]() 最外层违背了泡利原理
最外层违背了泡利原理
②处于最低能量状态原子叫基态原子,1s22s22px1→1s22s22py1过程中形成的是发射光谱
③所有元素中,氟的第一电离能最大
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中N-Cl键的键长比CCl4中C-Cl键的键长短
⑥金属元素的电负性均小于1.8
⑦主族元素的电负性越大,其元素原子的第一电离能一定越大
⑧在任何情况下,都是σ键比π键强度大
A.0个B.1个C.2个D.3个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有关图象,说法正确的是( )
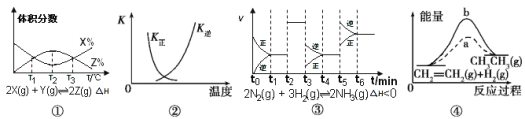
A.由图①知,反应在T1、T3处达到平衡,且该反应的△H<0
B.图②中曲线表示反应2SO2(g)+O2(g) ![]() 2SO3(g),ΔH<0正、逆反应的平衡常数K随温度的变化
2SO3(g),ΔH<0正、逆反应的平衡常数K随温度的变化
C.由图③知,反应在t6时,NH3体积分数最大,t3时采取降低反应温度的措施
D.图④中a、b曲线分别表示反应CH2= CH2(g)+H2(g) ![]() CH3CH3(g) ΔH<0使用和未使用催化剂时, 反应过程中的能量变化
CH3CH3(g) ΔH<0使用和未使用催化剂时, 反应过程中的能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com