
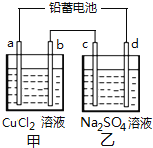
【题目】用铅蓄电池电解甲、乙电解池中的溶液.已知铅蓄电池的总反应为:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l),电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是( )
A.d极为阴极
B.放电时铅蓄电池负极的电极反应式为:PbO2(s)+4H+(aq)+SO42-(aq)+4e-=PbSO4(s)+2H2O(l)
C.若利用甲池精炼铜,b极应为粗铜
D.若四个电极材料均为石墨,当析出6.4gCu时,两池中共产生气体3.36L标准状况下
【答案】C
【解析】
A.电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,说明c电极c(OH-)增大,溶液中H+放电,则c电极是阴极、d电极是阳极,A错误;
B.原电池放电时,正极反应式为PbO2(s)+4H+(aq)+SO42-(aq)+4e-=PbSO4(s)+2H2O(l),负极为Pb+SO42--2e-=PbSO4,B错误;
C.根据选项A分析可知c电极是阴极、d电极是阳极,则b是阳极,a是阴极。电解精炼粗铜时,粗铜作阳极,所以b电极为粗铜,C正确;
D.电解析出6.4gCu,其物质的量n(Cu)=6.4g÷64g/mol=0.1mol,转移电子的物质的量是0.2mol电子,则在乙池中,阴极c电极上发生反应2H++2e-=H2↑,反应生成0.1mol氢气、d电极上发生反应:4OH--4e-=2H2O+O2↑,生成0.05molO2,在甲池的b电极上析出0.1molCl2,所以两个电池中反应产生的气体的总物质的量是0.1mol+(0.1mol+0.05mol)=0.25mol,故生成气体体积=0.25mol×22.4L/mol=5.6L,D错误;
故合理选项是C。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】我国自主研发的对二甲苯绿色合成项目取得新进展,其合成过程如图所示。

下列说法不正确的是
A. 异戊二烯所有碳原子可能共平面
B. 可用溴水鉴别M和对二甲苯
C. 对二甲苯的一氯代物有2种
D. M的某种同分异构体含有苯环且能与钠反应放出氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。若将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是( )
A. 反应后的固体混合物中还含有碳
B. 反应后的固体混合物中Cu的质量为12.8 g
C. 反应后的固体混合物总质量为14.4 g
D. 反应后的固体混合物中氧化物的物质的量为0.05mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:锂硫电池的总反应为2Li+xS===Li2Sx。以锂硫电池为电源,通过电解含(NH4)2SO4 的废水制备硫酸和化肥的示意图如图 (不考虑其他杂质离子的反应)。下列说法正确的是

A. b为电源的正极
B. 每消耗32 g硫,理论上导线中一定通过2 mol e-
C. SO42-通过阴膜由原料室移向M室
D. N室的电极反应式为2H2O-4e-===O2↑+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g),经6min后测得D的浓度为0.75mol/L,c(A):c(B)=3:5,以C表示的平均反应速率v(C)=0.125mol/(L·min),下列说法正确的是
A.以B表示的平均反应速率为v(B)=0.03125mol/(L·min)
B.6min时,转化了的A占起始A的50%
C.该反应方程式中,x=3
D.6min时,A的物质的量为0.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和稀醋酸,各加入生铁块,放置一段时间。下列有关描述错误的是

A. 生铁块中的碳是原电池的正极
B. 两试管中相同的电极反应式是:Fe-2e- = Fe2+
C. a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
D. 红墨水柱两边的液面变为左低右高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)D在元素周期表中的位置______。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键类型为______;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程______。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为______。
(4)A、B、D、E的离子半径由大到小的顺序为:______;(请用化学用语填写,下同),C、D、E的气态氢化物的稳定性顺序为:______。
(5)工业上将干燥的E单质通人D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应H2 + Cl2 ![]() 2HCl下列说法中正确的是
2HCl下列说法中正确的是
A. 该反应中,化学能只转变为热能
B. 反应物所具有的总能量高于产物所具有的总能量
C. 产物所具有的总能量高于反应物所具有的总能量
D. 断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将SO2通入BaCl2溶液至饱和的过程中,始终未观察到溶液中出现浑浊,若再通入另一种气体A,则产生白色沉淀。制备气体A的试剂不能是

A. 大理石和稀盐酸
B. NaOH和NH4Cl
C. Cu和浓硝酸
D. MnO2和浓盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com