
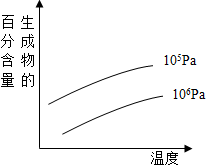
 由可逆反应测绘出的图象如图所示,纵坐标为生成物在平衡体系中的百分含量,下列对该反应判断正确的是( )
由可逆反应测绘出的图象如图所示,纵坐标为生成物在平衡体系中的百分含量,下列对该反应判断正确的是( )| A、反应物中一定有气体 |
| B、生成物中一定无气体 |
| C、正反应一定是放热反应 |
| D、正反应一定是吸热反应 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验Cl-离子的试剂是硝酸银溶液和稀硝酸 |
| B、检验SO42-离子的试剂一般用氯化钡溶液和稀盐酸 |
| C、检验CO32-离子的试剂用盐酸和澄清石灰水 |
| D、在某溶液中加入BaCl2溶液产生白色沉淀,证明溶液中有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | I2(H2O) | CCl4 | 萃取、分液 |
| B | CO2(CO) | O2 | 点燃 |
| C | Zn (Cu) | 稀硫酸 | 过滤 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当周围有人感染埃博拉病毒(EBOV)时,可以吃些抗生素以防被传染 |
| B、上呼吸道感染、咽痛等病毒疾病应该使用抗生素治疗 |
| C、抗生素在治病的同时也有副作用,没有一种抗生素是绝对安全而无副作用的 |
| D、使用某抗生素一两天后病情没有明显好转,应尽快换用其他抗生素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com