
(12分)1,2 -二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2 -二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。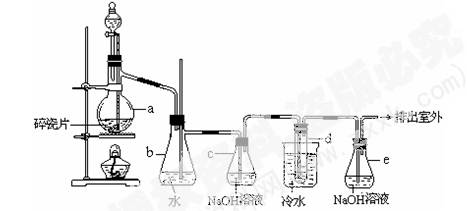
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式。_ ;_____________________。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:____________________________________________。
(3)容器c中NaOH溶液的作用是:________________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因: ______________, _____________________。
(1)C2H5OH 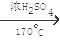 CH2=CH2↑+H2O ,CH2=CH2+Br2
CH2=CH2↑+H2O ,CH2=CH2+Br2 CH2BrCH2Br;(2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出。(3)除去乙烯中带出的酸性气体(或除去CO2、SO2);(4)原因:①乙烯发生速度过快,②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当”亦可)。
CH2BrCH2Br;(2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出。(3)除去乙烯中带出的酸性气体(或除去CO2、SO2);(4)原因:①乙烯发生速度过快,②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答“控温不当”亦可)。
解析试题分析:(1)题中制备1,2-二溴乙烷的两个化学反应方程式是C2H5OH 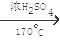 CH2=CH2↑+H2O ,CH2=CH2+Br2
CH2=CH2↑+H2O ,CH2=CH2+Br2 CH2BrCH2Br;(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:b中水面会下降,玻璃管中的水柱会上升,甚至溢出。(3)容器c中NaOH溶液的作用是:除去在制取乙烯的气体中产生的带出的酸性气体(或除去CO2、SO2);(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因有:①乙烯发生速度过快,②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃,发生了副反应而消耗乙醇,使其量增大。
CH2BrCH2Br;(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象:b中水面会下降,玻璃管中的水柱会上升,甚至溢出。(3)容器c中NaOH溶液的作用是:除去在制取乙烯的气体中产生的带出的酸性气体(或除去CO2、SO2);(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因有:①乙烯发生速度过快,②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃,发生了副反应而消耗乙醇,使其量增大。
考点:考查乙烯的实验室制取原理、操作、现象、性质及误差分析的知识。


科目:高中化学 来源: 题型:填空题
NiSO4·6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等杂质)为原料获得。操作步骤如下: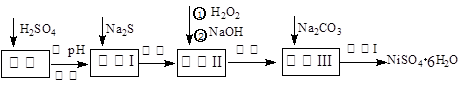
(1)加Na2S的目的是除去铜、锌等杂质,请写出除去Cu2+的离子方程式__________ __________
(2) 加6%的H2O2时,温度不能过高,是因为: _____ ________ 。
(3) 除铁方法:用H2O2充分氧化后,再用NaOH控制pH值3~4范围内生成氢氧化铁沉淀。在上述方法中,氧化剂可用NaClO3代替,请写出用氯酸钠氧化Fe2+的离子方程式为:___________________________________________________________________________
(4)上述流程中滤液Ⅲ的主要成分是: 。(填化学式)
(5)操作Ⅰ包括以下过程:过滤,用 (填试剂化学式)溶解, ,洗涤获得产品。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下: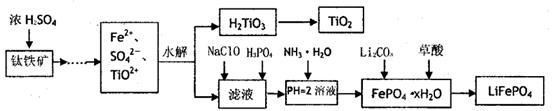
已知:H2LiO3是种难溶于水的物质。
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的
(2)TiO2+水解生成H2TiO3的离子方程式
(3)加入NaClO发生反应的离子方程式
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作 。
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁己全部转化为二价铁离子),采取KMnO4标准液漓定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果 。 (填“偏高、偏低、无影响”),滴定终点的现象 。滴定分析时,称取a g钛铁矿,处理后,用cmol/LKMnO4标准液滴定,消耗VmL,则铁元素的质量分数的表达式为
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
工业上常利用低品位软锰矿浆(主要成分是MnO2)来吸收含SO2的废气,最终制得硫酸锰晶体(MnSO4·H2O),其主要流程如下: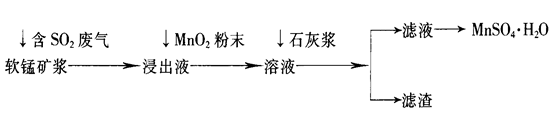
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(12 分)硫酸钠-过氧化氢加合物(xNa2SO4 ·yH2O2 ·zH2O)的组成可通过下列实验测定:①准确称取1. 7700 g 样品,配制成100. 00 mL 溶液A。②准确量取25. 00 mL 溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0. 5825 g。③准确量取25. 00 mL 溶液A,加适量稀硫酸酸化后,用0. 02000 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液25. 00 mL。H2O2与KMnO4反应的离子方程式如下:2MnO4- +5H2O2+6H+=2Mn2++8H2O+5O2↑
(1)已知室温下BaSO4的Ksp ="1." 1伊10-10,欲使溶液中c(SO42- )≤1. 0×10-6 mol·L-1,应保持溶液中c(Ba2+)≥ mol·L-1。
(2)上述滴定若不加稀硫酸酸化,MnO4- 被还原为MnO2,其离子方程式为 。
(3)通过计算确定样品的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(6分)A、B、C、D四种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+和阴离子OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。通过实验,得出如下结论:
①A和D的溶液显碱性,0.1mol·L-1A溶液的pH小于13;
②铜粉能溶解在B的溶液中;
③往C的溶液中加入过量的D溶液,最终没有沉淀。
根据以上实验事实,回答下列问题:
(1) 试写出A和B的化学式:A ,B___________。
(2) 试写出实验③中反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
甲苯氧化法制备苯甲酸的反应原理如下: + 2KMnO4
+ 2KMnO4
 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O + HCl
+ HCl
 +KCl
+KCl
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100 ℃时, 反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯。


图1回流搅拌装置 图2抽滤装置
⑴实验室中实现操作Ⅰ所需的玻璃仪器有 、烧杯;操作Ⅱ的名称为 。
⑵如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是 。
⑶在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是 ;如图2所示抽滤完毕,应先断开 之间的橡皮管。
⑷纯度测定:称取1.220 g产品,配成100 mL溶液,取其中25.00 mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3 mol。产品中苯甲酸质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氮化铝(AlN)是一种新型无机材料。某氮化铝(AlN)仅含有Al2O3杂质,某学习小组为测定该氮化铝样品中AlN的纯度,查阅资料得知:AlN + NaOH + 3H2O = Na[Al(OH)4] + NH3↑。设计如下2种方案。
方案一:量气法——如图所示。
(1)按图连接好装置,检查装置气密性的方法是 。
(2) 导管a的主要作用是 。
(3)为测定生成气体的体积,量气装置中的X液体可以是: 。(填标号)
| A.CCl4 | B.H2O | C.NH4Cl溶液 | D.植物油 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某兴趣小组同学在实验室用加热1-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如图所示装置,其中夹持仪器、加热仪器及冷却水管没有画出。
请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷。
竖直冷凝管接通冷凝水,进水口是_____(填“I”或“Ⅱ”);竖直冷凝管的主要作用是________。
(2)理论上,上述反应的副产物可能有:丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等。熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物,已知B、C装置中为常见物质的水溶液。
B装置检验的物质是_________,写出C装置中主要的化学方程式:_______________。
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
| 物质 | 熔点/℃ | 沸点/℃ |
| 1-丁醇 | -89.5 | 117.3 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com