
【题目】化学反应都有能量变化,吸热或放热是化学反应中能量变化的主要形式之一。
(1)反应A(g)+B(g)=C(g)+D(g),反应过程中能量变化如下图所示,回答下列问题:

①化学反应中产生能量变化的本质原因是______________;
②该反应是_____反应(填“吸热或放热”)、ΔH=__________ (用E1、E2表示);
③加入催化剂对该反应的ΔH是否有影响?___________。
(2)已知:一定条件下,拆开1molH-H键、1molCl-Cl键、1molH-Cl键需要的能量分别是436kJ、243kJ、432kJ,则反应H2(g)+Cl2(g)=2HCl(g) 的ΔH=_____。
(3)已知:2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g) ΔH1=-a kJmol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=-b kJmol﹣1
H2O(g)=H2O(l) ΔH3=-c kJmol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为_________________________________。
【答案】 破坏反应物中化学键吸收的能量与形成生成物中化学键放出的能量存在差异 放热 E1-E2或-(E2-E1) 无影响 -185 kJmol﹣1 CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(1分) ΔH1=-(
O2(g)=CO2(g)+2H2O(1分) ΔH1=-(![]() 2c) kJmol﹣1
2c) kJmol﹣1
【解析】本题主要考查反应热的计算。
(1)①化学反应中产生能量变化的本质原因是破坏反应物中化学键吸收的能量与形成生成物中化学键放出的能量存在差异;
②该反应是放热反应、ΔH=E1-E2;
③加入催化剂对该反应的ΔH是否有影响?无影响。
(2)ΔH=(436+243-2×432) kJmol﹣1= -185 kJmol﹣1。
(3)将已知热化学方程式依次表示为A、B、C,2C-A/2-B/2得表示CH3OH(l)燃烧热的热化学方程式为CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(1分) ΔH1=-(
O2(g)=CO2(g)+2H2O(1分) ΔH1=-(![]() 2c) kJmol﹣1。
2c) kJmol﹣1。


科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.甲烷燃烧生成二氧化碳和水
B.乙醇与氧气反应生成乙醛和水
C.乙烯与溴反应生成1,2—二溴乙烷
D.甲烷与氯气反应生成一氯甲烷和氯化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是
(已知:氧化性Fe2+<Ni2+<Cu2+)
A. 阳极发生还原反应,其电极反应式:Ni2++2e-===Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )

A. 6:1 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
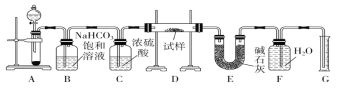
回答下列问题:
(1)实验前必须检查装置的气密性。仪器连接好后,在________中加适量的水,关闭A中分液漏斗阀门后微热试管,若看到________,说明装置气密性好。
(2)装置A中液体试剂选用盐酸而不是硫酸,理由是__________________________________________。
(3)装置B的作用是___________;装置C的作用是______________;装置E中碱石灰的作用是__________________。
(4)装置D中发生反应生成气体的化学方程式是_____________________________________________。
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,C1-的物质的量浓度最大的是
A.300 mL0.1 mol/L NaCl溶液
B.100 mL0.1 mol/LFeCl3溶液
C.标准状况下,4.48LHC1气体溶于水配成的1 L溶液
D.向1 L0.2 mol/L BaCl2溶液中加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液(忽略溶液混合时的体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶炼金属铝的废弃物铝灰为原料制取超细![]() -氧化铝,既能降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备流程如下:
-氧化铝,既能降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备流程如下:
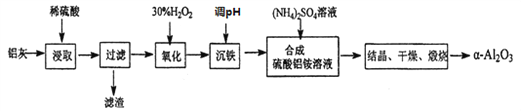
(1)用上图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为____(填选项编号)。

(2)流程中加入H2O2 有气体产生,原因是_______________________________。
(3)通过调节溶液的pH来“沉铁”,得到Fe(OH)3。己知:
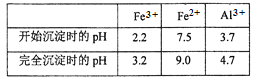
为保证产品的纯度,可以选用下列物质中的_______调节溶液pH(填字母),调节pH的范围为___________________________。
a.A12O3 b.NaOH c.Al(OH) 3 d.Na2CO3
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4 Al(SO4)2·12H2O] ![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
将产生的气体通过下图所示的装置:
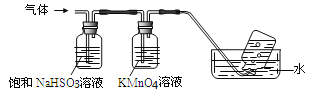
①集气瓶中收集到的气体是_____________________(填化学式);
②装有KMnO4溶液洗气瓶的作用是__________________________________;
③选用一种常用化学试剂和稀硝酸检验硫酸铝铵,该试剂是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学方法区别NaCl、MgCl2、AlCl3、CuCl2、FeCl3和NH4Cl六种溶液(必要时可加热),下列试剂中可选用的是( )
A.KSCN溶液B.AgNO3溶液C.BaCl2溶液D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.乙烷和乙烯可用溴水加以区别
B.乙烯与氢气在催化剂作用下生成乙烷的反应属于取代反应
C.可以用分液的方法分离乙醇和水
D.有机化合物都能燃烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com