
【题目】NA代表阿伏加德罗常数,在含4克NaOH溶质的溶液中通入一定量的CO2,将溶液蒸干并灼烧,最后得到的固体是
A.0.1NA的NaHCO3
B.0.05NA Na2CO3
C.0.05NA~0.1NA Na2CO3和NaHCO3混合物
D.0.1NA的NaHCO3和NaOH混合物
【答案】B
【解析】
n(NaOH)=![]() =0.1 mol,一定量CO2通入NaOH溶液中,可能发生:①CO2+2NaOH=Na2CO3+H2O,②CO2+NaOH=NaHCO3,得到的溶液蒸干并灼烧碳酸氢钠分解生成碳酸钠,其反应为:2NaHCO3
=0.1 mol,一定量CO2通入NaOH溶液中,可能发生:①CO2+2NaOH=Na2CO3+H2O,②CO2+NaOH=NaHCO3,得到的溶液蒸干并灼烧碳酸氢钠分解生成碳酸钠,其反应为:2NaHCO3![]() Na2CO3+H2O+CO2↑,如果氢氧化钠完全反应,则最终得到的固体是碳酸钠。
Na2CO3+H2O+CO2↑,如果氢氧化钠完全反应,则最终得到的固体是碳酸钠。
A.NaHCO3不稳定,加热条件下分解生成碳酸钠,所以最终得到的固体不能是NaHCO3而是Na2CO3,A错误;
B.如果最终得到的是碳酸钠,根据钠原子守恒得0.05NA Na2CO3,B正确;
C.NaHCO3不稳定,加热条件下分解生成碳酸钠,所以最终得到的固体不能含有NaHCO3,C错误;
D.如果NaOH有剩余,则溶液中不能存在NaHCO3,且NaHCO3不稳定,加热条件下分解生成碳酸钠,所以最终得到的固体不能含有NaHCO3,D错误;
故合理选项是B。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】聚酯纤维(涤纶)是重要的衣服面料,以下是一种合成路线(部分反应条件略去)。
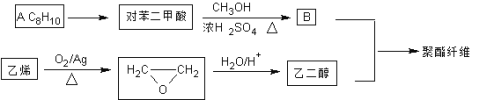
已知:酯与醇(或酚)可发生如下酯交换反应:![]()
(1)C8H10的系统命名为______________;它的同系物分子通式为________________。
(2)在其它催化剂作用下,乙烯与氧气反应的产物是____________(写结构简式)。
(3)若B过量,生成的聚酯纤维可表示为:![]() ,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
,若乙二醇过量,则生成的聚酯纤维可表示为_______________________________。
(4)将废涤纶和甲醇在一定条件下反应,对聚合物进行降解,生成物是______________(填名称)。
(5)对苯二甲酸有多种芳香族同分异构体,写出一种满足以下条件的有机物的结构简式________。
①遇氯化铁溶液显紫色;②能发生银镜反应;③有三种不同化学环境的H原子。
(6)聚合物PC也由酯交换反应合成,其结构可表示为:![]() ,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
,合成PC的2种单体中:醇(或酚)的结构简式为______________________,酯的名称为
_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如右图所示。下列说法正确的是
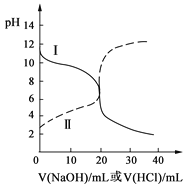
A.曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用有机物甲可制备环己二烯(![]() ),其反应路线如图所示:
),其反应路线如图所示:
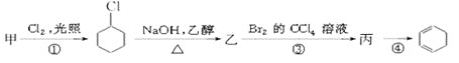
已知:RCH2CH2Br![]() RCH=CH2
RCH=CH2
下列有关判断正确的是( )
A.甲的化学名称是苯B.乙的结构简式为![]()
C.反应①为加成反应D.有机物丙既能发生加成反应,又能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近科学家获得了一种稳定性好、抗氧化能力强的活性化合物A;其结构如下:

为了研究X的结构,将化合物A在一定条件下水解只得到 和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
和C。经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生。
请回答下列问题:
(1)化合物B能发生下列哪些类型的反应________。
A.取代反应 B.加成反应
C.缩聚反应 D.氧化反应
(2)写出化合物C所有可能的结构简式______________________________。
(3)C可通过下图所示途径合成,并制取冬青油和阿司匹林。

(ⅰ)写出有机物的结构简式:D:______________,C:________________,E:______________。
(ⅱ)写出变化过程中①、⑥的化学方程式(注明反应条件)
反应①__________________________________;反应⑥_____________________________。
(ⅲ)变化过程中的②属于____________反应,⑦属于________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向一定体积0.1 mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的变化关系如图所示,则正确的是

A.M点所示溶液导电能力强于Q点
B.N点所示溶液中c(Na+)>c(CH3COO-)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备

①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 已知,CO 的毒性表现在 CO 与血红蛋白(Hb)结合成Hb·CO,使血红蛋白失去输送 O2功能。CO进入血液后有如下平衡:CO+Hb·O2![]() O2+Hb·CO,已知在人体体温 37℃下,该平衡常数为 220。试回答:
O2+Hb·CO,已知在人体体温 37℃下,该平衡常数为 220。试回答:
(1)煤气中毒病人,可以通过进入高压氧舱的方法来救治,请用化学平衡的原理加以说明:______。
(2)抽烟时,进入肺部的空气中c(CO)=10-6mol·L-1,c(O2)=10-2mol·L-1,则c(Hb·CO)为c(Hb·O2)的___________倍。
(3)已知当血液中c(Hb·CO)/c(Hb·O2)的比值大于 0.02时,人的智力会很快受到损伤,为避免人的智力受到损伤,c(O2)与c(CO)的比值应大于_____。
Ⅱ.在某一温度条件下, Bodensteins 研究了反应:2HI(g)![]() H2(g) +I2(g),气体混合物中 HI 的物质的量浓度x(HI)(mol·L-1)与反应时间t的关系如下表:
H2(g) +I2(g),气体混合物中 HI 的物质的量浓度x(HI)(mol·L-1)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 | |
第一次试验 | x(HI) | 1 | 0.90 | 0.85 | 0.815 | 0.795 | 0.784 |
第二次试验 | x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
(4)根据上述实验结果,该反应的平衡常数K的计算式为_________。
(5)上述反应,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)×x(I2),其中k正、k逆为速率常数,则k逆为_________(以K和k正表示)。若k正=0.002·min-1,第一次实验时,当t=20 min,v正=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色液体,易溶于水。为研究A 的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
①称取9.0gA,升温使其气化,测其密度是相同条件下H2的45 倍 | 试通过计算填空:(1)A的相对分子质量为________ |
②将此9.0gA在足量纯O2中充分 燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g | (2)A的分子式为________ |
③又知A含有官能团—COOH、—OH,且A的核磁共振氢谱如图: |
|
(3)综上所述,A的结构简式为________ | |
II. 工业上常以A物质为原料合成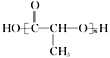 ,该反应类型属于______(填字母代号,下同)反应。
,该反应类型属于______(填字母代号,下同)反应。
A 加聚 B 缩聚
III. 下列关于物质的分离、提纯实验中的一些操作或做法,正确的是_______。
A 在组装蒸骝装置时,温度计的水银球应伸入液面下
B 用96%的工业酒精制取无水乙醇时,先加入无水CuSO4,再过滤
C 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加入少量蒸馏水
D 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com