
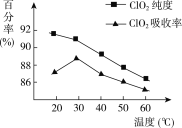
【题目】以黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备二氧化氯气体,再用水吸收获得二氧化氯溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2气体的吸收率。具体情况如下图所示。
请回答下列问题:
(1)据图可知,反应时需要控制的适宜温度是________ ℃,达到此要求采取的适宜措施是________。
(2)已知:黄铁矿中的硫元素在酸性条件下被ClO3-氧化成SO42-,写出制备二氧化氯的离子方程式:____________________________________。
(3)某校化学学习小组拟以“m(ClO2)/m(NaClO3)”作为衡量ClO2产率的指标。若取NaClO3样品质量6.0 g,通过反应和吸收可得400 mL ClO2溶液,取出20 mL,加入37.00 mL 0.500 mol·L-1(NH4)2Fe(SO4)2溶液充分反应,过量Fe2+再用0.0500 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗20.00 mL。反应原理如下:
4H++ClO2+5Fe2+===Cl-+5Fe3++2H2O
14H++6Fe2++Cr2O72-===2Cr3++6Fe3++7H2O
试计算ClO2的“产率”为_________________________。
【答案】30 水浴加热(或水浴控制恒温)15ClO3-+FeS2+14H+===15ClO2↑+Fe3++7H2O+2SO42-56.25%
【解析】
(1)据图可知,在20℃反应时ClO2气体制取纯度高,但是气体的吸收率较低,在30℃无论是反应制取ClO2气体纯度高还是气体的吸收率都较高。若温度再升高,制取ClO2气体纯度高还是气体的吸收率都降低。所以需要控制的适宜温度是30℃;达到此要求采取的适宜措施是水浴加热(或水浴控制恒温);(2)黄铁矿中的硫元素在酸性条件下被ClO3-氧化成SO42-,制备二氧化氯的离子方程式为15ClO3-+FeS2+14H+=15ClO2↑+Fe3++7H2O+2SO42-;(3)由方程式4H++ClO2+5Fe2+=Cl-+5Fe3+ +2H2O、14H+ + Cr2O72-+6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O可结合电子得失守恒可得1×n(Fe2+)=5×n(ClO2)+2×3×n(Cr2O72-).与K2Cr2O7反应的n(Fe2+)=6n(Cr2O72-)=6×20×10-3L×0.0500mol/L=6×10-3mol;与ClO2反应的n(Fe2+)=37×10-3L× 0.0500mol/L -6×10-3mol=1.25×10-2mol。所以n(ClO2)=![]() ×1.25×10-2mol=2.5×10-3mol。ClO2的“产率”=
×1.25×10-2mol=2.5×10-3mol。ClO2的“产率”=![]() 。
。


科目:高中化学 来源: 题型:
【题目】常温下有浓度均为0.5 mol/L的四种溶液:
①Na2CO3、②NaHCO3、③HCl、④NH3·H2O
(1)上述溶液中,可发生水解的是______(填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为:____________________________________。
(3)向④中加入少量氯化铵固体,此时c(NH![]() )/c(OH-)的值________(填“增大”、“减小”、或“不变”)。
)/c(OH-)的值________(填“增大”、“减小”、或“不变”)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积________④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是____________。
(5)取10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是:

A. X可能是一种氢化物
B. 若Y为单质,Y生成Z属于化合反应
C. E可能是一种有色气体
D. F中M元素的化合价可能为+5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置。
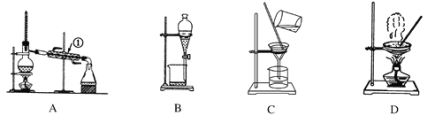
利用以上装置,可以按以下实验方案从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)

(1)装置A中仪器①的作用是________,使用装置A的操作是_____(填“a”、“b”、“c”或“d”,下同)。
(2)使用装置B的操作是______,为使其中液体顺利滴下,除打开下端活塞外,还应进行的具体操作是___________________。
(3)使用装置C的操作是_______,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________________________________________________________________________________。
(4)使用装置D的操作是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近日,中国科学院深圳先进技术研究院研发出一种高性能的钙离子电池:以溶有六氟磷酸钙Ca(PF6)2的碳酸酯类溶剂为电解液,放电时合金Ca7Sn6发生去合金化反应,阴离子(PF6)从石墨烯中脱嵌,进入电解质溶液。放电时其工作原理如下图,下列说法错误的是(已知:比能量为单位质量的电极放出电能的大小)
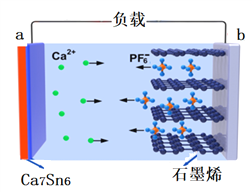
A. 电池放电时,化学能转化为电能和热能
B. 放电时,a电极的电极反应方程式为:Ca7Sn6 —14e- =7Ca2+ + 6Sn
C. 充电时,b电极接电源的正极
D. 与锂离子电池相比较钙离子电池具有材料储量丰富、比能量高的优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙炔能够导电,下列关于聚乙炔![]() 和聚合物A
和聚合物A![]() 的说法中正确的是
的说法中正确的是
A. 聚合物A和聚乙炔均能使溴水褪色
B. 两种聚合物的单体互为同系物
C. 聚合物A的相对分子质量是聚乙炔的两倍
D. 1mol 两种聚合物的单体分别与Br2发生反应,最多消耗Br2的物质的量之比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com