
【题目】室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )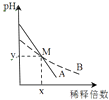
A.稀释前,c(A)>10 c(B)
B.中和等浓度等体积的盐酸时,B用的体积较多
C.M点时A和B的浓度相等
D.在M点,A,B两种碱溶液中阳离子的物质的量浓度相等
【答案】D
【解析】解:A.AB稀释相同倍数,A的pH变化大,则A的碱性强,稀释前,设c(A)=0.1mol/L,c(B)>0.01mol/L,则c(A)<10c(B),故A错误;
B.稀释前A溶液中氢氧根离子浓度大于B溶液中,即A的浓度大于B,所以中和等浓度等体积的盐酸时,A用的体积较多,故B错误;
C.M点AB溶液pH相同,A的碱性强,A的电离度大于B,所以浓度B大于A的浓度,不相等,故C错误;
D.M点AB溶液pH相同,氢氧根离子浓度相同,由电荷守恒c(A+)+c(H+)=c(OH﹣),c(B+)+c(H+)=c(OH﹣)可知c(A+)=c(B+),所以M点A、B两种碱溶液中阳离子的物质的量浓度相等,故D正确;
故选D.
【考点精析】本题主要考查了弱电解质在水溶液中的电离平衡的相关知识点,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能正确解答此题.


 能力评价系列答案
能力评价系列答案科目:高中化学 来源: 题型:
【题目】某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的
A.正反应活化能小于 100 kJ·mol-1B.逆反应活化能一定小于 100 kJ·mol-1
C.正反应活化能不小于 100 kJ·mol-1D.正反应活化能比逆反应活化能大 100 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属性质的叙述中正确的是
A.钠与氧气反应时,产物是由O2的用量决定的
B.铝箔在空气中受热可以熔化且会发生剧烈燃烧
C.金属与非金属发生反应时,被氧化的一定是金属
D.铁丝不论在空气中还是在纯氧中都不会燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子反应可用H++OH-= H2O表示的是( )
A. 氢氧化钡和硫酸B. 氢氧化铁和盐酸C. 硝酸和氢氧化铜D. 硫酸氢钠和氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2﹣CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( ) 
A.阳极产生的气体为氟气
B.阳极区放出的气体只是纯氧气
C.TiO2在阴极表面放电
D.制备金属钛前后,CaO的总量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)11H、21H、31H互为________O2、O3互为_________
(2)在下列固体中: a.CaCl2 b.KOHc.Hed.H2SO4e.NH4Clf.金刚石
①其中不含化学键的物质是________
②既含有离子键又含有共价键的物质是____________(填序号)
(3)下图是几种常见的电池装置。请回答:

①电池Ⅰ中负极反应式是_____,溶液中H+向_____(填“负”或“正”)极移动,若1mol电子流过导线,则产生氢气的物质的量是______mol。
②电池Ⅱ属于________电池(填“一次”或“二次”).
③电池Ⅲ是氢氧燃料电池,写出负极的电极反应式是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某溶液中加入BaCl2溶液,再加入稀硝酸,产生的白色沉淀不消失,下列叙述正确的是( )
A.溶液中一定含有SO42﹣
B.溶液中一定含有Ag+
C.溶液中一定含有SO32﹣
D.溶液中可能含有SO42﹣、SO32﹣、Ag+中的某一种、两种或三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及有机化合物的分离提纯的说法正确的是( )
A.除去乙烷中混有的乙烯,可将混合气体通过酸性高锰酸钾溶液
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.除去溴苯中混有的Br2 , 可用NaOH溶液洗涤分液
D.乙酸乙酯中的少量乙酸和乙醇可用氢氧化钠溶液除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯的氧化物是氯与氧的二元化合物的总称,也称为氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有关数据见下表:
化学式 | Cl2O | ClO2 | Cl2O7 |
相对分子质量 | 87 | 67.5 | 183 |
沸点/℃ | 2 | 9.7 | 81 |
完成下列填空:
(1)Cl2O是酸的酸酐,Cl2O电子式为 .
(2)下列能判断Cl和O两种元素非金属性强弱的是(选填编号).
a.氧化氯的分子式 b.与金属反应得电子的数目
c.气态氢化物的稳定性 d.最高价氧化物对应水化物的酸性
(3)根据分子间作用力对沸点影响的变化规律:组成和结构相似的分子,其沸点随着相对分子质量的增大而升高,但上表中相对分子质量是Cl2O7>Cl2O>ClO2 , 其沸点的变化不是Cl2O7>Cl2O>ClO2的原因是
(4)ClO2和碱溶液反应生成亚氯酸盐(阴离子是ClO2﹣)和氯酸盐,其离子方程式是 , 氧化产物 . (填离子符号)
(5)一定条件下,在水溶液中1mol Cl﹣、ClO ![]() (x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示).
(x=1,2,3,4)的能量(kJ)相对大小如图所示.D是(填离子符号).B→A+C的热化学方程式为(用离子符号表示). 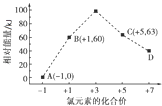
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com