
【题目】Ⅰ.用![]() 表示原子:
表示原子:
(1)中性原子的中子数:N=______。
(2)阴离子的中子数:AXn-共有x个电子,则N=______。
(3)中性分子中子数:12C16O2分子中,N=______。
(4)A2-原子核内有x个中子,其质量数为m,则n g A2-所含电子的物质的量为____ mol。
Ⅱ.有①![]() 、
、![]() 、
、![]() ②H2、D2、T2 ③石墨、金刚石 ④
②H2、D2、T2 ③石墨、金刚石 ④![]() 、
、![]() 、
、![]() 四组微粒或物质,回答下列问题:
四组微粒或物质,回答下列问题:
(1)互为同位素的是________(填编号,下同)。
(2)互为同素异形体的是________。
(3)有①和④的微粒可组成______种相对分子质量不同的三原子化合物.
【答案】 A-Z A-x+n 22 (m-x+2)n/m ①④ ③ 7
【解析】(1)根据在原子中:质量数=质子数+中子数,所以中子数=质量数-质子数,因此,本题正确答案是:![]() 。
。
(2)根据在阴离子中:核电荷数=质子数=核外电子数-所带电荷数,即核电荷数=质子数![]() ,又根据质量数=质子数+中子数,即中子数=质量数-质子数
,又根据质量数=质子数+中子数,即中子数=质量数-质子数![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]() ;
;
(3)根据![]() 中核电荷数=质子数=核外电子数=6,再根据
中核电荷数=质子数=核外电子数=6,再根据![]() 中核电荷数=质子数=核外电子数=8,所以
中核电荷数=质子数=核外电子数=8,所以![]() 分子中,电子数为
分子中,电子数为![]() ,因此,本题正确答案是:22;
,因此,本题正确答案是:22;
(4)元素A的质量数为m,![]() 离子的原子核内有x个中子,则A的质子数为
离子的原子核内有x个中子,则A的质子数为![]() ,所以
,所以![]() 中核外电子数为
中核外电子数为![]() ,
,![]() ,
,
则n克![]() 离子中包含电子个数是
离子中包含电子个数是![]() ;
;
因此,本题正确答案是:![]() 。
。
Ⅱ同位素指质子数相同,中子数不同的同一类元素的不同原子,所以①④,互为同素异形体的是指同一元素形成的不同单质,所以③;水分子是由1个氧原子和2个氢原子构成,从氢的三种同位素中选两个氢原子,两个氢原子可以相同也可不同,所以有6种选法;氧原子有3种选法,所以3×6=18,期中相对分子质量不同的三原子化合物由7种;故答案为:①④;③;7。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列物质有如下转化关系(有的生成物未列出),其中:D为碱,G为酸,金属甲在G 的浓溶液中会钝化;F的溶液中只含一种溶质.
A、B、C、D,E均由Q,R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素.则:
(1)X在周期表中的位置是 , R、X、T的原子半径从小到大的顺序为(用元素符号表示);
(2)A和G等物质的量反应产物的水溶液显性,其原因用离子方程式表示为;
(3)A和X2反应的化学方程式为;
(4)pH均为12的D溶液和F溶液中,水电离出的c(OH﹣)之比为;
(5)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和CO反应转化为两种空气的成分,当反应转移1 mol电子时,生成的气体在标准状况下的总体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一结晶水合物x6H2O,可发生如下的转化(部分反应物生成物已略).其中B、D、F均为无色气体,G为难于水的红褐色固体,在A溶液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀.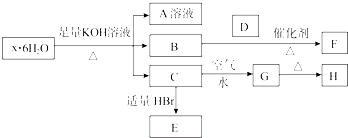
(1)该结晶水合物的化学式为 .
(2)把C溶于过量的稀H2SO4 , 再加KMnO4溶液,所涉及的离子方程式: .
(3)向E溶液中通入等物质的量的Cl2 , 写出反应的离子方程式: .
(4)C→G的现象为 , 该反应的化学方程式为 .
(5)向一定量的Cu与H的混合物中加入300 mL 1 mol/L HCl溶液,恰好使混合物完全溶解,向所得溶液中加入KSCN溶液后无红色出现.若用过量的CO在高温下还原相同质量的此混合物,固体的质量减小g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体.再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀.根据题意推断气体x的成分可能是( )
A.0.3mol NO2 和0.3mol NO
B.0.2mol NO2和0.1mol N2O4
C.0.1mol NO,0.2mol NO2和0.05mol N2O4
D.0.6mol NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出).其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体.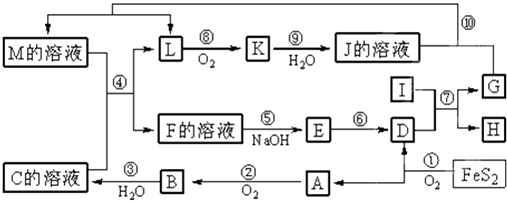
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第周期族.
(2)在反应⑦中氧化剂与还原剂的物质的量之比为 .
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是 . (填写序号)
(4)反应④的离子方程式是: .
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式中,正确的是( )
A. Al2(SO4)3=2A13++3SO42- B. Ba(OH)2=Ba2++(OH-)2
C. Na2SO4=2Na++S04-2 D. Ca(N03)2=Ca2++2(N03) 2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率﹣v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.![]() (NH3)=0.01 mol/(L?s)
(NH3)=0.01 mol/(L?s)
B.![]() (O2)=0.00l0 mol/(L?s)
(O2)=0.00l0 mol/(L?s)
C.![]() (NO)=0.00l0 mol/(L?s)
(NO)=0.00l0 mol/(L?s)
D.![]() (H2O)=0.045 mol/(L?s)
(H2O)=0.045 mol/(L?s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示式错误的是( )
A.Na+的轨道表示式: ![]()
B.Na+的结构示意图: ![]()
C.Na的电子排布式:1s22s22p63s1
D.Na的简化电子排布式:[Ne]3s1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com