
【题目】一个真空恒容密闭容器中盛有1molPCl5,加热到200℃时发生如下反应:PCl5(气) ![]() PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系 ( )
PCl3(气)+Cl2(气),反应达到平衡时,混合气体中PCl5所占体积分数为M%. 若在同一温度和同一容器中,最初投入是2molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%.则M和N的关系 ( )
A. 大于B. 小于C. 等于D. 不能肯定
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】己知A是气态烃,完全燃烧时产生的CO2和,H2O的物质的量之比为1:1,A的相对分子量小于30。在如图所示的变化中,中间产物C跟葡萄糖一样也能银新制的Cu(OH)2发生反应产生砖红色沉淀,E有香味,F是高分子化合物(反应条件未写出)。
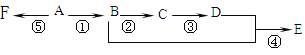
写出下列各步变化的化学方程式及反应类型。
反应①______;_______________
反应②______;________________
反应④______;___________________
反应⑤______;________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.在粗铜的精炼过程中,若电路中转移1 mol 电子,则阳极质量一定减少了32 g
B.反应8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
C.1.2g的金刚石和12g 的SiO2分别含有0.4mol的C-C键与0.4mol 的Si-O 键
D.常温下,向NH4Cl溶液中加入少量NaOH固体(溶液温度没有变化),溶液中![]() 的值增大
的值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】一定温度下,反应N2(g)+3H2(g)![]() 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A. c(N2):c(H2):c(NH3)=1:3:2
B. N2、H2和NH3的物质的量分数不再改变
C. N2与H2的物质的量之和是NH3的物质的量的2倍
D. 单位时间里每增加lmolN2,同时增加3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100.0 mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到16.84g沉淀,用过量稀硝酸处理后沉淀质量减少至6.99g,同时溶液中有气泡产生。试求:
(1)原混合液中Na2SO4的物质的量浓度为_____;
(2)产生的气体在标准状况下的体积为多少__________?(要求写出计算过程,只写结果不给分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】mA(g)+nB(g)![]() pC(g)△H<0,室温条件下,在一容积不变的密闭容器中加入一定量的A、B,B%与压强(P)的关系如图所示,则下列有关叙述正确的是( )
pC(g)△H<0,室温条件下,在一容积不变的密闭容器中加入一定量的A、B,B%与压强(P)的关系如图所示,则下列有关叙述正确的是( )
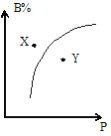
A.m+n>p
B.n>p
C.X点时混合物的正反应速率小于逆反应速率
D.X点比Y点混合物的反应速率慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于新制氯水的叙述正确的是( )
A.光照新制氯水有气泡逸出,该气体是Cl2B.新制氯水放置数天后酸性减弱
C.新制氯水中只含有Cl2和H2O两种分子D.新制氯水可使蓝色石蕊试纸先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有铜的印刷线路板浸入200 mL氯化铁浓溶液中,有19.2 g铜被腐蚀掉。取出印刷线路板,向溶液中加入16.8 g铁粉,经充分反应,溶液中还存在9.6 g不溶解的物质。(设溶液体积不变)。请回答下列问题:
(1)充分反应后,溶液中存在9.6 g不溶物的成分为____。
(2)充分反应后溶液中一定不存在的金属离子为_____。
(3)比较Fe2+、Fe3+、Cu2+的氧化性大小:______。
(4)试计算最后溶液中Fe2+的物质的量浓度____mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S与CO2在高温下发生反应:H2S(g)+CO2(g) ![]() COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,4min时反应达到平衡,平衡后水的物质的量分数为8%。下列说法中正确的是( )
COS(g) +H2O(g)。在610 K时,将0.10 mol CO2与0.40 mol H2S充入2.5 L的空钢瓶中,4min时反应达到平衡,平衡后水的物质的量分数为8%。下列说法中正确的是( )
A.速率V(H2S)=4×10-3molL-1min-1B.CO2的转化率为60%
C.平衡时H2S与CO2的物质的量之比为4:1D.当体系中压强不变时,反应达到平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com