
【题目】设NA为阿伏加德罗常数的数值。下列说法正确的是( )
A.12g金刚石和石墨的混合物中,碳原子数为NA
B.2Fe2++2H++3H2O2=2Fe3++O2↑+4H2O,则每生成1 mol O2转移电子数为2NA
C.已知H3PO2+OH(足量)= ![]() +H2O,说明1 mol H3PO2电离出H+数为NA
+H2O,说明1 mol H3PO2电离出H+数为NA
D.标准状况下,11.2 L乙烷和苯的混合物中C-H数目为 3NA
【答案】A
【解析】
A.金刚石和石墨都由C原子构成,则n(C)=![]() =1mol,即12g金刚石和石墨的混合物中,碳原子数为NA,A正确;
=1mol,即12g金刚石和石墨的混合物中,碳原子数为NA,A正确;
B.反应2Fe2++2H++3H2O2=2Fe3++O2↑+4H2O中,Fe元素化合价从+2升高到+3,升高了2×1,3H2O2中2个-1价的O化合价从-1升高到0,升高了2×1,化合价总升高2×1+2×1=4,3H2O2中4个-1价的O化合价从-1降低到-2,化合价总降低4×1=4,则2Fe2++2H++3H2O2=2Fe3++O2↑+4H2O~4e-,即每生成1 mol O2转移电子数为4NA,B错误;
C.H3PO2+OH(足量)=![]() +H2O,说明H3PO2是一元酸,如果H3PO2是强酸,1 mol H3PO2电离出H+数为NA,如果H3PO2是弱酸,1 mol H3PO2电离出H+数小于NA,C错误;
+H2O,说明H3PO2是一元酸,如果H3PO2是强酸,1 mol H3PO2电离出H+数为NA,如果H3PO2是弱酸,1 mol H3PO2电离出H+数小于NA,C错误;
D.标准状况下,苯不是气体,无法准确计算,D错误。
答案选A。


科目:高中化学 来源: 题型:
【题目】实验小组从富含 NaBr 的工业废水中提取Br2 的过程主要包括:氧化、萃取、分液、蒸馏等步骤。
已知:①蒸馏时各组分的沸点差异越大,分离效果越好;②可能用到的数据信息和装置如下:
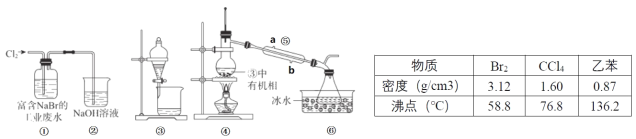
下列说法错误的是
A.②的作用是吸收多余 Cl2,防止空气污染
B.用③进行萃取时,选择乙苯比 CCl4 更合理
C.乙苯和 CCl4 萃取 Br2 时现象相同,都是分层,上层无色,下层橙色
D.仪器⑤的名称为冷凝管,其中 b 为进水口,a 为出水口
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从牛至精油中提取的三种活性成分的结构简式如下图所示,下列说法正确的是( )
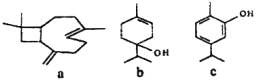
A. a、b、c均能使酸性KMnO4溶液褪色
B. a、b中均含有2个手性碳原子(手性碳原子指连有四个不同基团的碳原子)
C. b、c均能发生加成反应、还原反应、取代反应、消去反应
D. c分子中所有碳原子可以处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】学习小组探究AgNO3、Ag2O(棕黑色固体,难溶于水)对氯水漂白性的影响。
实验记录如下:
| 实验 | 方案和现象 |
ⅰ | 加入1mL蒸馏水,再滴加1滴品红溶液,品红溶液较快褪色 | |
ⅱ | 加入少量Ag2O固体,产生白色沉淀a。再加入1mL蒸馏水和 1滴品红溶液,品红溶液褪色比i快 | |
ⅲ | 加入1mL较浓AgNO3溶液,产生白色沉淀b。再滴加1滴品红溶液,品红溶液褪色比i慢 |
(1)用离子方程式表示i中品红溶液褪色的原因:______。
(2)经检验,ii中的白色沉淀a是AgCl。产生AgCl的化学方程式是_______。
(3)ⅰ是iii的对比实验,目的是排除iii中______造成的影响。
(4)研究白色沉淀b的成分。进行实验iv(按实验iii的方案再次得到白色沉淀b,过滤、洗涤,置于试管中):
实验iv:
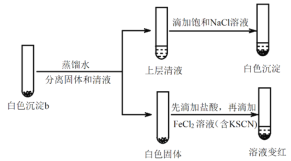
①设计对比实验证实白色沉淀b不只含有AgCl,实验方案和现象是_______。
②FeCl2溶液的作用是_______。由此判断,白色沉淀b可能含有AgClO。
(5)进一步研究白色沉淀b和实验iii品红溶液褪色慢的原因,进行实验v:
实验v:

①结合离子方程式解释加入饱和NaCl溶液的目的:_______。
②推测品红溶液褪色的速率:实验iii比实验v______(填“快”或 “慢”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原 料,可用作止痛剂、退热剂、防腐剂和染料中间体。乙酰苯胺的制备原理为:
![]() +CH3COOH
+CH3COOH![]() +H2O
+H2O

注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。

实验步骤:
步骤 1:在圆底烧瓶中加入无水苯胺 9.2 mL,冰醋酸 17.4 mL,锌粉0.1 g,安装仪器,加入沸石,调节加热温度,使分馏柱顶温度控制在105℃ 左右,反应约 60~80 min,反应生成的水及少量醋酸被蒸出。 步骤 2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛有 100 mL 冰 水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰 苯胺粗品。步骤 3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)步骤 1 中所选圆底烧瓶的最佳规格是_________(填序号)。
a.25 mL b.50 mL c.150 mL d.200 mL
(2)实验中加入少量锌粉的目的是___________________________________________________________________________。
(3)从化学平衡的角度分析,控制分馏柱上端的温度在 105℃左右的原因____________________________________________________________________________。
(4)洗涤乙酰苯胺粗品最合适的方法是_____(填序号)。
a.用少量冷水洗 b.用少量热水洗 c.用酒精洗
(5)乙酰苯胺粗品因含杂质而显色,欲用重结晶进行提纯,步骤如下:热水溶解、
_______________、过滤、洗涤、干燥(选则正确的操作并排序)。
a.蒸发结晶 b.冷却结晶 c.趁热过滤 d.加入活性炭
(6)该实验最终得到纯品 8.1g,则乙酰苯胺的产率是______________ %。
(7)如图的装置有 1 处错误,请指出错误之处____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设nA为阿伏伽德罗常数的数值,下列说法正确的是
A. 23g Na 与足量H2O反应完全后可生成nA个H2分子
B. 1 molCu和足量热浓硫酸反应可生成nA个SO3分子
C. 标准状况下,22.4L N2和H2混合气中含nA个原子
D. 3mol单质Fe完全转变为Fe3O4,失去8nA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)比较氧元素和氟元素的非金属性强弱:O_______F(填“<”“>或”“=”);用一个化学方程式说明两者非金属的相对强弱______________________________________。
(2)2002年1月18日在《科学》期刊中报导罗马大学的Fulvio Cacace及其同事发现氮的一种同素异形体N4,已知N4所有原子均满足8电子稳定结构。写出N4的结构式_______________。
(3)CO2和SiO2均是IVA族元素氧化物,CO2常温为气态,SiO2为高熔点固体。请分析原因_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芬太尼属于管制类药物,可用作镇痛麻醉药。其合成路线如下:
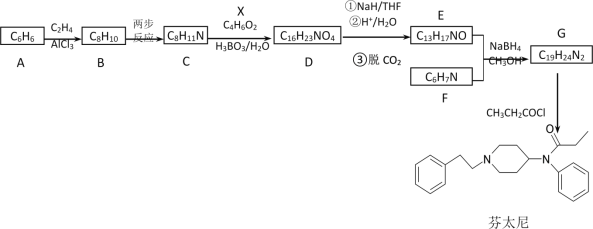
已知信息: ①RX+![]()
![]()
![]()
②RCH2COOR′+R″COOR′′′![]()
![]()
③![]() + CH2=CH2
+ CH2=CH2![]()
![]()
(1)下列说法正确的是______________。
A.化合物B到C的转变涉及到的两步反应依次是加成反应、取代反应
B.化合物C具有碱性,能与盐酸反应
C.化合物F可通过化合物A一步反应制备得到
D.芬太尼的分子式是C22H28N2O
(2)化合物X的结构简式是________________________。
(3)D→E的转化过程有多个中间产物,写出D在NaH/THF条件下发生反应的化学方程式______________________________。
(4)有机物Y(C4H7O2N)是有机物X的含氮衍生物,同时符合下列条件的Y的同分异构体的结构简式_________________________。
①分子中有一个六元环;
②1HNMR谱和IR谱检测表明分子中有3种化学环境不同的氢原子,没有过氧键(-O-O-)。
(5)设计以NH3和X为原料制备M(![]() )的合成路线(无机试剂任选,合成中须用到上述②③两条已知信息,用流程图表示)______________。
)的合成路线(无机试剂任选,合成中须用到上述②③两条已知信息,用流程图表示)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海南粗榧新碱具有抗肿瘤、抗炎等作用,其中间体G的合成线路如图:
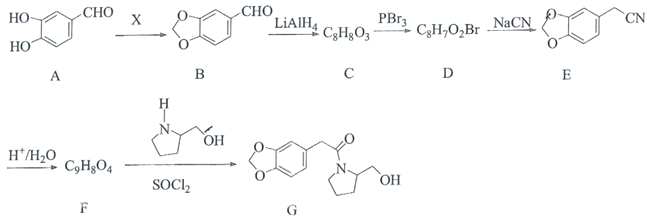
已知:
①R-COOH+R′-NH2![]()
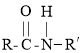 +H2O;
+H2O;
②R-CN![]()
![]()
回答下列问题:
(1)X为醛类物质,其名称为________,C中含氧官能团的名称为________。
(2)C→D的反应类型为________。
(3)化合物F的结构简式为________。
(4)B与新制的氢氧化铜悬浊液反应的化学方程式为________。
(5)有机物Y是A的同分异构体,满足条件:①能与![]() 溶液发生显色反应,②
溶液发生显色反应,②![]() 与足量金属Na反应生成
与足量金属Na反应生成![]() ,③结构中含“
,③结构中含“![]() ”,Y共有________种,其中核磁共振氢谱显示为4组峰,且峰面积比为
”,Y共有________种,其中核磁共振氢谱显示为4组峰,且峰面积比为![]() 的物质为________(写出其中一种结构简式)。
的物质为________(写出其中一种结构简式)。
(6)设计以![]() 为起始原料制备
为起始原料制备![]() 的合成线路(无机试剂任选) ________。
的合成线路(无机试剂任选) ________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com