
【题目】肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4H2O).
CO(NH2)+2NaOH+NaClO═Na2CO3+N2H4H2O+NaCl
(1)实验一:制备NaClO溶液.(实验装置如图1所示)
①配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有(填标号).
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
②锥形瓶中发生反应的化学方程式是 .
③因后续实验需要,需利用中和滴定原理测定反应后锥形瓶中混合溶液的NaOH的浓度.请选用所提供的试剂,设计实验方案.提供的试剂:H2O2溶液、FeCl2溶液、0.1000molL﹣1盐酸、酚酞试液;
(2)实验二:制取水合肼.(实验装置如图2所示)
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应.加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分.(已知:N2H4H2O+2NaClO═N2↑+3H2O+2NaCl)分液漏斗中的溶液是(填标号).
A.CO(NH2)2溶液B.NaOH和NaClO混合溶液
选择的理由是 .
(3)实验三:测定馏分中肼含量.
称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液,移出25.00mL,用0.1000molL﹣1的I2溶液滴定.滴定过程中,溶液的pH保持在6.5左右.(已知:N2H4H2O+2I2═N2↑+4HI+H2O)
①滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是 .
②实验测得消耗I2溶液的平均值为18.00mL,馏分中水合肼(N2H4H2O)的质量分数为 .
【答案】
(1)BD;Cl2+2NaOH=NaClO+NaCl+H2O;取一定量锥形瓶内混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用0.100mol?L﹣1盐酸滴定,重复上述操作2~3次
(2)B;如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化
(3)NaHCO3会与滴定过程中产生的HI反应;9%
【解析】解:(1)①配制一定质量分数的溶液时,溶解时需要烧杯、玻璃棒,所以答案是:BD;②锥形瓶中氯气和NaOH反应生成氯化钠、次氯酸钠和水,所以答案是:Cl2+2NaOH=NaClO+NaCl+H2O;③中和滴定测定混合溶液中NaOH的浓度时,需要排除溶液里的NaClO的干扰,可通过加入还原性的H2O2除去NaClO,然后滴加酚酞指示剂,再用标准的盐酸滴定测出NaOH溶液的浓度,所以答案是:取一定量锥形瓶内混合溶液,加入适量的H2O2溶液后,滴加2~3滴酚酞试液,用 0.100molL﹣1盐酸滴定,重复上述操作2~3次;(2)反应CO(NH2)+2NaOH+NaClO=Na2CO3+N2H4H2O+NaCl中,水合肼(N2H4H2O)作还原剂,具有还原性,易被次氯酸钠氧化,所以答案是:A;如果次氯酸钠溶液装在烧瓶中,反应生成的水合肼会被次氯酸钠氧化;(3)①NaHCO3能控制溶液的pH在6.5左右,是因为碳酸氢钠和碘化氢反应,所以答案是:NaHCO3会与滴定过程中产生的HI反应;②结合反应定量关系计算得到馏分中水合肼(N2H4H2O)的质量分数,
N2H2H2O+2I2=N2+4HI+H2O
1 2
n 0.1000mol/L×0.018L
n=0.0009mol
250ml溶液中含有的物质的量=0.0009mol× ![]() =0.009mol
=0.009mol
水合肼(N2H2H2O)的质量分数= ![]() ×100%=9.0%
×100%=9.0%
所以答案是:9%.


科目:高中化学 来源: 题型:
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物,E的合成路线如图(部分反应条件和试剂略): 已知:
已知:  (R1和R2代表烷基)
(R1和R2代表烷基)
请回答下列问题:
(1)试剂Ⅰ的名称是 , 试剂Ⅱ中官能团的名称是 , 第②步的反应类型是 .
(2)第①步反应的化学方程式是 .
(3)第⑥步反应的化学方程式是 .
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是 .
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH.若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X和Y发生缩聚反应所得缩聚物的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的原因是( )
A. 相对原子质量逐渐增大B. 核电荷数逐渐增大
C. 核外电子排布呈周期性变化D. 元素的化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是海水中含量较多的金属元素,单质镁、镁合金以及镁的化合物在科学研究和工业生产中用途非常广泛.
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(s)△H1=﹣74.5kJmol﹣1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s)△H2=﹣64.4kJmol﹣1
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)△H3
则△H3=kJmol﹣1
(2)工业上可用电解熔融的无水氯化镁获得镁.其中氯化镁晶体脱水是关键的工艺之一.一种正在试验的氯化镁晶体脱水的方法是:先将MgCl26H2O转化为MgCl2NH4ClnNH3 , 然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为;
(3)镁的一种化合物氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等.为了确定实验室制备的Mg(ClO3)26H2O的纯度,做如下试验:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL 1.000molL﹣1的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100molL﹣1 K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O.
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL.产品中Mg(ClO3)26H2O的纯度为(用百分号表示,精确到小数点后一位)
(4)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率如1图所示.250~300℃时,温度升高而乙酸的生成速率降低的原因是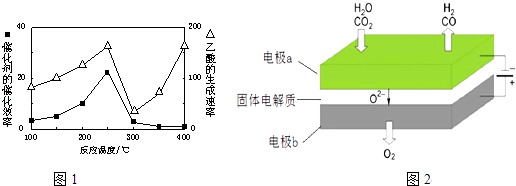
(5)Li2O、Na2O、MgO均能吸收CO2 .
①如果寻找吸收CO2的其它物质,下列建议合理的是
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4 , Li4SiO4用于吸收、释放CO2 , 原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2 , Li4SiO4再生,说明该原理的化学方程式是
(6)利用反应A可将释放的CO2转化为具有工业利用价值的产品.反应A:CO2+H2O ![]() CO+H2+O2高温电解技术能高效实现(3)中反应A,工作原理示意图如图2:CO2在电极a放电的反应式是 .
CO+H2+O2高温电解技术能高效实现(3)中反应A,工作原理示意图如图2:CO2在电极a放电的反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是 ( )
A.用石灰、碳酸钠等碱性物质处理废水中的酸
B.氯气可用于自来水杀菌消毒
C.氢氧化铝可用于中和过多胃酸
D.用谷物酿造出酒和醋,酿造过程中只发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释物质用途或现象的反应方程式不正确的是( )
A.汽车尾气中发生的催化转化反应:2NO+2CO ![]() N2+2CO2
N2+2CO2
B.铝热反应用于焊接钢轨:2Al+Fe2O3 ![]() Al2O3+2Fe
Al2O3+2Fe
C.燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2 ![]() 2CaSO3+2CO2
2CaSO3+2CO2
D.用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+CO![]() ═CaCO3+SO
═CaCO3+SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)地壳中含量第一金属元素构成的单质A与化合物B(分子量为232)发生置换反应,产物为黑色固体C和另一单质D,单质D与水蒸气在高温下可得到B.则
(i)写出构成金属单质A的元素在周期表中的位置为 .
(ii)写出D与水蒸气反应的化学方程式 .
(2)某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用工艺设计如下: 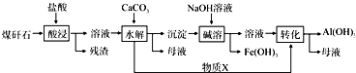
(i)物质X的化学式为 . “碱溶”时反应的离子方程式为 .
(ii)为加快“酸浸”时的速率,可采取的措施有、等.(填两种即可)
(iii)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4.为了获得更多产品Al(OH)3 , 从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续操作的实验方案是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量氯气通入KI溶液中,振荡,再加入CCl4,振荡,静置,观察到的现象是( )
A. 有紫黑色固体析出B. 形成均匀的紫红色溶液
C. 液体分层,下层紫红色D. 液体分层,上层紫红色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com