
����Ŀ��NaBiO3����Ϊ�ⶨ�̵���������Bi2O3�ڵ�����ҵ���Ź㷺Ӧ�ã������ø�ѡ���Ļ����(��Ҫ�ɷ���Bi2S3,��������SiO2������)���Ʊ���������������:
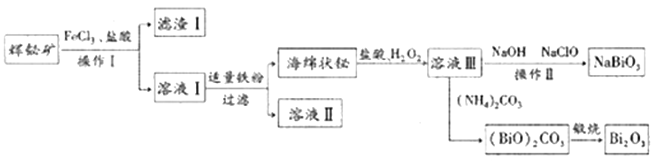
��֪:NaBiO3������ˮ��
�ش���������
��1����Һ������Ҫ�ɷ�ΪBiCl3��FeCl2,������������Ҫ�ɷ���________(д��ѧʽ)��
��2�������������ᡢH2O2��Ӧ�Ļ�ѧ����ʽ��__________
��3������Һ���м���NaOH��NaClO������Ӧ�����ڷ���ʽ��______���ӷ�Ӧ��Ļ����ϵ�л�ô���NaBiO3,����������_________��
��4��һ���¶��£���ˮ��ͨ��CO2���õ� (NH4)2CO3��NH4HCO3�����ʣ���Һ�и����������ʵ���������pH�Ĺ�ϵ��ͼ��ʾ������CO2��ͨ�룬��Һ��c(OH-)/c(NH3��H2O)��______(��������������С������������)��pH=9ʱ����Һ��c(NH4+)+c(H+)=______(������Ũ�ȱ�ʾ)��

��5��ȡ����NaBiO3��Ʒ2.0g,����ϡ�����MnSO4��Һʹ����ȫ�ܽ⣬Ȼ���������Ƶ�0.5mol/LFeSO4��Һ�ζ����ɵ�MnO4-���ζ���ɺ�����22.00mLFeSO4��Һ�����������NaBiO3����Ϊ_________��
���𰸡� SiO2��S 2Bi+3H2O2+6HCl=2BiCl3+6H2O Na++Bi3++ClO-+4OH-=NaBiO3��+C1-+2H2O ���ˡ�ϴ�ӡ����� ��С 2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-) 77%
����������1������I��Fe3+���Խ�Bi2S3�е�S����ΪS���ʣ�SiO2���ʱȽ��ȶ��������ᷴӦ��������������Ҫ�ɷ�Ϊ��SiO2��S��
��2������Ա�H2O2�����������ķ���ʽΪ��2Bi+3H2O2+6HCl=2BiCl3+6H2O
��3�����ݷ�Ӧ����ͼ��֪�������з����ķ�ӦΪ��Na++Bi3++ClO-+4OH-=NaBiO3��+C1-+2H2O����Ҫ��ô���NaBiO3������Ҫ���������˳������ٽ���ϴ�ӡ�����ſ��Եõ�������NaBiO3�����Բ�����Ϊ�����ˡ�ϴ�ӡ����
��4��![]() ��Kb���䣬c(NH4+)��������ֵ���ϼ�С�����ݵ���غ㶨�ɣ�pH=9ʱ����Һ�д��ڵ���غ�c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)��
��Kb���䣬c(NH4+)��������ֵ���ϼ�С�����ݵ���غ㶨�ɣ�pH=9ʱ����Һ�д��ڵ���غ�c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)��
��5����5NaBiO3+2Mn2++14H+=2MnO4+5Na++5Bi3++7H2O��MnO4+5Fe2++8H+=5Fe3++Mn2++4H2O��֪��
5NaBiO32 MnO410Fe2+��
5 10
n(NaBiO3)0.5mo1L1��0.0220L
n(NaBiO3)=0.0055mol
�õ�����������������=0.0055mol��280g/mol/2.0g��100%=77%���ʴ�Ϊ��77%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ����Ȼ�ѧ����ʽΪ��N2(g)��3H2(g) ![]() 2NH3(g) ��H����92.4 kJ��mol��1���ֽ�1 mol N2(g)��3 mol H2(g)����һ�ݻ�Ϊ2 L���ܱ������У���500 ���½��з�Ӧ��10 minʱ�ﵽƽ�⣬NH3���������Ϊ������˵������ȷ����( )
2NH3(g) ��H����92.4 kJ��mol��1���ֽ�1 mol N2(g)��3 mol H2(g)����һ�ݻ�Ϊ2 L���ܱ������У���500 ���½��з�Ӧ��10 minʱ�ﵽƽ�⣬NH3���������Ϊ������˵������ȷ����( )


A. ���ﵽƽ��ʱ�������ϵ�ų�9.24 kJ��������H2��Ӧ���ʱ仯������ͼa��ʾ
B. ��Ӧ�����У��������ƽ����Է�������ΪM����������ܶ�Ϊd���������ѹǿΪp�����ߵı仯������ͼb
C. ��ͼc��ʾ��������͢�ﵽƽ��ʱ��NH3���������Ϊ����������ų���������������������֮��Ϊ92.4 kJ
D. ����ʼ��������Ϊ1 mol N2��3 mol H2���ڲ�ͬ�����´ﵽƽ��ʱ��NH3����������仯��ͼd��ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CuClΪ��ɫ����������ˮ���������Ҵ���ϡ�������ڿ�����Ѹ�ٱ���������ɫ��������ֽ�����ɺ�ɫ����֪CuCl+3Cl-=[CuCl4]3-�������Ե�Ʒ�Һ(��Ҫ��Cu2+��Fe3+)���Ʊ��Ȼ���ͭ�Ĺ�������ͼ����:
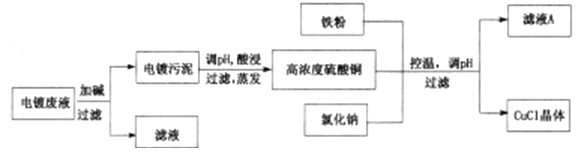
��1��ͼ�е����ۿ����ö�������������棬���Լ�����Ⱦ������ŷ�����д����SO2�������۽��з�Ӧ�����ӷ���ʽ:_____________��
��2���������γɵ������ʱ����ҺpH=9����֪Ksp[Fe(OH)3]=4��10-38��Ksp[Cu(OH)2]=2��10-20����ʱ��Һ��c(Fe3+)��c(Cu2+)=_______��
��3������CuCl����������ù��˵ķ������з������ٶԾ������ϴ�ӡ����й���ϴ�ӵ�˵����ȷ����______(�����)��
A.��Ϊ����CuCl�ij����ܽ�ƽ��,�����ñ���NaCl��Һϴ�ӿ��Խ���CuCl���ܽ��
B.��������ˮϴ������ֹ���ܽ��ˮ������CuOH
C.�������Ҵ�ϴ��ʹ��Ʒ���ٸ���
D.ϴ��ʱ��©���г�ֽ�����ʹ���ʾ����ܵ��ܽ�ﵽ��ȥ��Ŀ��
E.������ü�ѹ��������ϴ��ʱӦ���ȴ����������ͨ���ٹرճ����ã�Ȼ������©���м���ϴ��Һ
��4�������ι��˵���Һ��Ҫ�ɷ���_________��
��5��������������ʱ�Ļ�ѧ��Ӧ����ʽΪ___________________��
��6������������ͭ����ϴ�Ӹɾ��IJ�����_______________��
��7���Դ�ͭΪ�缫���һ��Ũ�ȵ��Ȼ�����Һ������һ���ĵ�ѹ�͵�����Ҳ�����Ƶ��Ȼ���ͭ��д�����ʱ��������Ӧʽ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ����㷺�Ľ����������Ȼ���������Ϊ��Ҫ�����
��1������ʦ��������ӡˢ��·��ķ�ˮ�л���ͭ�������FeCl3��Һ��������·�����
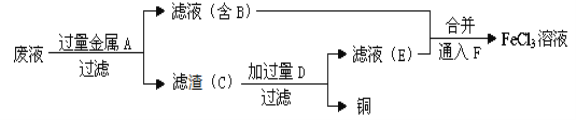
������C�Ļ�ѧʽΪ_____________��
��ͨ��F������Ӧ�Ļ�ѧ����ʽΪ_________________________��
��Ҫ֤��ij��Һ�в���Fe3+�����ܺ���Fe2+����������ʵ�����ʱ�����˳��Ϊ________��
a.����������ˮb.��������KMnO4��Һ c.��������KSCN��Һ
A��ac B��cb C��ca D��abc
(2)������������Fe3O4�������������ȶ���������������;�㷺�����ٴ���ϡ����\���ͻ�����ѧ�������DZ��Ӧ�õ��������ߣ�ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ�ǣ�
3Fe2++2S2O32-+O2+xOH- �TFe3O4��+S4O62-+2H2O����ش��������⣮
��ˮ�ȷ��Ʊ�Fe3O4�������ķ�Ӧ�У���ԭ����__________��
�ڷ�Ӧ�Ļ�ѧ����ʽ��x=______��
��ÿ����1molFe3O4����Ӧת�Ƶĵ���Ϊ____________mol����Fe2+��ԭ��O2�����ʵ���Ϊ______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:2CH3COCH3(1)![]() CH3COCH2COH(CH3)2(1)��ȡ����CH3COCH�ֱ���0����20���·�Ӧ,�����ת����(��)��ʱ��(t)�仯�Ĺ�ϵ��������ͼ��ʾ������˵����ȷ����
CH3COCH2COH(CH3)2(1)��ȡ����CH3COCH�ֱ���0����20���·�Ӧ,�����ת����(��)��ʱ��(t)�仯�Ĺ�ϵ��������ͼ��ʾ������˵����ȷ����
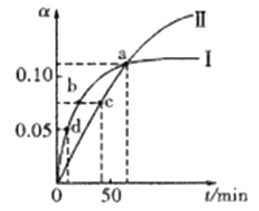
A. ��������ʾ20��ʱ��ת����Ӧ
B. �����¶�����߷�Ӧ���ƽ��ת����
C. ��a��ʱ,������������ʾ��Ӧ�Ļ�ѧƽ�ⳣ�����
D. ��ѧ��Ӧ���ʵĴ�С˳��Ϊ:d>b>c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ѽ��仯�����Ӧ��Խ��Խ�ܵ����ǵĹ�ע��
��1����̬Tiԭ�Ӻ�������Ų�������ܼ�������________������ͬ����Ԫ���У���̬ԭ�ӵ�δ�ɶԵ�����������ͬ����_______�֡�
��2���ѱȸ��ᣬ����Ӳ���������˵Ľṹ���ϡ���Ӳ�ȱ������ԭ����_________
��3������M�ܴ���ϩ����ϩ������ϩ�ȵľۺϣ���ṹ��ͼ��ʾ��
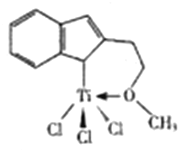
��M�У�̼ԭ�ӵ��ӻ���ʽ��__________�֡�
��M������___________(����)��
a.���� b.���� c.��λ�� d.��� e.���ӽ�
��4�����ʯ(TiO2)�Ǻ��ѵ���Ҫ����֮һ�����е��͵��ķ���ϵ�ṹ���侧���ṹ(��������ͬλ�õ�ԭ����ͬ)��ͼ��ʾ��
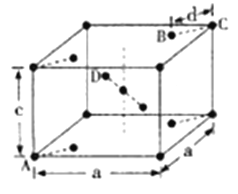
��4����A��B��C��D�У�������ԭ�ӵ���______
����A��B��C��ԭ������ֱ�ΪA(0,0,0)��(0.69a,0.69a,c)��C(a,a,c)����D��ԭ������ΪD(0.19a,___________,_____________);����������d=_________(�ô���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������滷����(b)����������Ľṹ��һֱ�ܵ��ṹ�����ۻ�ѧ�ҵ�ע�⣬������ת����ϵ������˵����ȷ����
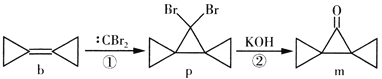
A. b������ԭ�Ӷ���һ��ƽ����
B. p���������Ƶ��Ҵ���Һ�м�������ϩ��
C. m��ͬ���칹�������ڷ����廯����Ĺ���5��
D. ��Ӧ���Ǽӳɷ�Ӧ����Ӧ������ȥ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɷ������·�Ӧ��P4��5O2===P4O10����֪�������л�ѧ����Ҫ���յ������ֱ�ΪP��P��a kJ��mol��1��P��O��b kJ��mol��1��P===O��c kJ��mol��1��O===O��d kJ��mol��1��������ͼ��ʾ�ķ��ӽṹ���й����ݹ���÷�Ӧ����H��������ȷ����(����)

A. (6a��5d��4c��12b) kJ��mol��1
B. (4c��12b��6a��5d) kJ��mol��1
C. (4c��12b��4a��5d) kJ��mol��1
D. (4a��5d��4c��12b) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20 mL 0��2 mol/L H2A��Һ�еμ�0��2 mol/L NaOH��Һ���й��������ʵ����仯����ͼ(����������H2A��������HA����������A2��)������ͼʾ�жϣ�����˵����ȷ����

A. H2A��ˮ�еĵ��뷽��ʽ�ǣ�H2A===H����HA����HA��![]() H����A2��
H����A2��
B. ��V(NaOH)��20 mLʱ����Һ�и�����Ũ�ȵĴ�С˳��Ϊ��c(Na��)>c(HA��)>c(H��)>c(A2��)>c(OH��)
C. �������Ũ�ȵ�NaOH��Һ��H2A��Һ��Ϻ�����Һ��ˮ�ĵ���̶ȱȴ�ˮ��
D. ��V(NaOH)��30 mLʱ����Һ�д������¹�ϵ��2c(H��)��c(HA��)��2c(H2A)��c(A2��)��2c(OH��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com