
【题目】是应用最广泛的金属,铁的氯化物、氧化物均为重要化合物。
(1)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
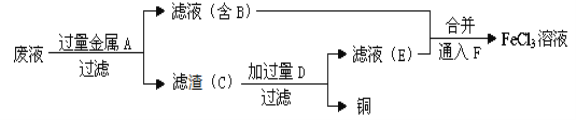
①滤渣C的化学式为_____________。
②通入F发生反应的化学方程式为_________________________。
③要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为________。
a.加入足量氯水b.加入足量KMnO4溶液 c.加入少量KSCN溶液
A.ac B.cb C.ca D.abc
(2)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具.水热法制备Fe3O4纳米颗粒的反应是:
3Fe2++2S2O32-+O2+xOH- ═Fe3O4↓+S4O62-+2H2O.请回答下列问题.
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是__________.
②反应的化学方程式中x=______.
③每生成1molFe3O4,反应转移的电子为____________mol,被Fe2+还原的O2的物质的量为______mol.
【答案】Fe、Cu 2FeCl2+Cl2=2FeCl3 C Fe2+ 和S2O32- 4 4 0.5
【解析】
(1)制取的是氯化铁溶液,金属A是铁,滤液B是氯化亚铁溶液,加入的铁过量,滤渣C是铁和铜;制取的是氯化铁,溶解铁,D加入应该是盐酸,氯化亚铁被氯气氧化为氯化铁,据以上分析解答。
(2)从电荷守恒的角度分析,可配平反应的离子方程式: 3Fe2++2S2O32-+O2+xOH- ═Fe3O4↓+S4O62-+2H2O ,反应中3Fe2+→Fe3O4,当3molFe2+参加反应时,有2molFe2+ 化合价升高,反应中Fe和S元素的化合价升高,被氧化,氧气为氧化剂,据以上分析解答。
(1)制取的是氯化铁溶液,金属A是铁;滤液B是氯化亚铁溶液;加入的铁过量,滤渣C是铁和铜;制取的是氯化铁,溶解铁,D加入应该是盐酸;氯化亚铁和氯气反应生成氯化铁,
①结合以上分析可知,滤渣C的化学式为Fe、Cu;
因此,本题正确答案是:Fe、Cu。
②结合以上分析可知,氯气能够将亚铁离子氧化成三价铁离子,反应方程式是: 2FeCl2+Cl2=2FeCl3 ;
综上所述,本题答案是:2FeCl2+Cl2=2FeCl3。
③鉴别某溶液中不含Fe3+而可能含有Fe2+的步骤为:先向溶液中加入含有KSCN的溶液,看是否有红色生成,若有红色生成则该溶液中含有Fe3+;若无红色生成,再向其中加入具有强氧化性的物质,观察是否有红色生成,若有红色生成,则该溶液中含有Fe2+。加入的氧化剂的本身颜色不能干扰该检验反应,紫红色的KMnO4溶液对于Fe3+和SCN-生成的红色物质有干扰,而黄色的氯水不会,故选ca 。
综上所述,本题选C。
(2) ①反应中Fe元素化合价部分升高为+3价,S元素化合价由+2价升高到+2.5价,则还原剂是. Fe2+ 和S2O32-;
因此,本题正确答案是: Fe2+ 和S2O32-。
②由电荷守恒可以知道,阳离子带的电荷总数等于阴离子带的负电荷总数,关系式为(+2)×3+(-2)×2+x×(-1)=-2,则x=4;
因此,本题正确答案是:4。
③Fe、S元素的化合价升高,O元素的化合价降低,由反应可以知道,该反应转移4e-,所以每生成1molFe3O4,由O元素的化合价变化可以知道,转移电子为1×2×[0-(-2)]=4,每生成1molFe3O4,消耗3molFe2+,其中有2molFe2+ 被氧化生成+3价,则被Fe2+还原的O2的物质的量为2/[2×(2-0)]=0.5mol;
因此,本题正确答案是:4,0.5。


科目:高中化学 来源: 题型:
【题目】在一恒温、恒容的密闭容器中存在化学平衡:H2(g)+I2(g) ![]() 2HI(g),已知H2和I2的起始浓度均为0.10molL-1,达到平衡状态时HI的浓度为0.16molL-1。若H2和I2的起始浓度均变为0.20molL-1,则平衡时H2的浓度为( )
2HI(g),已知H2和I2的起始浓度均为0.10molL-1,达到平衡状态时HI的浓度为0.16molL-1。若H2和I2的起始浓度均变为0.20molL-1,则平衡时H2的浓度为( )
A. 0.16molL-1 B. 0.08 molL-1 C. 0.04 molL-1 D. 0.02molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,Ⅰ、Ⅱ是两个完全相同的装置,分别装有10 mL相同浓度的盐酸,某学生分别在Ⅰ、Ⅱ的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,然后将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是
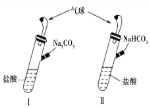
A. 装置Ⅰ的气球膨胀得快
B. 最终两试管中Na+、Cl-的物质的量分别相等
C. 若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol·L-1
D. 若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7∶8,E与B的质量比为1∶1。试回答:
(1)写出D元素基态原子的电子排布式:____________________________________。
(2)写出AB2的路易斯结构式:__________________。
(3)B、C两元素的第一电离能大小关系为________>________(填元素符号),原因是_______________。
(4)根据VSEPR模型预测C的氢化物的立体结构为________,中心原子C的轨道杂化类型为________。
(5)C的单质分子中π键的数目为________,B、D两元素的气态氢化物的稳定性大小关系为________>________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)称取一定质量的纯碱溶于水中,与适量的盐酸作用,下列关于盐酸的用量和气体产量的变化是(填偏大、偏小、不变)
①若纯碱中混有K2CO3,盐酸用量将____________;气体产量将_______________。
②若纯碱中混有NaHCO3,盐酸用量将___________;气体产量将_______________。
(2)写出下列离子方程式
①金属钠投入CuSO4溶液_____________________ 。②向饱和食盐水中通入足量氨气和二氧化碳:___________.
(3)向1L,1mol/L的氯化铝溶液中加入含氢氧化钠xmol的氢氧化钠溶液,当铝元素以Al(OH)3和AlO2-形式存在时x的取值范围是_______,当x=3.6时,Al(OH)3的质量为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。下列说法错误的是

A. 单核阴离子的还原性Y强于X
B. W的气态氢化物与其最高价含氧酸反应生成离子化合物
C. X、Y、Z最简单氢化物中稳定性最弱的是Y
D. 在元素周期表中118号元素与Z位于同一主族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBiO3可作为测定锰的氧化剂,Bi2O3在电子行业有着广泛应用,可利用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)来制备,工艺流程如下:
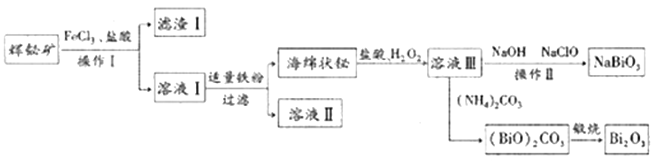
已知:NaBiO3难溶于水。
回答下列问题
(1)溶液Ⅰ中主要成分为BiCl3、FeCl2,则滤渣Ⅰ的主要成分是________(写化学式)。
(2)海绵铋与盐酸、H2O2反应的化学方程式是__________
(3)向溶液Ⅲ中加入NaOH和NaClO发生反应的离于方程式是______,从反应后的混合体系中获得纯净NaBiO3,操作Ⅱ包括_________。
(4)一定温度下,向氨水中通入CO2,得到 (NH4)2CO3、NH4HCO3等物质,溶液中各种微粒的物质的量分数与pH的关系如图所示。随着CO2的通入,溶液中c(OH-)/c(NH3·H2O)将______(填“增大”“减小”或“不变”)。pH=9时,溶液中c(NH4+)+c(H+)=______(用离子浓度表示)。

(5)取所得NaBiO3样品2.0g,加入稀硫酸和MnSO4溶液使其完全溶解,然后用新配制的0.5mol/LFeSO4溶液滴定生成的MnO4-,滴定完成后消耗22.00mLFeSO4溶液。则该样晶中NaBiO3纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解NaB(OH)4溶液制备H3BO3的原理如下图所示,下列叙述错误的是

A. M室发生的电极反应式:2H2O-4e-=O2↑+4H+
B. a、c为阴离子交换膜,b为阳离子交换膜
C. N室中:a%<b%
D. 理论上每生成1 mol H3BO3,两极室共产生标准状况下16.8 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到实验目的且符合操作要求的是
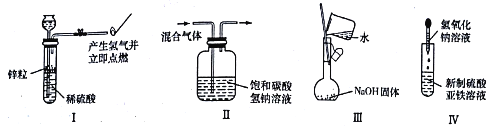
A. I可用于制备并检验氢气的可燃性
B. II可用于除去CO2中的HCl
C. 用Ⅲ来配制一定物质的量浓度的NaOH溶液
D. 用IV中操作制备氢氧化亚铁并观察其颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com