
【题目】已知:某些强酸盐的水溶液呈中性,如NaCl溶液,某些弱酸盐的水溶液呈碱性,如Na2CO3溶液。请根据如下图所示转化关系回答有关问题。A和B均为焰色反应呈黄色的水溶液,A呈中性,B呈碱性并具有强氧化性。
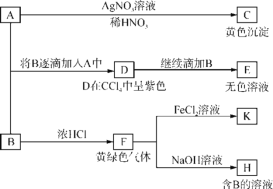
(1)写出C的化学式:________。
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式: ___________________,_____________________。
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:____________。
(4)检验K溶液中阳离子的简易方法是__________。
【答案】AgI 2I-+ClO-+H2O=I2+Cl-+2OH- I2+5ClO-+2OH-=2IO3-+5Cl-+H2O 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ 取少量K溶液于试管中,滴加少量的KSCN溶液,溶液变红
【解析】
A、B的焰色反应均为黄色,则A、B均含有Na元素;A和AgNO3溶液生成不溶于稀HNO3的黄色沉淀C为AgI,则说明A为NaI溶液;B和浓盐酸反应生成的黄绿色气体F为Cl2,且B呈碱性,则B为NaClO溶液,K为FeCl3溶液,H为NaCl和NaClO的混合溶液;将B逐滴滴入A中,NaClO将NaI氧化为I2(D),再继续加入B,NaClO将I2氧化,根据题(2)可以推测E为NaIO3溶液。
(1)根据分析,C为AgI;
(2)A为NaI溶液,D为I2,E为NaIO3溶液,A→D的离子方程式为:2I-+ClO-+H2O=I2+Cl-+2OH-,D→E的离子方程式为:I2+5ClO-+2OH-=2IO3-+5Cl-+H2O;
(3)K溶液为FeCl3溶液,向此溶液中通入SO2的离子方程式为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(4)K溶液中阳离子为Fe3+,检验该阳离子的方法为:取少量K溶液于试管中,滴加少量的KSCN溶液,若溶液变红,说明该溶液中含有Fe3+。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L、体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是
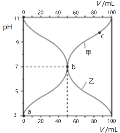
A.点c对应的溶液中有:c(B+)+c(BOH)=0.1molL-1
B.点b对应的溶液中有:c(B+)=c(A-)
C.曲线甲表示加入BOH溶液的体积与pH的关系曲线
D.在由点a到点c的过程,水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】指出下列分子中带*号的原子采用的杂化方式:
(1)HO2________
(2) _________
_________
(3)*CO2________
(4)CHCH2OH_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g);△H=-akJ/mol(a>0)。在一定温度下,在一个恒压的密闭容器中充入2mol NO和2mol CO,下列有关该反应说法正确的是
N2(g)+2CO2(g);△H=-akJ/mol(a>0)。在一定温度下,在一个恒压的密闭容器中充入2mol NO和2mol CO,下列有关该反应说法正确的是
A.反应达到平衡时,放出的热量为akJ
B.当压强不再变化时,反应达到平衡状态
C.当NO和CO转化率相同时,反应达到平衡状态
D.混合气体的密度不再变化时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M溶液受热会发生分解反应。体积均为2L的4组溶液(忽略反应前后体积的变化),M的物质的量随时间的变化如下表,则下列说法不正确的是
0min | 10min | 20min | 30min | 40min | 50min | 60min | ||
① | 10℃ | 1.1 | 0.90 | 0.80 | 0.73 | 0.68 | 0.65 | 0.65 |
② | 10℃ | a | 0.70 | 0.65 | 0.65 | 0.65 | 0.65 | 0.65 |
③ | 25℃ | 1.0 | 0.70 | 0.50 | 0.35 | 0.25 | 0.20 | 0.20 |
④ | 30℃ | 2.0 | 1.4 | 0.90 | 0.50 | 0.20 | 0.13 | 0.13 |
A.在10-20min内,实验①中M的平均分解速率为0.005mol/(L·min)
B.a>1.1,且说明浓度越大反应速率越快
C.对比实验①和④,不能说明M的平均反应速率随温度升高而增大
D.不考虑其它影响因素,仅由③可知,反应物浓度越大反应速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某空间站能量转化系统的局部示意图:其中燃料池采用KOH溶液为解液,下列有关说法中不正确的是( )

A.燃料电池系统产的能量实际上来自于太阳能
B.该能量转化系统中的水可以循环利用
C.背日面时,燃料电池负极反应为:H2+2OH﹣﹣2e﹣═2H2O
D.向日面时,水电解产生的H2和O2的体积比为1:2(相同条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)环氧乙烷(EO)是一种重要的化工原料,可用于生产乙二醇、乙醇胺等化工产品,目前乙烯直接氧化法被广泛应用于环氧乙烷的生产并得到广泛关注。制备环氧乙烷工艺装置如图: ,其中“反应床”中发生的反应有:
,其中“反应床”中发生的反应有:
主反应①:2CH2=CH2(g)+O2(g) ![]() 2
2![]() (g) △H1=-221.0kJ/mol;
(g) △H1=-221.0kJ/mol;
副反应②:CH2=CH2(g)+3O2(g) ![]() 2CO2(g)+2H2O(g) △H2=-1323.0kJ/mol;
2CO2(g)+2H2O(g) △H2=-1323.0kJ/mol;
副反应③:2![]() (g)+5O2(g)
(g)+5O2(g) ![]() 4CO2(g)+4H2O(g) △H3;
4CO2(g)+4H2O(g) △H3;
副反应④:![]() (g)
(g)![]() CH3CHO(g) △H3=-115.0kJ/mol
CH3CHO(g) △H3=-115.0kJ/mol
已知:环氧乙烷选择性是指乙烯进行反应①生成环氧乙烷的优势
(1)写出反应③的△H3=______kJ/mol;
(2)下列有关环氧乙烷制备说法不正确的是______
A.由图1可知,进料气体的初始温度对环氧乙烷的选择性影响不大,可得出乙烯的转化率受初始温度影响不大
B.由图2可知,原料气的流速加快,乙烯转化率下降;主要是原料气与催化剂接触时间过短造成
C.图2表明,原料气的流速加快,环氧乙烷选择性略微增大;主要原因是温度得到较好控制,催化剂活性较强
D.若进料气中O2比例增大,环氧乙烷产率降低;其中主要原因是环氧乙烷转化为乙醛
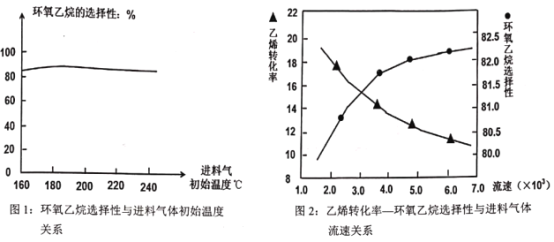
(3)已知“反应床”中压强对乙烯转化率和环氧乙烷选择性的影响如图3:
请解释当反应体系中压强高于2.4Mpa,导致环氧乙烷选择性下降的主要原因:______。
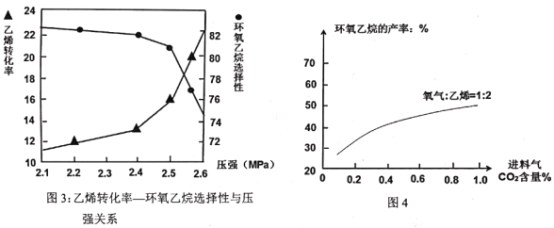
(4)不同进料组分,环氧乙烷产率不同;其中进料气n(O2):n(C2H4)=1:2时,随CO2含量变化,环氧乙烷的产率变化如图4。请在图4上画出进料气n(O2):n(C2H4)=3:1时,随CO2含量变化,环氧乙烷的产率变化曲线_______。
(二)环氧丙烷是一种重要的化工原料,且广泛用途。有机电化学法电解合成环氧丙烷是一种常见的生成工艺;其原理是将丙烯与电解饱和食盐水的电解产物反应,转化为氯丙醇(CH3CHOHCH2Cl),氯丙醇进一步反应生成环氧丙烷。其电解简易装置如图。
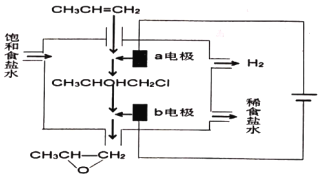
(1)写出a电极的电极反应式:__________;
(2)写出b电极区域生成环氧丙烷的化学方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设nA为阿伏伽德罗常数的数值,下列说法正确的是
A. 23g Na 与足量H2O反应完全后可生成nA个H2分子
B. 1 molCu和足量热浓硫酸反应可生成nA个SO3分子
C. 标准状况下,22.4L N2和H2混合气中含nA个原子
D. 3mol单质Fe完全转变为Fe3O4,失去8nA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验。
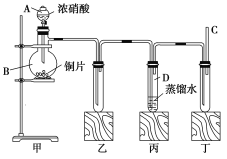
回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是_____,该装置中发生反应的化学方程式为___。
(2)实验过程中,装置乙、丙中出现的现象分别是__________、____________;装置丙中的试管内发生反应的离子方程式为________________(不是离子反应的不写)。
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________色,为了证明铁元素在该反应中的产物,可以再向溶液中滴加KSCN溶液,溶液变为________色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com