
【题目】部分氧化的铁铜合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

(1)滤液A中的阳离子为_____________.
(2)样品中Fe元素的质量为___________g
(3)向滤液A中加H2O2,反应的离子方程式为_____________________.
(4)向样品中加足量稀硫酸时共生成H2O_________g
【答案】 Fe2+ H+ 2.24 2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O 0.36
【解析】根据流程图,足量稀硫酸,由于氧化性:Fe3+>Cu2+>H+,铁离子优先与铁反应,滤液A不含铜离子,且有气体氢气生成,滤液A中不含铁离子,滤渣3.2g为金属铜,物质的量为3.2g/64g·mol-1=0.05mol,即合金样品中总共含有铜元素0.05mol,滤液A中加入足量氢氧化钠溶液,所得滤渣灼烧得到的固体3.2g为Fe2O3,其物质的量=3.2g/160g·mol-1=0.02mol,铁元素的物质的量为0.04mol,滤液A溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,硫酸含氢离子0.08mol,其中部分氢离子生成氢气,其余的H+和合金中的氧结合成水。
(1)滤液A中阳离子为Fe2+、H+,故A错误;(2)合金中Fe元素质量=0.04mol×56g·mol-1=2.24g;(3)向滤液A中加H2O2,将Fe2+ 氧化,反应的离子方程式为 2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O;(4)向样品中加足量稀硫酸时共生成H2O的质量:m(H2O)= ![]() =0.36g
=0.36g


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学反应C(s) + H2O(g) CO(g) + H2(g) – Q 达到平衡,下列叙述正确的是
A.减小压强,平衡向正反应方向移动
B.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.加入水蒸气使容器压强增大,平衡向逆反应方向移动
D.加入固体碳,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:

回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3 = Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后NaNO3与FeO·Cr2O3的系数比为__________。该步骤能否_________(填“能”或“不能”)使用陶瓷容器。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是_______________及含硅杂质。
(3)步骤④调滤液2的pH使之变_________ (填“大”或“小”),理由是________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到10℃得到的K2Cr2O7固体产品最多。

步骤⑤的化学方程式为 _________________。
(5)某工厂用76Kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品41.16Kg, 则产率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

(1)步骤Ⅰ中涉及的主要反应用离子方程式表示为_____.
(2)步骤Ⅱ中试剂①是_____(填代号).
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO的目的是_____.
(4)步骤Ⅳ获得硫酸铜晶体,需要经过_____、_____、过滤等操作.
(5)孔雀石与焦炭一起加热可以生成Cu及其它无毒物质,写出该反应的化学方程式_____.
(6)测定硫酸铜晶体(CuSO4xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在____(填实验仪器名称)中加热至质量不再改变时,称量粉末的质量为1.6g.则计算得x=_____(计算结果精确到0.1).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用优质大理石与稀盐酸反应制取CO2 , 实验结果如图所示,对于图中曲线的叙述正确的是( ) 
A.AB段表示反应速率最慢
B.BC段表示反应速率最快,在该时间内收集到的气体最多
C.OC段表示随时间增加,反应速率逐渐增大
D.OC段表示反应产物中气体体积随时间的变化关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应3A(g) ![]() 3B(?)+C(?) ΔH>0,达到化学平衡后,改变一个条件,其他条件不变。
3B(?)+C(?) ΔH>0,达到化学平衡后,改变一个条件,其他条件不变。
(1)升高温度:
①若B、C都是气体,气体的平均相对分子质量____(用“变大”、“变小”或“不变”填空,下同);
②若B、C都不是气体,气体的平均相对分子质量____;
③若B是气体,C不是气体,气体的平均相对分子质量____。
(2)增大压强:
①若B是气体,C不是气体,气体的平均相对分子质量____(填“变大”、“变小”或“不变”);
②若B、C均为气体,则气体的平均相对分子质量____(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为反应2H2(g)+O2(g)=2H2O(g)的能量变化示意图.下列说法正确的是( ) 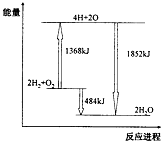
A.拆开2molH2(g)和1 molO2 (g)中的化学键成为H、O原子,共放出1368 kJ能量
B.由H、O原子形成2 molH2O(g),共吸收1852 kJ能量
C.2 molH2(g)和1 molO2(g)反应生成2 molH2O(l),共吸收484 kJ能量
D.2 molH2(g)和1 molO2 (g)反应生成2 moIH2O(g),共放出484 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com