
ЎѕМвДїЎїДі»ЇС§РЛИ¤РЎЧйОЄМЅѕїSO2µДРФЦКЈ¬°ґИзНјЛщКѕЧ°ЦГЅшРРКµСйЎЈ
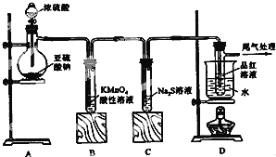
ПВБРОКМвЈє
(1)Ч°ЦГAЦРКў·ЕСЗБтЛбДЖµДТЗЖчГыіЖКЗ___ Ј¬·ўЙъ·ґУ¦µД»ЇС§·ЅіМКЅОЄ___Ј»
(2)КµСй№эіМЦР,Ч°ЦГBЎўCЦР·ўЙъµДПЦПу·Ц±рКЗ___Ўў___,ХвР©ПЦПу·Ц±рЛµГчSO2ѕЯУРµДРФЦККЗ___єН___Ј»Ч°ЦГCЦР·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅОЄ___Ј»
(3)Ч°ЦГDµДДїµДКЗМЅѕїSO2УлЖ·ємЧчУГµДїЙДжРФЈ¬ЗлРґіцКµСйІЩЧчј°ПЦПу___Ј»
(4)ОІЖшїЙІЙУГ___ИЬТєОьКХ
Ўѕґр°ёЎїХфБуЙХЖї Na2SO3+H2SO4(ЕЁ)=Na2SO4+SO2Ўь+H2O ИЬТєУЙЧПємЙ«±дОЄОЮЙ« ОЮЙ«ИЬТєЦРіцПЦ»ЖЙ«»лЧЗ »№ФРФ Сх»ЇРФ 2S2+5SO2+2H2O=4HSO3+3SЎэ Ж·ємИЬТєНЛЙ«єуЈ¬№Ш±Х·ЦТєВ©¶·µДРэИыЈ¬µгИјѕЖѕ«µЖјУИИЈ¬ИЬТє»ЦёґОЄємЙ« ЗвСх»ЇДЖЎЈ
ЎѕЅвОцЎї
ЕЁБтЛбУлСЗБтЛбДЖ№ММе·ґУ¦ЙъіЙSO2Ј¬ЅбєПSO2µД»№ФРФЎўИхСх»Їј°ЖЇ°ЧРФ·ЦОцЈ¬ЧўТвSO2КЗЛбРФСх»ЇОпј°¶Ф»·ѕіµДОЫИѕЎЈ
(1) Ч°ЦГAЦРКў·ЕСЗБтЛбДЖµДТЗЖчГыіЖКЗХфБуЙХЖїЈ»ЕЁБтЛбУлСЗБтЛбДЖ·ґУ¦ЙъіЙ¶юСх»ЇБтєНЛ®ЎўБтЛбДЖ,»ЇС§·ЅіМКЅОЄЈєNa2SO3+H2SO4(ЕЁ)=Na2SO4+SO2Ўь+H2OЈ»
(2)¶юСх»ЇБтѕЯУР»№ФРФЈ¬ДЬ№»»№ФЛбРФµДёЯГМЛбјШЈ¬К№ИЬТєЧПЙ«НКИҐЈ»¶юСх»ЇБтѕЯУРСх»ЇРФЈ¬ДЬ№»Сх»ЇБтАлЧУЙъіЙµҐЦКБтЈ¬№эБїµД¶юСх»ЇБтНЁИлµЅБт»ЇДЖИЬТєЦР·ўЙъСх»Ї»№Ф·ґУ¦ЙъіЙСЗБтЛбЗвДЖєНБтµҐЦКЈ¬АлЧУ·ЅіМКЅОЄЈє2S2+5SO2+2H2O=4HSO3+3SЎэЈ»
(3)¶юСх»ЇБтѕЯУРЖЇ°ЧРФЈ¬ДЬ№»К№Ж·ємИЬТєНКЙ«Ј¬µ«КЗ¶юСх»ЇБтЖЇ°ЧРФѕЯУРІ»ОИ¶ЁМШµгЈ¬ЛщТФКЬИИОЮЙ«ИЬТє»ЦёґФАґСХЙ«Ј¬КµСйІЩЧчОЄЈєЖ·ємИЬТєНЛЙ«єуЈ¬№Ш±Х·ЦТєВ©¶·µДРэИыЈ¬µгИјѕЖѕ«µЖјУИИЈ¬ИЬТє»ЦёґОЄємЙ«Ј»
(4)¶юСх»ЇБтУР¶ѕЈ¬ОЄЛбРФСх»ЇОпЈ¬ДЬ№»УлЗвСх»ЇДЖ·ґУ¦Ј¬їЙТФУГЗвСх»ЇДЖОьКХ¶аУаµД¶юСх»ЇБтЎЈ



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїёхФЄЛШј°Жд»ЇєПОпФЪЙъІъЎўЙъ»оЦРѕЯУР№г·єµДУГНѕЎЈТФДіёхїуКЇ(ЦчТЄіЙ·ЦКЗCr2O3Ј¬є¬Fe2O3ЎўSiO2µИФУЦК)ОЄФБПЙъІъCr2O3µДБчіМИзПВЈє
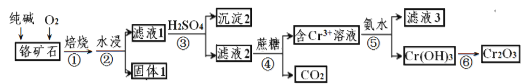
(1)Cr2O3ФЪ±єЙХК±ЙъіЙNa2CrO4Ј¬РґіцµЪўЩІЅ·ўЙъµДЛщУР·ЅіМКЅ_________ЎЈ
(2)іБµн2µД»ЇС§КЅОЄ_______ЎЈ
(3)ІЅЦиўЫЦРCrO42-ЧЄ»ЇіЙCr2O72- Ј¬РґіцЖдАлЧУ·ЅіМКЅ_______Ј¬БтЛбДЬ·с»»іЙСОЛбІўЛµГчЖдАнУЙ______ЎЈ
(4)ВЛТє3ЦРЦчТЄИЬЦКµД»ЇС§КЅОЄ____________ЎЈ
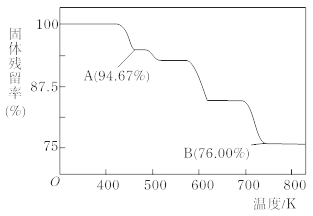
(5)CrO3µДИИОИ¶ЁРФЅПІоЈ¬јУИИК±ЦрІЅ·ЦЅвЈ¬Жд№ММеІРБфВКЛжОВ¶ИµД±д»ЇИзПВНјЛщКѕЈ¬ФтBµгК±ёхµДСх»ЇОп»ЇС§КЅОЄ_______ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДО±ШВе¶ыКЗТ»ЦЦУГУЪСЄ№ЬА©ХЕµДЅµСЄС№Т©ОпЈ¬Т»ЦЦєПіЙДО±ШВе¶ыЦРјдМеGµДІї·ЦБчіМИзПВЈє
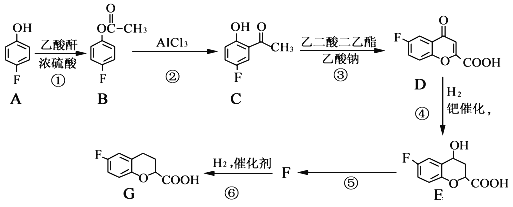
ТСЦЄЈєТТЛбфыµДЅб№№јтКЅОЄ![]() ЎЈ
ЎЈ
Зл»ШґрПВБРОКМвЈє
ЈЁ1Ј©AµДГыіЖКЗ______Ј»BЦРЛщє¬µДє¬Сх№ЩДЬНЕµДГыіЖКЗ______.
ЈЁ2Ј©GµД·ЦЧУКЅОЄ______.
ЈЁ3Ј©·ґУ¦ўЭµД»ЇС§·ЅіМКЅОЄ______Ј¬ёГ·ґУ¦µД·ґУ¦АаРНКЗ______.
ЈЁ4Ј©РґіцТ»ЦЦВъЧгПВБРМхјюµДEµДН¬·ЦТм№№МеµДЅб№№јтКЅЈє___________.
ўсЈ®±Ѕ»·ЙПЦ»УРИэёцИЎґъ»щ
ўтЈ®єЛґЕ№ІХсЗвЖЧНјЦРЦ»УР4ЧйОьКХ·е
ўуЈ®1 molёГОпЦКУлЧгБїNaHCO3ИЬТє·ґУ¦ЙъіЙ2 molCO2
ЈЁ5Ј©ёщѕЭТСУРЦЄК¶ІўЅбєППа№ШРЕПўЈ¬РґіцТФ![]() ОЄФБПЦЖ±ёµД
ОЄФБПЦЖ±ёµД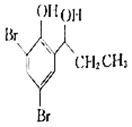 єПіЙВ·ПЯБчіМНјЈЁОЮ»ъКФјБИОСЎЈ©______Ј¬єПіЙВ·ПЯБчіМНјКѕАэИзПВЈєCH3CH2Br
єПіЙВ·ПЯБчіМНјЈЁОЮ»ъКФјБИОСЎЈ©______Ј¬єПіЙВ·ПЯБчіМНјКѕАэИзПВЈєCH3CH2Br ![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДіН¬С§АыУГПВНјЅшРРЕзИЄКµСйЈ¬ТСЦЄФІµЧЙХЖїДЪідВъXЖшМеЈ¬ЅєН·µО№ЬДЪЧ°УРЙЩБїYТєМеЈ¬ЙХ±ДЪЧ°УРЧгБїZТєМеЈ¬ПВБРЧйєПДЬЅшРРЕзИЄКµСйЗТЧоЦХТєМеТ»¶ЁДЬідВъХыёцЙХЖїµДКЗЈЁ Ј©
XЖшМе | YКФјБ | ZКФјБ | |
AЈ® | NO2 | H2O | H2O |
BЈ® | CO2 | H2O | H2O |
CЈ® | HCl | ±ҐєНКіСОЛ® | Л® |
DЈ® | NO2 єНO2 | H2O | H2O |
A.AB.BC.CD.D
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїєгОВєгИЭГЬ±ХИЭЖчЦРЈ¬·ўЙъ·ґУ¦ИзПВЈєX(g) + 2Y(g) ![]() W(g) + Z(g)ЎЈПВБРОпАнБїІ»ФЩёД±дЈ¬І»ДЬ±нГч·ґУ¦КЗ·сТСґпµЅЖЅєвЧґМ¬µДКЗ
W(g) + Z(g)ЎЈПВБРОпАнБїІ»ФЩёД±дЈ¬І»ДЬ±нГч·ґУ¦КЗ·сТСґпµЅЖЅєвЧґМ¬µДКЗ
A. YµДОпЦКµДБїЕЁ¶ИB. »мєПЖшМеµДГЬ¶И
C. »мєПЖшМеµДС№ЗїD. XµДЧЄ»ЇВК
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїИзНјКЗN2УлH2·ґУ¦µДДЬБї±д»ЇЗъПЯНјЎЈПВБРРрКцХэИ·µДКЗ
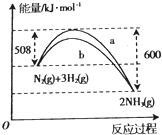
A. ёГ·ґУ¦µДИИ»ЇС§·ЅіМКЅОЄЈєN2(g) + 3H2(g) ![]() 2NH3(g)Ј¬ЎчH = +92 kJ/mol
2NH3(g)Ј¬ЎчH = +92 kJ/mol
B. bЗъПЯКЗјУИлґЯ»ЇјБК±µДДЬБї±д»ЇЗъПЯ
C. јУИлґЯ»ЇјБЈ¬ёГ»ЇС§·ґУ¦µД·ґУ¦ИИјхРЎ
D. јУИлґЯ»ЇјБїЙФцґуХэ·ґУ¦ЛЩВКЈ¬ЅµµНДж·ґУ¦ЛЩВК
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБР№ШУЪµзЅвЦКИЬТєµДРрКцХэИ·µДКЗ
A. ФЪПЎCH3COOHИЬТєЦРјУИлЙЩБїCH3COONa№ММеЈ¬ґЧЛбµДЕЁ¶ИФцґуЈ¬µзАліМ¶ИјхРЎ
B. CH3COOHИЬТєУлNa2CO3ИЬТє·ґУ¦ЙъіЙCO2Ј¬їЙТФЦ¤ГчCH3COOHКЗИхЛб
C. 0.1 mol AgClєН0.1mol AgI»мєПєујУИл1 LЛ®ЦРЈ¬ЛщµГИЬТєЦРc(ClЈ) = c(IЈ)
D. КТОВПВЈ¬pH = 2µДСОЛбУлpH = 12µД°±Л®µИМе»э»мєПЈ¬ЛщµГИЬТєЦРЈєc(ClЈ)Јѕc(NH4Ј«)Јѕc(HЈ«)Јѕc(OHЈ)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї·ЦЦ¦ЛбїЙУГУЪЙъ»ЇСРѕїЎЈЖдЅб№№јтКЅИзНјЎЈПВБР№ШУЪ·ЦЦ¦ЛбµДРрКцХэИ·µДКЗ

A. ·ЦЧУЦРє¬УР2ЦЦ№ЩДЬНЕ
B. їЙУлТТґјЎўТТЛб·ґУ¦Ј¬ЗТ·ґУ¦АаРНПаН¬
C. 1mol·ЦЦ¦ЛбЧо¶аїЙУл3molNaOH·ўЙъЦРєН·ґУ¦
D. їЙК№деµДЛДВИ»ЇМјИЬТєЎўЛбРФёЯГМЛбјШИЬТєНКЙ«Ј¬ЗТФАнПаН¬
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї20ЎжК±,УГNaOHµчЅЪ0.10mol/LH2C2O4ИЬТєµДpH,јЩЙиІ»Н¬pHПВѕщУРc(H2C2O4)+c(HC2O4ЎЄ)+c(C2O42-)=0.10mol/LЎЈК№УГКэЧЦґ«ёРЖчІвµГИЬТєЦРёчє¬МјОўБЈµДОпЦКµДБїЕЁ¶ИЛжpHµД±д»ЇЗъПЯИзПВНјЎЈПВБРУР№Ш·ЦОцХэИ·µДКЗ

A. ЗъПЯaґъ±нH2C2O4ЕЁ¶ИЛжpHµД±д»Ї
B. pHґУ4µЅ6К±ЦчТЄ·ўЙъµД·ґУ¦АлЧУ·ЅіМКЅОЄ2OH-+H2C2O4====2H2O+C2O42-
C. ФЪЗъПЯaЎўcЅ»ЅзµгУР:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-)
D. µ±ИЬТєpH=7К±:c(Na+)>c(C2O42-)>c(HC2O4-)>c(H2C2O4)
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com