
【题目】碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i. CH2=CHCH3(g)+ Cl2(g)=CH2ClCHClCH3(g) △H1= -133 kJ·mol-1
ii. CH2=CHCH3(g)+Cl2(g)=CH2 =CHCH2Cl(g)+HCl(g) △H2= -100 kJ·mol-1
又已知在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g) 的正反应的活化能Ea(正)为132 kJmol-1,则逆反应的活化能Ea(逆)为________kJmol-1。
(2)查阅资料得知,反应CH3CHO(aq)=CH4(g)+CO(g)在含有少量I2的溶液中分两步进行:
第I步反应为CH3CHO(aq)+I2(aq)→CH3I(l) +HI(aq)+CO(g)(慢反应);
第II步为快反应。增大I2的浓度________(填“能”或“ 不能”)明显增大总反应的平均速率,理由为______________。
(3)用催化剂Fe3(CO)12/ZSM -5催化CO2加氢合成乙烯的反应,所得产物含CH4、C3H6、C4H8等副产物,反应过程如图。

催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表。

欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM -5中添加__________助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是__________________。
(4)在一密闭容器中,起始时向该容器中充入H2S和CH4且n(H2S):n(CH4) =2:1,发生反应:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。0. 11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
CS2(g)+4H2(g)。0. 11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:

为提高H2S的平衡转化率,除改变温度外,还可采取的措施是______________(列举一条)。N点对应温度下,该反应的Kp=______ ( MPa)2(Kp为以分压表示的平衡常数)。
(5)合成碳酸二甲酯的工作原理如下图所示。

阳极的电极反应式为_______,离子交换膜a为__________(填“阳膜”、“阴膜”)。
【答案】165 能 总反应的平均速率由慢反应决定,I2 为慢反应的反应物,增大I2的浓度,慢反应的反应速率增大,则总反应的反应速率增大(或根据总反应可知I2可为该反应的催化剂,增大I2的浓度,可以增大总反应的平均反应速率) K 降低生成乙烯的反应所需要的活化能,加快乙烯生成速率,而对其他副反应几乎无影响 减小体系压强,或及时分离出产物,或减小起始时![]() 等(任写一条) 8×10-4 2CH3OH+CO-2e-=(CH3O)2CO+2H+ 阳膜
等(任写一条) 8×10-4 2CH3OH+CO-2e-=(CH3O)2CO+2H+ 阳膜
【解析】
(1)i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) △H1= -133 kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2Cl(g)+HCl(g) △H2= -100 kJ·mol-1
根据盖斯定律,将i-ii得CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g),△H=Ea(正)-Ea(逆);
(2)第II步反应可由总反应-第I步反应得到,总反应的平均速率由慢反应决定,根据增大I2的浓度对反应速率的影响分析,或从催化剂的角度分析;
(3)由表中数据,兼顾乙烯的产率、CO2转化率和对副反应的影响,选择添加K助剂效果最好,其他副反应占比少,根本原因是降低反应的活化能、加快乙烯生成速率;
(4)根据图示,升高温度,CH4的物质的量分数减小,说明升高温度,平衡正移;为提高H2S的平衡转化率,即平衡正移,除改变温度外,还可减小体系压强、及时分离出产物、减小起始时![]() 等;N点时,n(H2S)%=n(H2)%,设起始加入甲烷物质的量为3mol,转化甲烷物质的量为xmol,列“三段式”:
等;N点时,n(H2S)%=n(H2)%,设起始加入甲烷物质的量为3mol,转化甲烷物质的量为xmol,列“三段式”:
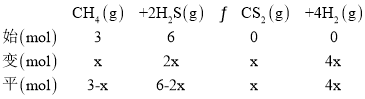
6-2x=4x,解出x,平衡常数KP= ;
;
(5)该装置为电解池,根据图示,O2在电极表面转化为H2O,氧元素的化合价降低,得电子,发生还原反应,则通入氧气的一极为阴极,电源电极B为负极,A为正极,故通入一氧化碳和甲醇的一极为阳极,阳极的电极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+,阴极的电极反应为:O2+4H++4e-=2H2O,据此分析解答。
(1)已知:i. CH2=CHCH3(g)+C12(g)=CH2ClCHClCH3(g) △H1= -133 kJ·mol-1
ii. CH2=CHCH3(g)+Cl2(g)=CH2 =CHCH2Cl(g)+HCl(g) △H2= -100 kJ·mol-1
根据盖斯定律,将i-ii得CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g) △H=-133 kJ·mol-1-(-100 kJ·mol-1)=-33 kJ·mol-1,△H=Ea(正)-Ea(逆),则逆反应的活化能Ea(逆)为132 kJmol-1+33 kJ·mol-1=165 kJ·mol-1;
(2)根据题意,第II步反应=总反应-第I步反应,则第II步反应为CH3I(l) +HI(aq)= I2(aq)+ CH4(g),总反应的平均速率由慢反应决定,I2为慢反应的反应物,增大I2的浓度,慢反应的反应速率增大,则总反应的反应速率增大(或根据总反应和两步反应可知,I2可为该反应的催化剂,增大I2的浓度,可以增大总反应的平均反应速率);
(3)由表中数据可知,添加Na助剂时其他副反应占比大,添加Cu助剂时CO2转化率低,兼顾乙烯的产率、CO2转化率和对副反应的影响,选择添加K助剂效果最好,不仅能提高单位时间内乙烯产量,并且其他副反应占比少,根本原因是降低反应的活化能、加快乙烯生成速率;
(4)根据图示,升高温度,CH4的物质的量分数减小,说明升高温度,平衡正移,正反应为吸热反应,△H>0;为提高H2S的平衡转化率,即平衡正移,除改变温度外,还可减小体系压强、及时分离出产物、减小起始时![]() 等;N点时,n(H2S)%=n(H2)%,设起始加入甲烷物质的量为3mol,转化甲烷物质的量为xmol,列“三段式”:
等;N点时,n(H2S)%=n(H2)%,设起始加入甲烷物质的量为3mol,转化甲烷物质的量为xmol,列“三段式”:
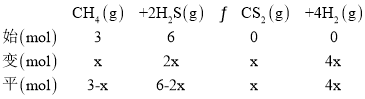
6-2x=4x,解出x=1,平衡时体系总物质的量为(2+4+1+4)mol=11mol,平衡常数KP= =
=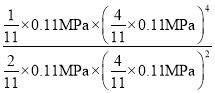 =8×10-4( MPa)2;
=8×10-4( MPa)2;
(5)该装置为电解池,根据图示,O2在电极表面转化为H2O,氧元素的化合价降低,得电子,发生还原反应,则通入氧气的一极为阴极,电源电极B为负极,A为正极,故通入一氧化碳和甲醇的一极为阳极,阳极的电极反应为2CH3OH+CO-2e-=(CH3O)2CO+2H+,阴极的电极反应为:O2+4H++4e-=2H2O,根据阴极反应,氧气和氢离子结合产生水,氢离子来自于阳极反应的产物,则H+透过交换膜向阴极移动,则离子交换膜a为阳膜。


科目:高中化学 来源: 题型:
【题目】对于可逆反应4 NH3(g)+5O2(g)![]() 4NO(g)+6 H2O(g),下列叙述正确的是
4NO(g)+6 H2O(g),下列叙述正确的是
A.NH3和H2O化学反应速率关系是2v正(NH3)= 3v正(H2O)
B.达到化学平衡时,4v正(O2)= 5v逆(NO )
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对工业生产、缓解环境污染、解决能源危机等具有重要意义。
(1)已知:①C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol
②C(s)+CO2(g)=2CO(g) △H2=+172.5kJ/mol
③4Fe(s)+3O2(g)=2Fe2O3(s) △H3=-1651.0kJ/mol
CO还原氧化铁的热化学方程式为_____________。
(2)氢硫酸、碳酸均为二元弱酸,其常温下的电离常数如下表:
H2CO3 | H2S | |
Ka1 | 4.410-7 | 1.310-7 |
Ka2 | 4.710-11 | 7.110-15 |
①煤的气化过程中产生的有害气体H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为_______;
②常温下,0.1mol·L-1 NaHCO3溶液和0.1mol·L-1 NaHS溶液的pH相比,pH较小的为________ 溶液(填化学式)。
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH (此反应在低温时为自发反应)。
①下图能表示该反应的平衡常数K与温度T之间的变化关系曲线为_____(填“a”或“b”),其判断依据是__________。
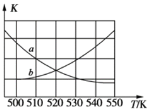
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如下图所示,则在该时间段内,恰好达到化学平衡时,此时容器内的压强与反应开始时的压强之比为_____________。
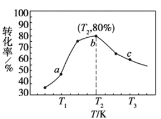
(4)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。
①NH3与NO2生成N2的反应中,当生成28g N2时,转移的电子数为____mol(结果保留三位有效数字)。
②将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置如图1)。反应相同时间NOx的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是______;当反应温度高于380 ℃时,NOx的去除率迅速下降的原因可能是____。
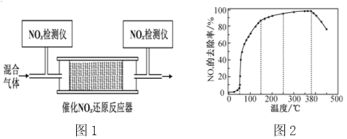
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
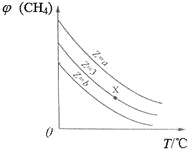
A. 该反应的焓变ΔH>0
B. 图中Z的大小为a>3>b
C. 图中X点对应的平衡混合物中![]() =3
=3
D. 温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种固定CO2的电化学装置如图,该电化学装置放电时可将CO2转化为Li2CO3和C,充电时选用合适催化剂,只有Li2CO3发生氧化反应,释放出CO2和O2。下列说法正确的是

A.放电时,Li+向电极X方向移动
B.充电时,电极Y应与外接直流电源的负极相连
C.充电时,阳极的电极反应式为C +2Li2CO3-4e- =3CO2 ↑+4Li +
D.充电时,每转移0.4mol电子,理论上阳极生成标准状况下4.48LCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量为0.10mol的镁条在只含有CO2和O2的容器中燃烧(产物不含碳酸镁,不考虑C与O2的反应),反应后容器内固体物质的质量不可能为( )
A.3.2g
B.4.0g
C.4.2g
D.4.7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)直接燃料电池具有启动快、效率高等优点,用二甲醚燃料电池电解甲基肼(CH3—NH—NH2)制氢的装置如图所示,其中X、Y、M、N均为惰性电极。下列说法正确的是( )
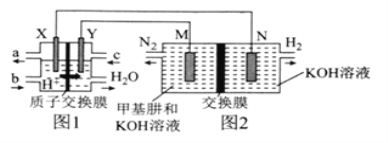
A.M极的电极反应式为CH3—NH—NH2+12OH--10e-=CO![]() +N2↑+9H2O
+N2↑+9H2O
B.图1中电解质溶液的pH减小,图2中电解质溶液的pH增大
C.图2中的交换膜是阴离子交换膜,OH-透过交换膜向N极移动
D.理论上,当生成6.72LH2时,消耗CH3OCH3的质量为2.3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。

(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______(填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________,反应的离子方程式为___________。
(4)请写出此铝热反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
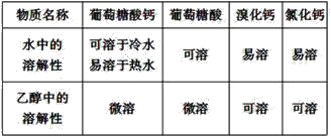
实验流程如下:
C6H12O6(aq)![]()
![]()
![]()
![]() 悬浊液
悬浊液![]()
![]()
![]() (C6H11O7)2Ca
(C6H11O7)2Ca
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最适合的是__。
A.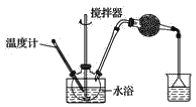
B.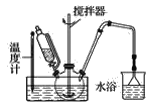
C.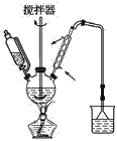
(2)制备葡萄糖酸钙的过程中,葡萄糖氧化也可用其它试剂,下列物质中最适合的是__。
A.新制氢氧化铜悬浊液
B.酸性高锰酸钾溶液
C.氧气/葡萄糖氧化酶
D.银氨溶液
(3)第②步充分反应后碳酸钙固体需有剩余,其目的是__。
(4)第②步实验中不用氯化钙替代碳酸钙的理由是__。
(5)第③步需趁热过滤的原因是__。
(6)第④步加入乙醇的作用是__。
(7)第⑥步中,下列洗涤剂最合适的是__。
A.冷水 B.热水
C.乙醇 D.乙醇-水混合溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com