
【题目】在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法正确的是( )
HCO3-+OH-。下列说法正确的是( )
A. 稀释溶液,水解平衡向逆反应方向移动,水解程度减小
B. 通入CO2,平衡向正反应方向移动
C. 升高温度,c(HCO3-)/c(CO32-)减小
D. 加入NaOH固体,溶液pH减小
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】用16mol/L 浓硫酸配制100mL 2.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题:
(1)该实验所需的玻璃仪器:______、玻璃棒、烧杯、胶头滴管、量筒。
(2)所需浓硫酸的体积是_____,量取浓硫酸所用的量筒的规格是____(规格从下列中选用A.10mL B.20mL C.50mL D.100mL)。
(3)第⑤步定容的具体实验操作是_______。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水____。
B.转移溶液前未冷却至室温_____。
C.定容时仰视溶液的凹液面______。
D. 向容量瓶中转移溶液时,不慎有少量溶液洒在容量瓶外面____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于难溶电解质溶解平衡的说法正确的是
A. 可直接根据 Ksp 的数值大小比较难溶电解质在水中的溶解度大小
B. 在 AgCl 的饱和溶液中,加入蒸馏水, Ksp(AgCl)不变
C. 难溶电解质的溶解平衡过程是可逆的,且在平衡状态时 v溶解=v沉淀=0
D. 25℃时, Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量 KI 固体,一定有黄色沉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁(![]() )广泛应用于航天、化工等领域中,其电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂),下列说法正确的是( )
)广泛应用于航天、化工等领域中,其电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂),下列说法正确的是( )
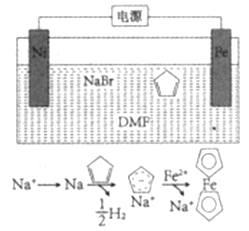
A. 该电解池的阳极反应Fe-3e-=Fe3+
B. DMF溶液可用水替代
C. 电解液中钠离子起到催化剂的作用
D. 该过程中消耗2mol环戊二烯理论上产生22.4L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是门捷列夫提出元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”。已知短周期元素W、X、Y、Z在周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。下列说法正确的是( )

A. W的氢化物与Z的氢化物反应,产物的水溶液呈碱性
B. 在元素周期表中,117号元素与Z元素位于同一主族
C. 氧化物对应水化物的酸性:Z>Y
D. W、X、Y、Z四种元素对应的单质的沸点:W<X<Y<Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. ![]() 氨水加水稀释后,溶液中所有离子的浓度都减小
氨水加水稀释后,溶液中所有离子的浓度都减小
B. 将![]() 溶液与
溶液与![]() 溶液混合可制取
溶液混合可制取![]()
C. 直接蒸干![]() 溶液就可以得到
溶液就可以得到![]() 固体
固体
D. 浓度相同的①![]() ;②
;②![]() ;③
;③![]() 。三种溶液中的
。三种溶液中的![]() :③>①>②
:③>①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于0.1 mol·L-1 Na2SO4溶液的叙述中,正确的是
A.从1 L该溶液中取出100 mL,则取出溶液中Na2SO4的物质的量浓度为 0.01 mol·L-1
B.0.5 L该溶液中钠离子的物质的量0.1 mol·L-1
C.1 L该溶液中含有Na2SO4的质量为142 g
D.取该溶液10mL,加水稀释至100 mL后Na2SO4的物质的量浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。它们的焰色实验均为黄色。
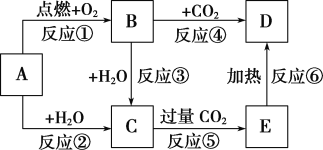
(1)写出下列物质的化学式:B________;E___________。
(2)以上6个反应中属于氧化还原反应的有________(填写编号)。
(3)写出B→C反应的离子方程式:________________________________________;
C→E的化学方程式:____________________________________________;
E→D的化学方程式:___________________________________________;
(4)加热5.00 g D和E的固体混合物,使E完全分解,固体混合物的质量减少了0.31 g,则原混合物中D的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1684 年,波义耳出版了一部名为《人血的自然史略》的医学著作,在这本书里, 他总结了自己在血液分析方面的实验成果。这是有史以来,人类第一次将化学分析方法用于 临床医学。通过实验,波义耳证明了血液中含有氯化钠,并将之称为固定盐。科研人员从海水得到的粗盐中含有泥沙等不溶性杂质,以及可溶性杂质:Ca2+,Mg2+,SO42-等,提纯的流程如下图:
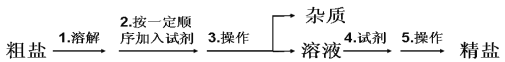
(1)整个流程中首先将粗盐溶解,再通过以下实验步骤进行提纯:①过滤②加过量 NaOH 溶 液③加适量盐酸④加过量 Na2CO3 溶液⑤加过量 BaCl2 溶液。
以下操作顺序不合理的是_____(填字母)
A.②⑤④③① B.④⑤②①③ C.⑤②④①③ D.⑤④②①③
除去 Mg2+的离子方程式_________。
(2)实验室将上述得到的精制食盐水制成精盐的过程中,还需要进行某一操作,该操作中 需要加热的仪器为:_____。
(3)下列实验仪器,可用酒精灯直接加热的是_______(填字母)
①试管 ②量筒 ③圆底烧瓶 ④烧杯 ⑤容量瓶 ⑥锥形瓶 ⑦燃烧匙
A. ①③④⑥⑦ B. ①⑦ C. ①③④⑤⑥ D. ①②③④⑤⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com