
����Ŀ�����·�ZnS��BaSO4��Ҳ��п���ף�����һ�ֳ��ð�ɫ���ϡ��ش��������⣺
��1��������ɫ��Ӧ��ԭ���ȿ���������ͷĽ����̻�����ɶ��Լ���ijЩ�����Ρ��������·���Ʒʱ��������ɫΪ__________�����ţ���
A����ɫ B����ɫ C����ɫ D����ɫ
��2�����ؾ�ʯ��BaSO4��Ϊԭ�ϣ��ɰ����¹����������·ۣ�

���ڻ�ת¯���ؾ�ʯ��������̿��ԭΪ�����������ù��̵Ļ�ѧ����ʽΪ______________________����ת¯β���к����ж����壬�����Ͽ�ͨ��ˮ�����任��Ӧ����ת��ΪCO2��һ�������Դ���壬�÷�Ӧ�Ļ�ѧ����ʽΪ______________________��
���ڳ�ʪ�����г��ڷ��õ�����ԭ���������ݳ���������ζ�����壬��ˮ���Ա���ԭ��������ԭ��������������������ˮ��___________���ѧʽ����
�۳������з�Ӧ�����ӷ���ʽΪ______________________��
��3����Ʒ��S2�ĺ���������������������á���ȡm g��Ʒ�����ڵ���ƿ�У���ȡ25.00 mL 0.1000 mol��L1��I2KI��Һ�����У�������������Һ���ܱգ��ð�����Ӧ5 min���е������������Ե�����ҺΪָʾ����������I2��0.1000 mol��L1Na2S2O3��Һ�ζ�����ӦʽΪI2+2![]() =2I+
=2I+![]() ���ⶨʱ����Na2S2O3��Һ���V mL���յ���ɫ�仯Ϊ_________________����Ʒ��S2�ĺ���Ϊ______________��д������ʽ����
���ⶨʱ����Na2S2O3��Һ���V mL���յ���ɫ�仯Ϊ_________________����Ʒ��S2�ĺ���Ϊ______________��д������ʽ����
���𰸡�D BaSO4+4C![]() BaS+4CO�� CO+H2O
BaS+4CO�� CO+H2O![]() CO2+H2 BaCO3 S2+Ba2++Zn2++
CO2+H2 BaCO3 S2+Ba2++Zn2++![]()
![]() BaS��BaSO4�� dz��ɫ����ɫ
BaS��BaSO4�� dz��ɫ����ɫ 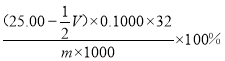
��������
��1����ɫ��Ӧ�����ڻ�ѧ�仯���������������Ԫ�ش��ڣ���������Ԫ����ɫ��
��Na����ɫ�� ���Li���Ϻ죩����K��dz�ϣ����Rb����ɫ������Ca��ש��ɫ������Sr����죩��ͭCu����ɫ������Ba�����̣����Cs���Ϻ죩��
��2�������ؾ�ʯ�뽹̿�ڻ�ת¯�з�ӦBaSO4+4C=BaS+4CO�������ɻ�ԭ��BaS������Һ������п�������ֽⷴӦS2-+Ba2++Zn2++SO42-=BaSO4+ZnS�����õ����·ۡ�
��ע�⽹̿��������CO����Ӧ��Ϊ���ᱵ�뽹̿������ΪBaS��CO��д������ʽ��CO��ˮ������Ӧ����CO2��H2��д������ʽCO+H2O=CO2+H2��
�ڸ�����Ϣ��������ζ����Ϊ�������壬��ǿ��������ԭ������ԭ�����������ˮ��������̼��Ӧ������̼�ᱵ���������壻
����������пΪ������ǿ����ʣ�д��������ʽ���������ᱵ����пΪ���������ɵ��룬д�����ӷ���ʽ��
��3���ⵥ������ۻ��Ϊ��ɫ������������Ƶζ�������I2�����յ���ɫ�仯Ϊdz��ɫ����ɫ������������ԭ��Ӧ��ʧ��������ȣ����ù�ϵʽ�����⣻
��1����ɫ��Ӧ���ǻ�ѧ�仯���������������Ԫ�ش��ڣ���������Ԫ����ɫ��
A.�Ƶ���ɫΪ��ɫ����A����
B.�Ƶ���ɫΪ��ɫ����B����
C.�ص���ɫΪ��ɫ����C����
D.������ɫΪ��ɫ����D��ȷ��
�𰸣�D��
��2����ע�⽹̿��������CO����Ӧ��Ϊ���ᱵ�뽹̿������ΪBaS��CO��д������ʽBaSO4+4C=BaS+4CO����CO��ˮ������Ӧ����CO2��H2��д������ʽ��CO+H2O=CO2+H2��
�𰸣�BaSO4+4C=BaS+4CO����CO+H2O=CO2+H2��
�ڸ�����Ϣ��������ζ����Ϊ�������壬��ǿ��������ԭ������ԭ�����������ˮ��������̼��Ӧ������̼�ᱵ���������壻
�𰸣�BaCO3��
����������пΪ������ǿ����ʣ�д��������ʽ���������ᱵ����пΪ���������ɵ��룬д�����ӷ���ʽ��S2-+Ba2++Zn2++SO42-=BaSO4+ZnS����
�𰸣�S2-+Ba2++Zn2++SO42-=BaSO4+ZnS����
��3���ⵥ���������ӵķ�Ӧ��S2-+I2=S+2I-���ⵥ������ۻ��Ϊ��ɫ������������Ƶζ�������I2�����յ���ɫ�仯Ϊdz��ɫ����ɫ������������ԭ��Ӧ��ʧ��������ȣ����ù�ϵʽ�����⣻���ݻ��ϼ���������й�ϵʽ�������������ʵ���Ϊnmol��
S2- �� I2 2S2O32- �� I2
1mol 1mol 2mol 1mol
n mol nmol 0.1V��10-3mol![]() 0.1V��10-3mol
0.1V��10-3mol
n+![]() 0.1V��10-3mol=25
0.1V��10-3mol=25![]() 0.1V��10-3mol����n=��25-
0.1V��10-3mol����n=��25-![]() V��0.1��10-3mol
V��0.1��10-3mol
����Ʒ�������Ӻ���Ϊ��![]() ��100%=
��100%= 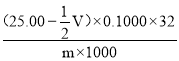 ��100%
��100%
�𰸣�dz��ɫ����ɫ��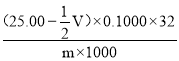 ��100%��
��100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������⣩ˮ��������֮��������������Զֵ��̽������������
(1) ���ڷ�ӦH2(g)��1/2O2(g)H2O(l)������˵������ȷ����________��
A���ʱ���H��0���ر���S��0
B�����ѷ�Ӧ��Ƴ�ԭ��أ�ʵ��������ת��
C��һ�������£����۲첻��ˮ�����ɣ�˵���������·�Ӧ�����Է�����
D��ѡ�ú��ʵĴ������п���ʹ��Ӧ�ڳ��³�ѹ���ԽϿ�����ʽ���
(2) �ٸ���H2O�ijɼ��ص㣬������ͼ��H2O����ֱ���������������(O��H��O)________��
�ڽ�һ����ˮ�����յĺ����ܱ������У��ⶨ��ͬ�¶�(T)����̬��Һ̬ˮƽ���[H2O(l)H2O(g)]ʱ��ѹǿ(p)����ͼ�л�����20�濪ʼ����100���p��T�仯��ϵʾ��ͼ(20��ʱ��ƽ��ѹǿ��p1��ʾ)________��
 ��������
��������
(3) ˮ�ڸ��¸�ѹ״̬�³���������������ʡ����¶ȡ�ѹǿ�ֱ��ٽ��¶�(374.2��)���ٽ�ѹǿ(22.1 MPa)ʱ��ˮ��Ϊ���ٽ�ˮ��
���볣�³�ѹ��ˮ��ȣ����¸�ѹҺ̬ˮ�����ӻ���������������ԭ��________��
�����ˮ�����ӻ�Kw��1.0��1014����1.0��1010������Ӧ�ĵ������ԭ����________����
�۳��ٽ�ˮ�ܹ���������������������������ܣ��ɴ˷�չ�˳��ٽ�ˮ����������һ��ʵ�������£�����Ҵ��ij��ٽ�ˮ���������ͼ��ʾ������xΪ��̼Ԫ�ؼƵ����ʵ���������tΪ��Ӧʱ�䡣
 ��������
��������
����˵����������________��
A���Ҵ��ij��ٽ�ˮ���������У�һ����̼���м���������̼�����ղ���
B����550�������£���Ӧʱ�����15 sʱ���Ҵ�����Ϊ������̼��������ȫ
C���Ҵ��ij��ٽ�ˮ���������У��Ҵ����������ʻ������̼���������ʶ�����������ʾ��Ӧ�����ʣ�����������ֵ���
D�����¶����ߣ�xCO��ֵ���ֵ�ʱ����ǰ���ҷ�ֵ���ߣ�˵���Ҵ����������ʱ�һ����̼�������ʵ��������ȸ���
(4) �Բ�������ʯī������Ƶ��أ�ͨ�����NH4HSO4��Һ����(NH4)2S2O8������ˮ��Ӧ�õ�H2O2���������ɵ�NH4HSO4����ѭ��ʹ�á�
�������ĵ缫��Ӧʽ��________��
���Ʊ�H2O2���ܷ�Ӧ����ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A������ʯ�͵���Ҫ�л�����ԭ�ϣ������ʿ�����������һ������ʯ�ͻ�����չˮƽ��E�Ǿ��й���ζ���л��F��һ�ָ߾�����Ƴɶ��ְ�װ���ϡ�

��1��F�Ľṹ��ʽΪ__________��C������Ϊ__________��
��2��ʹ1molA������������ȫ�ӳɷ�Ӧ��Ȼ��ʹ�üӳɷ�Ӧ�IJ����������ڹ��յ������·�����ȫȡ����Ӧ�����������������ĵ��������ܵ����ʵ�����_______mol��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��__________________________________________________________��
��__________________________________________________________��
��__________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��Ӧ2A(g) ![]() B(g) + D(g)�����ֲ�ͬ�������½��У�B��D��ʼŨ��Ϊ0����Ӧ��A��Ũ���淴Ӧʱ��ı仯������±���
B(g) + D(g)�����ֲ�ͬ�������½��У�B��D��ʼŨ��Ϊ0����Ӧ��A��Ũ���淴Ӧʱ��ı仯������±���
ʵ����� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
(1) | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
(2) | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
(3) | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
(4) | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
�����������ݣ�����˵���������
A. ��(1)�У���Ӧ��10~20 min��A��ƽ������Ϊ0.013 mol/(L��min)
B. ��(2)�У�A�ij�ʼŨ��c2<1.0 mol/L
C. ��(3)�ķ�Ӧ����Ϊ��3��(1)�ķ�Ӧ����Ϊ��1�����3 > ��1
D. �Ƚ�(1)��(4)�����Ʋ�÷�Ӧ������Ӧ�����ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ�����й��������ἰ�����ε�˵������ȷ����
A. Na2SO3��Һ�� NaHSO3��Һ�к��е�����������ȫ��ͬ
B. pH=3�� NaHSO3��Һϡ�ͺ���Һ�и�����Ũ�Ⱦ���С
C. H2SO3��Һ��c(H��)��c(SO32��)/c(H2SO3)��С�����ܵĴ�ʩ�Ǽ���NaHSO4����
D. ��0.1 mol/L NaHSO3��Һ��pH=2����0.1 mol/L H2SO3��Һ��c(H+)һ��С��0.11 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��̽����������(CH3COOC2H5)�ڲ�ͬ�¶ȡ���ͬŨ��NaOH��Һ�е�ˮ�����ʣ�ȡ��֧��С��ͬ���Թܣ����Թ������������̶�ֽ�����±����ж���ʵ�顣�����ֲ�ͬ�¶ȵ�ˮԡ�м�����ͬʱ���¼����������ȷ��ˮ�ⷴӦ�����ʡ�
ʵ���Լ� | �Թܢ�(55 ��) | �Թܢ�(55 ��) | �Թܢ�(55 ��) | �Թܢ�(75 ��) |
��������/mL | 1 | V1 | V2 | V3 |
1 mol/L NaOH mL | V4 | 3 | 0 | V5 |
����ˮ/mL | 0 | V6 | 5 | 2 |
��֪����ˮ�ⷴӦCH3COOC2H5 + H2O ![]() CH3COOH + C2H5OH��
CH3COOH + C2H5OH��
��CH3COOC2H5������ˮ���ܶȱ�ˮС��
��1��V4 = ____________��
��2��������˵����ȷ����____________________________��
A������ˮ��ƽ�������ƶ�
B������ϡ�����ʹƽ�������ƶ�
C������������ٸı�ʱ����Ӧֹͣ
D��c(CH3COOH) = c(C2H5OH)ʱ����Ӧ��ƽ��״̬
���ø����ʵ�Ũ�ȱ�ʾˮ��ƽ�ⳣ��Kh�������ʽΪ____________��
��3��ʵ���г��ñ���ʳ��ˮ��������ˮ��Ŀ���Ǽ�С����������ˮ�е��ܽ�ȣ���ʹʵ������ȷ��______________��ܡ����ܡ�)�ñ���Na2CO3��Һ��������ˮ��
��4��ʵ���У��Թܢ����Թܢ��е�������ٸ��죬���ܵ�ԭ����_______��(���������ķе�Ϊ77.1 ��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��������ͼװ�öԵ������Һ�����Խ���ʵ��̽��������˵������ȷ����(����)

A.�պϿ���K��������ָ�뷢��ƫת��֤�������ǵ����
B.�պϿ���K�����ձ��м���NaCl���壬����HCl��NaCl����Ӧ��������ʾ���������仯
C.�պϿ���K������Һ�м���CaCO3���壬������ʾ����������
D.�պϿ���K������Һ�м���AgNO3���壬��Ϊ������AgCl������������ʾ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ۺ���P�ĽṹƬ����ͼ��ʾ������˵������ȷ���ǣ�ͼ��![]() ��ʾ���ӳ���
��ʾ���ӳ���

A. �ۺ���P������������ˮ��
B. �ۺ���P�ĺϳɷ�ӦΪ���۷�Ӧ
C. �ۺ���P��ԭ��֮һ������������֬ˮ����
D. �ڱ���������Ҷ����ھۺϹ�����Ҳ���γ����ƾۺ���P�Ľ����ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ�������[Fe2(OH)6-2n(SO4)n]m�㷺����ˮ�ľ�������FeSO4��7H2OΪԭ�ϣ����ܽ⡢������ˮ��ۺϵȲ��裬���Ʊ��ۺ���������
��1����һ������FeSO4��7H2O����ϡ���ᣬ��Լ70 ���±߽����������һ������H2O2��Һ��������Ӧһ��ʱ�䣬�õ�����ɫ��Һ�塣H2O2����Fe2+�����ӷ���ʽΪ________��ˮ��ۺϷ�Ӧ�ᵼ����Һ��pH________��
��2���ⶨ�ۺ���������Ʒ����������������ȷ��ȡҺ̬��Ʒ3.000 g������250 mL��ƿ�У���������ϡ���ᣬ���ȣ��μ��Թ�����SnCl2��Һ��Sn2+��Fe3+��ԭΪFe2+������ַ�Ӧ��ȥ������Sn2+����5.000��102 mol��L1 K2Cr2O7��Һ�ζ����յ㣨�ζ�������![]() ��Fe2+��Ӧ����Cr3+��Fe3+��������K2Cr2O7��Һ22.00 mL��
��Fe2+��Ӧ����Cr3+��Fe3+��������K2Cr2O7��Һ22.00 mL��
������ʵ����������ȥ������Sn2+����Ʒ���������������IJⶨ�����________������ƫ��������ƫС��������Ӱ��������
�ڼ������Ʒ����������������д��������̣�_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com