
����Ŀ���ҹ��Ŵ��Ƽ�ʮ�ַ�����жԹ����Ľ��Ͳ���ȷ����
��� | ���� | ���� |
A | �վƷǹŷ�Ҳ����Ԫʱ��ʼ���䷨��Ũ�ƺ������ | �� |
B | ���� | ����������ұ��ͭ |
C | �����˲�֪���෨��Ԫʱ�ϰ��лƳ���Ϊլ���ǣ�լԫ������ȥ�����ǰף�������Ч֮ | ���ǵķ����ᴿ�����˻��������������е�ɫ�� |
D | ��ɰ��֮��ˮ���������ֳɵ�ɰ | ����ʱ��ɰ |
A.AB.BC.CD.D
 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ʵ���ҽ�������ͼ��ʾ��ʵ�飬����˵���д������

A. X��Z�ձ��з�ɢ����ͬ
B. Y�з�Ӧ���ӷ���ʽΪ3CaCO3��2Fe3����3H2O==2Fe(OH)3(����)��3CO2����3Ca2
C. ���ù��˵ķ������ɽ�Z�й�����Һ�����
D. Z�з�ɢϵ�ܲ��������ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ο�����ͼ�����й�Ҫ��ش����⣺
��1��ͼ����1molNO2(g)��1molCO(g)��Ӧ����CO2��NO�����������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��___(��������������С����������������ͬ)����H�ı仯��__����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��__��
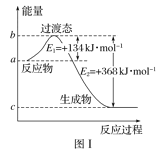
��2���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)��H2O(g)=CO2(g)��3H2(g) ��H����49.0kJ��mol��1
��CH3OH(g)��![]() O2(g)=CO2(g)��2H2(g) ��H����192.9kJ��mol��1
O2(g)=CO2(g)��2H2(g) ��H����192.9kJ��mol��1
��֪��H2O(g)=H2O(l) ��H����44kJ��mol��1
��״�ȼ������Һ̬ˮ���Ȼ�ѧ����ʽ��___��
��3���±��Dz��ֻ�ѧ���ļ������ݣ�
��ѧ�� | P��P | P��O | O=O | P=O |
����/kJ��mol��1 | a | b | c | x |
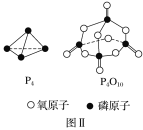
��֪1mol����(P4)��ȫȼ�շ���ΪdkJ����������ȫȼ�յIJ���ṹ��ͼ����ʾ�������x��___kJ��mol��1(�ú���a��b��c��d�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±�����Ҫ�ɷ���MgCl2�������Fe3+��Fe2+��Mn2+�����ӡ�������Ϊԭ�ϰ���ͼ��ʾ�������̽������������Ƶ���������þ��
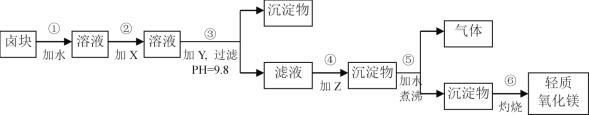
��1
���� | ��ʼ���� | ������ȫ |
Fe��OH��3 | 2.7 | 3.7 |
Fe��OH��2 | 7.6 | 9.6 |
Mn��OH��2 | 8.3 | 9.8 |
Mg��OH��2 | 9.6 | 11.1 |
�~Fe2+�����������״�����״���Һ�г�ȥ�����뽫����������Fe(OH)3������ʽ���ܳ���
��2
���� | �۸�Ԫ/�֣� |
Ư��Һ����25.2%NaClO�� | 450 |
˫��ˮ����30%H2O2�� | 2400 |
�ռ��98%NaOH�� | 2100 |
�����99.5%Na2CO3�� | 600 |
��Ҫ���Ʒ�����������ʣ����������ɱ��ϵͣ����ݱ�1�ͱ�2�ṩ�����ϣ��ش��������⣺
(1)������м�����Լ�X�����ѡ��_____________�����������ƣ�����������___________________��
(2)��������ɵij����ﺬ��____________________(�ѧʽ)��
(3)������з�����Ӧ�Ļ�ѧ����ʽΪ_____________________________��
(4)����ʵ���ҽ��в��������ʵ�飬�����õ��������������š��ƾ���ơ�________�������ǡ�
(5)��ʵ�����У�Ϊ�˳�ȥMgCl2������Һ�е�Fe3+���õ��ϴ�����MgCl2��Һ�����ڼ��Ƚ���������¼���һ���Լ������˺�������Һ�м������������ᣬ�����Լ���____________(����ĸ)��
A��NH3��H2O B��NaOH C��Na2CO3 D��MgCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ����õ�ΰ�����ɲ���ʵ�飬�ȿɽ�ԼҩƷ���ֱ��ڹ۲�ʵ������ͼ����ʾ��ʵ������������ȷ����
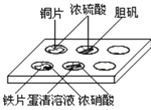
��װ��ͭƬ�Ŀ�Ѩ����Һ����ɫ
��װ�е����Ŀ�Ѩ�й������ɫ��dz
��װ����Ƭ�Ŀ�Ѩ����Һ��dz��ɫ
��װ�е�����Һ�Ŀ�Ѩ����Һ�ʻ�ɫ��
A.��B.�ڢ�C.�٢�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F��G��Ϊ������Ԫ�أ�ԭ���������ε�����AԪ��ԭ�Ӻ��������ӣ�BԪ��ԭ�������������Ǵ�����������2����D�ǵؿ��к�������Ԫ�أ�E�Ƕ������н�������ǿ��Ԫ�أ�F��Gλ�����ڣ�G��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ����û�ѧ����ش�
��1���ƶ�B��Ԫ�����ڱ��е�λ��______________��д��E2D�ĵ���ʽ__________��
��2��д��A��D�γɵ�10���������ӵĻ�ѧʽ______________��
��3��E��F��G����Ԫ�����γɵļ����ӣ��뾶�ɴ�С��˳����_______________��
��4�������£�1molA�ĵ�����D�ĵ�������ȫȼ������Һ̬ˮ���ų�286kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ________________________��
��5����Fe��Cu�Ļ�����У�����һ������C������������Ӧ��ˮ�����ϡ��Һ����ַ�Ӧ��ʣ�����m1g���������м���һ������ϡ���ᣬ��ַ�Ӧ��ʣ�����m2g������˵����ȷ����_____________��
A��m1һ������m2
B��ʣ�����m2��һ��û�е���Cu
C������ϡ����ǰ�������Һ�п϶�����Fe2+
D������ϡ����ǰ�������Һ�п϶�����Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������CO��ˮ������һ�������·�����Ӧ��ȡ������
CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H����41 kJ/mol
CO2(g)��H2(g) ��H����41 kJ/mol
ijС���о�����ͬ�¶��¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪVL���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ���ʱ��/min | ��ƽ��ʱ��ϵ�����ı仯/kJ | |||
CO | H2O | CO2 | H2 | |||
�� | 1 | 4 | 0 | 0 | t1 | �ų�������32.8 kJ |
�� | 2 | 8 | 0 | 0 | t2 | �ų�������Q |
(1)�÷�Ӧ�����У���Ӧ����ӻ�ѧ������ʱ�����յ�������_____________(����ڡ�����С�ڡ����ڡ�)��������ӻ�ѧ���γ�ʱ���ͷŵ���������
(2)�������з�Ӧ��ƽ��ʱ��CO��ת����Ϊ_____________��
(3)�����������з�Ӧ��ƽ�ⳣ��K=_____________��ijʱ�̲���������������ʵ���Ϊ1.8mol,���ʴ˿�V�� V��(����ڣ�С�ڻ����)
(4)����������ȷ����_____________(����ĸ���)��
a��ƽ��ʱ����������H2������������
b���������з�Ӧ��ƽ��״̬ʱ��Q > 65.6 kJ
c����Ӧ��ʼʱ���������з�Ӧ�Ļ�ѧ��Ӧ�������
d��ƽ��ʱ����������CO��ת������ͬ
(5)��֪��2H2(g)+O2(g)=2H2O(g)��H����484kJ/mol����д��CO��ȫȼ������CO2���Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��N��X��Y��Z��ԭ��������������Ķ���������Ԫ�ء�Y������������������������ȡ��ס��ҡ�����������������ЩԪ����ɵĻ���������ȼҵ��-�ֲ����Ϊ��Ԫ�����������0.01 mol��L�� 1����Һ��pHΪ2���������ʵ�ת����ϵ��ͼ��ʾ������˵���д������

A.ԭ�Ӱ뾶: N<Y<XB.W2N���ӵı���ģ��Ϊ![]()
C.���ʶ��к������Ӽ����ۼ�D.���ڹ�̬ʱ���ڷ��Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦCOCl2(g)![]() CO(g)��Cl2(g) ��H>0���ﵽƽ��ʱ�����д�ʩ��
CO(g)��Cl2(g) ��H>0���ﵽƽ��ʱ�����д�ʩ��
������ �ں���ͨ��������� ������COŨ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ��ǣ� ��
A.�٢ڢ�B.�٢ܢ�C.�ڢۢ�D.�ۢݢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com