
【题目】根据方程式3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,回答下列问题:
(1)用双线桥法表示电子的转移的方向及数目_______。
(2)该反应中的氧化剂是________,氧化产物是________。
(3)该反应中体现了浓硝酸的性质有________、_______。
(4)将其改为离子反应方程式_____________。
【答案】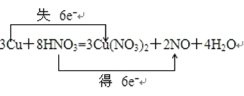 HNO3 Cu(NO3)2 酸性 氧化性 3Cu+8H++2NO3=3Cu2++2NO↑+4H2O
HNO3 Cu(NO3)2 酸性 氧化性 3Cu+8H++2NO3=3Cu2++2NO↑+4H2O
【解析】
(1)该氧化还原反应中的,化合价升高的是铜元素,化合价降低的是硝酸中的氮元素,转移电子数为6mol,双线桥法表示电子转移的方向和数目如下所示: 。
。
(2)化合价升高的是铜元素,被氧化,化合价降低的元素是氮元素,所在的反应物硝酸是氧化剂,氧化产物是Cu(NO3)2。
(3)该反应中硝酸与金属反应,体现酸性,因为是氧化还原反应,硝酸的化合价降低,所以具有氧化性。
(4)改成离子方程式为:3Cu+8H++2NO3=3Cu2++2NO↑+4H2O。
(1)该氧化还原反应中的,化合价升高的是铜元素,化合价降低的是硝酸中的氮元素,转移电子数为6mol,双线桥法表示电子转移的方向和数目如下所示: ,
,
故答案为: ;
;
(2)化合价升高的是铜元素,被氧化,化合价降低的元素是氮元素,所在的反应物硝酸是氧化剂,氧化产物是Cu(NO3)2,
故答案为HNO3,Cu(NO3)2;
(3)该反应中硝酸与金属反应,体现酸性,因为是氧化还原反应,硝酸的化合价降低,所以具有氧化性,
故答案为:酸性;氧化性;
(4)改成离子方程式为:3Cu+8H++2NO3=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3=3Cu2++2NO↑+4H2O。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
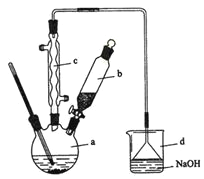
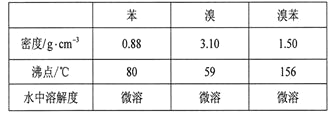
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__________气体。继续滴加至液溴滴完。装置d的作用是__________________________________________;
(2)该反应的化学方程式:__________________________________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是__________________________;
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为_______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A重结晶 B过滤 C蒸馏 D萃取
(5)在该实验中,a的容积最适合的是______(填入正确选项前的字母)。
A.25 mL B .50 mL C. 250 mL D. 509 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84g/cm3)配制100mL 1.0mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为________mL
(2)实验时选用的仪器有________
(3)配制过程中,下列情况会使配制结果偏高的是________ (填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
④量取浓硫酸时仰视量简刻度
⑤移液时未洗涤烧杯和玻璃棒
(4)在容量规使用方法中,下列操做不正确的是________ (填序号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶
D.将准确量取的18.4mol/L的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关说法正确的是
A. 60g冰醋酸晶体中,含阴离子数目为NA
B. 标准状况下,22.4LCCl4中含有分子的数目为NA
C. 常温下,46gNO2与N2O4混合气体中含分子数为NA
D. 32gCu投入300mL10mol/L的浓硝酸中,充分反应后转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H(![]() ),是一种常见的抗结肠炎药物。如图是利用芳香烃A为原料设计制备H的路线。
),是一种常见的抗结肠炎药物。如图是利用芳香烃A为原料设计制备H的路线。
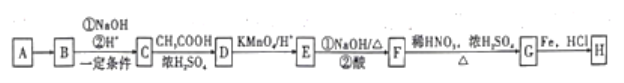
已知:①A蒸气的密度是相同条件下氢气密度的46倍;
②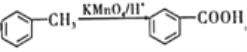 。
。
回答下列问题
(1)A的名称是_______,C中含有官能团的名称是____。
(2)写出C生成D的化学方程式:______,该反应的类型是______。
(3)G的结构简式是______。
(4)设计C→D和E→F两步反应的目的是______。
(5)化合物X是D的同分异构体,符合下列条件的X共______种。
①芳香族化合物,且苯环上有两个取代基②能发生水解反应
写出其中核磁共振氢谱显示有4种不同化学环境的氢原子,峰面积之比为3:3:2:2的所有X的结构简式:______。
(6)已知![]() 易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻、对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物
易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻、对位,而当苯环上连有羧基时则取代在间位。据此写出以A为原料制备化合物![]() 的合成路线(无机试剂任选)___________。
的合成路线(无机试剂任选)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
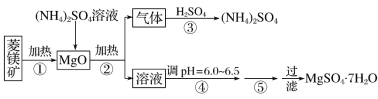
(1)步骤②中发生反应的离子方程式为__________________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是_______________________________________。
(3)步骤⑤的操作为________________________________________________________。
(4)若要除去MgSO4溶液中的FeSO4应先加________,再加入过量__________,过滤即可把杂质除尽;请用离子方程式以及文字说明除杂原理___________________________________
(5)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25 ℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____________(已知25 ℃时 ,Ksp[Mg(OH)2]=5.6×10-12 )。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中中心原子价层电子对几何构型为四面体且分子或离子空间的构型为V形的是( )
A. NH4+ B. PH3 C. H3O+ D. OF2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2+3B2 ![]() 2C的反应来说,以下化学反应速率的表示中,反应速度最慢的是
2C的反应来说,以下化学反应速率的表示中,反应速度最慢的是
A. v(B2)=0.8 mol/(L·s)B. v(B2)= 3mol/(L·min)
C. v(C)=0.6 mol/(L·s)D. v(A2)=0.4 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药用有机化合物A(C8H8O2)为一种无色液体。从A出发可发生如图所示的一系列反应。则下列说法正确的是
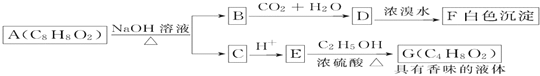
A. 根据D和浓溴水反应生成白色沉淀可推知D为三溴苯酚
B. 上述各物质中能发生水解反应的有A、B、D、G
C. G的同分异构体中属于酯且能发生银镜反应的有2种
D. 1molA能与lmolNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com