
【题目】下列指定反应的离子方程式正确的是( )
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O
B.NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
C.向FeBr2溶液中通过量的Cl2:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2
D.氯气溶于水:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。已知乙二酸晶体加热分解的方程式为:H2C2O42H2O ![]() 3H2O + CO2↑+ CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。
3H2O + CO2↑+ CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。
请回答下列问题:

(1)检验装置A气密性的方法是 。
(2)按气流方向连接各仪器,用数字表示接口的连接顺序: ①→ ;
(3)证明CO存在的实验现象是 ;
(4)本实验尾气处理的方法是 ;
(5)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),D中溶质及对应的物质的量是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 乙醇在加热的条件下,可以使黑色的氧化铜变红,生成具有特殊气味的乙醛
B. 葡萄糖在一定条件下可以水解生成乙醇和二氧化碳
C. 油脂和乙酸乙酯都属于酯类物质,碱性条件下水解都称之为皂化反应
D. 豆浆中富含大豆蛋白,煮沸后蛋白质即水解生成氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
A.78g 由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA
B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C.5.6g铁与足量盐酸反应转移的电子数为0.3NA
D.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:
①HNO2为弱酸,
②2NO+Na2O2=2NaNO2,
③2NO2+Na2O2=2NaNO3
④酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。
NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
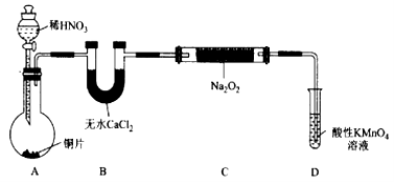
制备装置2:
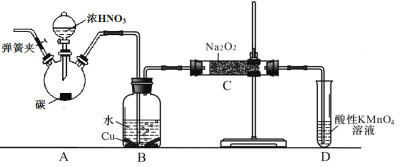
(1)在制备装置1中:
① 如果没有B装置,C中发生的副反应有 ;
② 甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了 装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为 。
(2)在制备装置2中:
① B装置的作用是 ;
② 写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移 ;
③ 为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为 ;
④ 实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸钠溶液pH>1
c.0.1mol/L亚硝酸钠溶液中存在:c(Na+)+c(H+)=c(NO2-)+c(OH-)
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2-)>c(Na+)>c(OH-)>c(H+)
⑤ 试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 溴被称为“海洋元素” B. 硅酸钠可作建筑行业的黏合剂
C. 碳酸钠可作治疗胃酸过多的药剂 D. 镁可用于制造信号和焰火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
A. 正极为Cu,负极为Fe,电解质为FeCl3溶液
B. 负极为Fe,正极为C,电解质为Fe(NO3)2溶液
C. 正极为Ag,负极为Fe,电解质为Fe2(SO4)3溶液
D. 负极为Fe,正极为Pt,电解质为Fe2(SO4)3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com