
����Ŀ���������ʯ�е�һ�֣�����Ҫ�ɷ�Ϊ��������NaAl(Si2O6)��������Cr��Ni��Mn��Mg��Fe��Ԫ�ء���ش��������⣺
(1)��̬��ԭ�ӵ���Χ�����Ų�ͼΪ___________;����ͬ���ڵĻ�̬ԭ�ӵ�M�����ȫ������Ԫ��λ�����ڱ���__________��___________����
(2)�������Ҫ�ɷֹ�������������Ԫ�ص縺����С�����˳����___________��
(3)�������γ�CrCl3��x NH3(x=3��4��5��6)��һϵ����λ��Ϊ6������
��NH3���ӵĢ�SEPRģ����___________��
�ڼ��Ǵ�С��ϵNH3___________PH3(�>��<����=��)��
��NF3������Cr3+�γ������ӣ���ԭ����___________��
(4)���Цġ��á�������ͬ�������壬����ͼ��ʾ��
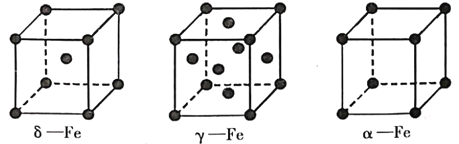
�ã�Fe�����һ�������������е���ԭ����Ϊ___________���ģ�Fe������Fe���־�������ԭ�ӵ���λ��֮��Ϊ___________����֪�ģ�Fe������ܶ�Ϊdg/cm��NA��ʾ����٤����������ֵ����Feԭ�Ӱ뾶Ϊ___________pm(�б���ʽ)
���𰸡�![]() ds p Na��Al��Si<O ������ �� F�ĵ縺�Ա�N��N��F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ�������γ���λ������NF3������Cr3+�γ������� 4 4:3
ds p Na��Al��Si<O ������ �� F�ĵ縺�Ա�N��N��F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ�������γ���λ������NF3������Cr3+�γ������� 4 4:3 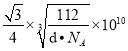
��������
(l)NiΪ28��Ԫ�أ����ݺ�������Ų�����,��̬Niԭ�ӵĵ����Ų�ʽΪ[Ar] 3d84s2�������Ų�ͼΪ![]() ������ͬ���ڵĻ�̬ԭ�ӵ�M�����ȫ������Ԫ����Zn��Ga��Ge��As��Se��Br��Kr��Znλ�����ڱ���ds����Ga��Ge��As��Se��Br��Krλ�����ڱ���p�����𰸣�
������ͬ���ڵĻ�̬ԭ�ӵ�M�����ȫ������Ԫ����Zn��Ga��Ge��As��Se��Br��Kr��Znλ�����ڱ���ds����Ga��Ge��As��Se��Br��Krλ�����ڱ���p�����𰸣�![]() ��ds��p��
��ds��p��
��2���ǽ�����Խǿ��һ������Խ��ͬһ���ڵ�Ԫ���������ҵ�һ�����ܳ��������ƣ����������к���Na��Al��Si��O����Ԫ�أ�O�ķǽ�������ǿ��Na��Al��Si��ͬ���ڣ���һ���������������Ե�һ��������С�����˳����Na��Al��Si��O����Ϊ�� Na��Al��Si��O��
��3���������γ�CrCl3��x NH3(x=3��4��5��6)��һϵ����λ��Ϊ6������
�ٰ��������е��۲���Ӷ���=��������+�µ��Ӷ���=3+1/2(5-3��1)=4,����VSEPRģ��Ϊ��������ṹ���𰸣��������塣
����N��P��ͬһ�����Ұ뾶��N��P,ԭ�Ӻ˼���������Լ���NH3��PH3���𰸣���
��NF3������Cr3+�γ������ӣ���ԭ����F�ĵ縺�Ա�N��N��F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ�������γ���λ������NF3������Cr3+�γ������ӣ��𰸣�F�ĵ縺�Ա�N��N��F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ�������γ���λ������NF3������Cr3+�γ������ӡ�
��4�������徧���������е���ԭ����Ϊ8��1/8+6��1/2=4�����������־�������ԭ�ӵ���λ���ֱ�Ϊ8��6������λ��֮��Ϊ8:6=4:3��һ������������m=M/NA=2��56/NAg������m=��V����V=2��56/NAd=2��56/dNAcm3�����ⳤΪ![]() ��������Խ����ϵ�ԭ�����ڣ���4r=
��������Խ����ϵ�ԭ�����ڣ���4r=![]() ����r=
����r=![]() =
=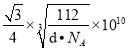 pm���𰸣�4�� 4:3 ��.
pm���𰸣�4�� 4:3 ��. 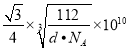



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ױ�(![]() )��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(
)��һ����Ҫ�Ļ���ԭ�ϣ���������������ȩ(![]() )��������(
)��������(![]() )�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
)�Ȳ�Ʒ���±��г����й����ʵIJ����������ʣ���ش�
���� | ��״ | �۵�(��) | �е�(��) | ����ܶ�(��ˮ��1g��cm��3) | �ܽ��� | |
ˮ | �Ҵ� | |||||
�ױ� | ��ɫҺ����ȼ�ӷ� | ��95 | 110.6 | 0.8660 | ���� | ���� |
����ȩ | ��ɫҺ�� | ��26 | 179 | 1.0440 | �� | ���� |
������ | ��ɫƬ״����״���� | 122.1 | 249 | 1.2659 | �� | ���� |
ע���ױ�������ȩ�������������ܡ�
ʵ���ҿ�����ͼװ��ģ���Ʊ�����ȩ��ʵ��ʱ��������ƿ�м���0.5g��̬�����Դ������ټ���15mL������(��Ϊ�ܼ�)��2mL�ױ�������������70�棬ͬʱ��������12mL�������⣬�ڴ��¶��½��跴Ӧ3Сʱ��
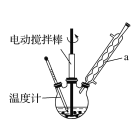
(1)װ��a��������______________��Ϊʹ��Ӧ��ϵ���ȱȽϾ��ȣ���________��
(2)����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ_______________________________________________________��
(3)д������ȩ��������Һ��һ���������·�����Ӧ�Ļ�ѧ����ʽ��________________________________��
(4)��Ӧ��Ϻ�Ӧ���Һ������Ȼ��ȴ������ʱ����Ӧ����____________��__________(���������)�Ȳ��������ܵõ�����ȩ�ֲ�Ʒ��
(5)ʵ���м���������������ҷ�Ӧʱ��ϳ�����ʹ����ȩ��Ʒ�в����϶�ı����ᡣ����ӻ��б�����ı���ȩ�з���������ᣬ��ȷ�IJ���������______________(������˳������ĸ)��
a���Ի��Һ���з�Һ b�����ˡ�ϴ�ӡ�����
c��ˮ���м����������pH��2 d����������̼��������Һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ�����������������( )
A.NaH��H2O��Ӧ����������ÿ����0.6g����ת�Ƶ�����Ϊ0.6NA
B.12gþ�ڿ����г��ȼ�գ�����ת����ĿΪNA
C.0.1 mol����NaHSO4�к�����������ĿΪ0.1NA
D.��״���£�6.72 L O2��N2�Ļ�����庬�е�ԭ����ĿΪ0.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ǹ�Ч�Ŀ�ű��ҩ��Ϊ��ɫ��״���壬�����ڱ�ͪ���ȷºͱ��У��״����Ҵ������ѡ�ʯ�����п��ܽ⣬��ˮ�м������ܣ��۵�Ϊ156-157��C�����ȶ��Բ��֪�����ѷе�Ϊ35��C����ȡ�����ص���Ҫ����Ϊ��

�����йش˹��ղ����������( )
A.�����Ŀ�����������������ѵĽӴ��������������ؽ�ȡ��
B.��������Ҫ�õ��IJ���������©�������������ձ�
C.�����������������������������صķе����ϴ�
D.���������Ҫ���̼�ˮ�ܽ⣬����Ũ������ȴ�ᾧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL NaOH��Һ����ͨ��һ������CO2��������Һ������䣩�����ȡ����Һ10mL������ϡ����100mL�������ϡ�ͺ����Һ����μ���0.1mol��L��1�����ᣬ����CO2������������״���£��������������������ϵ��ͼ�����з����������( )

A.OA����������Ӧ�����ӷ���ʽ��H++OH����H2O��CO32��+H+��HCO3��
B.NaOH������CO2��������Һ������ΪNaOH��Na2CO3�������ʵ���Ũ��֮��Ϊ1��1
C.������CO2�������״���£�Ϊ0.056 L
D.ԭNaOH��Һ�����ʵ���Ũ��Ϊ0.5 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ṹ��ʽΪ ��������������ȷ����(����)
��������������ȷ����(����)
A. 1 mol ���л����ڼ��Ⱥʹ��������£�����ܺ�4 mol H2��Ӧ
B. ���л�����ʹ��ˮ��ɫ��Ҳ��ʹ����KMnO4��Һ��ɫ
C. ���л�������������Һ������ɫ����
D. ���л�����һ���������ܷ�����ȥ��Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ΪVL�ĺ����ܱ�������ʢ��һ����H2��ͨ��Br2(g)������Ӧ��H2(g)��Br2(g)![]() 2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ����ͼ��ʾ������˵������ȷ����(����)
2HBr(g)����H��0�����¶ȷֱ�ΪT1��T2��ƽ��ʱ��H2�����������Br2(g)�����ʵ����仯��ϵ����ͼ��ʾ������˵������ȷ����(����)

A.��ͼ��֪��T1��T2
B.a��b����ķ�Ӧ���ʣ�b��a
C.Ϊ�����Br2(g)��ת���ʣ��ɲ�ȡ��HBrҺ������ʱ���ߵķ���
D.T1ʱ������Br2(g)���룬ƽ��ʱHBr�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£����淴ӦA(g)��2B(g)![]() 2C(g)�ﵽƽ��ı�־��(����)
2C(g)�ﵽƽ��ı�־��(����)
A.C������������C�ֽ���������
B.��λʱ��������nmol A��ͬʱ����2nmol B
C.��λʱ��������nmol A��ͬʱ����2nmol C
D.B������������C�ֽ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij��ҵ�������̡�

�ܽ�ȱ���
�¶��� | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
�Ȼ�� | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 65.6 | 71.3 | 77.3 |
����� | 70.6 | 73 | 75.4 | 78 | 81 | 88 | 95 | 98 | 103 |
����� | 7.4 | 9.3 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 22.9 | 24.1 |
�Ȼ��� | 28 | 31.2 | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 53.9 | 56.3 |
��1������ҵ�������̵�Ŀ���Ʒ��____________________________________����д��ѧʽ��
��2���������������ù����У���CaCO3���һ�����ʣ��ù������;��_________���Ծ�һ������
��3�������ܽ�ȱ�ת�������˵��¶���________
A��0~10�� B��20~30�� C��40~60�� D��90~100��
��������������������__________��
��4���ҹ������Ļ�ѧ��Ҳ������ת�����ķ�Ӧԭ���Ʊ���һ����Ҫ�ļ���Ʊ��Ļ�ѧ��Ӧ����ʽΪ��___________________________________________________
��5���Ȼ��ƽᾧˮ���CaCl2��6H2O��������ˮ�������Ƶó��õĸ������������ͼѡ�������ˮ�ķ�����__________

A���Ȼ��������м��ȵ�174�� B��ֱ�Ӽ�����174��
C��ֱ�Ӽ�����260�� D���Ȼ��������м��ȵ�260��
��6��������ҵ����ʵ������ɫ��ѧ���������__________________���ѧʽ��ʵ����ѭ�����ã�����Ʒ_________________________���ѧʽ����ת��Ϊԭ�ϣ��������̻���ʵ������Ⱦ�����ŷš�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com