
【题目】下图是某工业生产过程。

溶解度表:
温度℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
氯化铵 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 65.6 | 71.3 | 77.3 |
硫酸铵 | 70.6 | 73 | 75.4 | 78 | 81 | 88 | 95 | 98 | 103 |
硫酸钾 | 7.4 | 9.3 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 22.9 | 24.1 |
氯化钾 | 28 | 31.2 | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 53.9 | 56.3 |
(1)本工业生产过程的目标产品是____________________________________。(写化学式)
(2)过滤Ⅰ操作所得固体中,除CaCO3外还有一种物质,该固体的用途有_________(试举一例)。
(3)根据溶解度表转化Ⅱ适宜的温度是________
A、0~10℃ B、20~30℃ C、40~60℃ D、90~100℃
过滤Ⅱ操作所得滤渣是__________。
(4)我国著名的化学家也利用了转化Ⅱ的反应原理制备了一种重要的碱,该制备的化学反应方程式为:___________________________________________________
(5)氯化钙结晶水合物(CaCl2·6H2O)进行脱水处理可制得常用的干燥剂,根据下图选择最佳脱水的方法是__________

A、氯化氢气流中加热到174℃ B、直接加热至174℃
C、直接加热至260℃ D、氯化氢气流中加热到260℃
(6)上述工业流程实现了绿色化学的理念,其中__________________(填化学式)实现了循环利用,副产品_________________________(填化学式)可转化为原料,整个流程基本实现了污染物零排放。
【答案】 CaCl2·6H2O 做石膏模型;加入到水泥中调节水泥的硬化速率;做建筑材料 D K2SO4(或K2SO4 和KCl) NH3+H2O+NaCl+CO2=NH4Cl+NaHCO3↓ C NH3 CaCO3
【解析】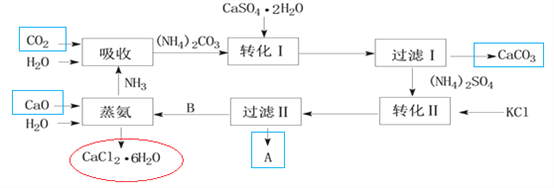
(1)根据上面流程,起点由水吸收氨气,再吸收二氧化碳,最后转化产出的为红色圈的CaCl2·6H2O,本工业生产过程的目标产品是CaCl2·6H2O;而箭头指出的CaCO3受热分解可提供氧化钙和二氧化碳,根据溶解性表中硫酸铵、氯化钾、硫酸钾和氯化铵中硫酸钾溶解度最小,在转化Ⅱ中溶解度最小的先析出,故过滤Ⅱ滤渣A为硫酸钾,即箭头指出的在流程序中间的碳酸钙和硫酸钾都不是目标产品;(2)过滤Ⅰ操作所得固体中,除CaCO3外还有一种物质,根据前面转化Ⅰ加入的石膏应该过量且是微溶,故还有的固体为石膏,用途有:做石膏模型;加入到水泥中调节水泥的硬化速率;做建筑材料等;(3)根据溶解度表转化Ⅱ适宜的温度是90~100℃,该温度范围内,硫酸铵、氯化钾、氯化铵的溶解度都比硫酸钾溶解度大得多,容易析出硫酸钾晶体;过滤Ⅱ操作所得滤渣是K2SO4(或K2SO4 和KCl);(4)我国著名的化学家也利用了转化Ⅱ的反应原理制备了一种重要的碱,该制备是在饱和食盐水中通入足量的氨气,再通入足量的二氧化碳产生碳酸氢钠,化学反应方程式为:NH3+H2O+NaCl+CO2=NH4Cl+NaHCO3↓;(5)由于CaCl2·6H2O的相对分子质量为219、假如有CaCl2·4H2O、CaCl2·2H2O、CaCl2·H2O、,则相对分子质量分别为183、147、129,CaCl2的相对分子质量为111,根据相对分子质量及质量关系,将CaCl2·6H2O转化为CaCl2最佳脱水的方法是应该选D;(6)上述工业流程(参照前面的图)实现了绿色化学的理念,其中蒸氨过程中NH3实现了循环利用,副产品CaCO3可转化为原料氧化钙和二氧化碳,整个流程基本实现了污染物零排放。


科目:高中化学 来源: 题型:
【题目】翡翠是玉石中的一种,其主要成分为硅酸铝钠NaAl(Si2O6),常含微量Cr、Ni、Mn、Mg、Fe等元素。请回答下列问题:
(1)基态镍原子的外围电子排布图为___________;与其同周期的基态原子的M层电子全充满的元素位于周期表的__________、___________区。
(2)翡翠中主要成分硅酸铝钠中四种元素电负性由小到大的顺序是___________。
(3)铬可以形成CrCl3·x NH3(x=3、4、5、6)等一系列配位数为6的配合物。
①NH3分子的ⅤSEPR模型是___________。
②键角大小关系NH3___________PH3(填“>”<”或“=”)。
③NF3不易与Cr3+形成配离子,其原因是___________。
(4)铁有δ、γ、α三种同素异形体,如下图所示。
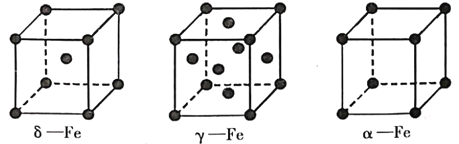
γ-Fe晶体的一个晶胞中所含有的铁原子数为___________,δ-Fe、α-Fe两种晶胞中铁原子的配位数之比为___________。已知δ-Fe晶体的密度为dg/cm,NA表示阿伏伽德罗常数的数值,则Fe原子半径为___________pm(列表达式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构简式可以用“键线式”表示,其中线表示键,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。已知利用某些有机物之间的转化可贮存太阳能,如降冰片二烯(NBD)经太阳光照射转化成四环烷(Q)的反应为 (反应吸热),下列叙述中错误的是( )
(反应吸热),下列叙述中错误的是( )
A. NBD和Q互为同分异构体
B. Q可使溴水褪色
C. Q的一氯代物只有3种
D. NBD的同分异构体可以是芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是
A. 实验I、II、III中均涉及Fe3+被还原
B. 对比实验I、II说明白色沉淀的产生与铜粉的量有关
C. 实验II、III中加入蒸馏水后c(Cu2+)相同
D. 向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种综合处理SO2废气的工艺流程,若每步都完全反应。下列说法正确的是 ( )

A.溶液B中发生的反应为2SO2+O2=2SO3
B.可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
C.由以上流程可推知氧化性:Fe3+>O2>SO42—
D.此工艺的优点之一是物质能循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A.标准状况下,22.4L CCl4含有的分子数为1NA
B.通常状况下,NA个CO2分子占有的体积为22.4L
C.常温常压下,1.06g Na2CO3溶于水,溶液中含Na+离子数为0.02NA
D.浓度为0.5mol/L的MgCl2溶液中,含有Cl数为NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酿酒和造醋是古代劳动人民的智慧结晶,白酒和醋也是日常生活中常见的有机物。
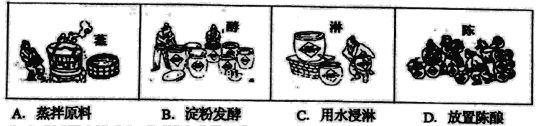
(1)上述以高粱为主要原料的酿醋工艺中,利用醋酸溶解性的是_________(填选项)。
(2)写出乙酸在水溶液中的电离平衡常数的表达式________。
(3)已知25℃下,CH3COOH在水中电离的电离常数Ka=2×10-5,则25℃时CH5COONa水解平衡常数Kh=_________(填数值)。
(4)近年来,研究者利用乙酸开发出新工艺合成乙酸乙酯,使产品成本明显降低,其主要反应为: CH2=CH2 (g)+CH3COOH(l) ![]() CH3COOC2H5(l)。
CH3COOC2H5(l)。
①该反应属于有机反应类型中的___________。
②下列描述能说明乙烯与乙酸合成乙酸乙酯的反应已达化学平衡的是_________(填选项)。
A 乙烯、乙酸、乙酸乙酯的浓度相同
B 酯化合成反应的速率与酯分解反应的速率相等
C 乙烯断开l mol碳碳双键的同时乙酸恰好消耗l mol
D 体系中乙酸的百分含量一定
(5)下图为n(乙烯)与n(乙酸)物料比为1时,在不同压强下进行了乙酸乙酯的产率随温度变化的测定实验,在相同时间点的实验结果如图所示。回答下列问题:
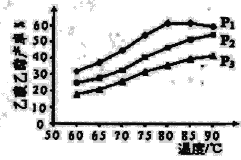
①温度在60-80℃范围内,乙烯与乙酸酯化合成反应速率由大到小的顺序是_______[用v(P1)、v(P2)、v(P3)分别表示不同压强下的反应速率]。
②压强为P1 MPa、温度60℃时,若乙酸乙酯的产率为30%,则此时乙烯的转化率为_______。
③压强为P1 MPa、温度超过80℃时,乙酸乙酯产率下降的原因可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化铬可用作毛织品防蛀剂、卤化催化剂、大理石硬化及着色剂。以铬云母矿石(含4.5%Cr2O3,还含Fe2O3、FeO、MgO、SiO2)为原料制备氟化铬的工艺流程如下。
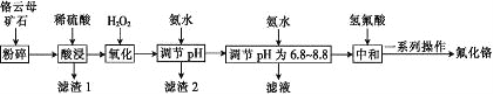
下表列出了相关金属离子生成氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 | Fe(OH)2 |
开始沉淀的pH | 2.3 | 8.8 | 4.9 | 7.5 |
沉淀完全的pH | 4.1 | 10.4 | 6.8 | 9.7 |
请回答下列问题:
(1)将铬云母矿石粉碎的目的是___________。
(2)Cr2O3与稀硫酸反应的化学方程式为________________。
(3)第一次滴加氨水调节pH范围为______。
(4)第二次滴加氨水调节pH 为6.8~8.8的目的是___________,Cr(OH)3与 Al(OH)3 一样具有两性,若第二次滴加的氨水改为NaOH溶液,生成的Cr(OH)3会部分溶解,写出Cr(OH)3溶解的离子方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 (15分)研究证明,高铁酸钾不仅能在饮用水源和废水处理过程中去除污染物,而且不产生任何诱变致癌的产物,具有高度的安全性。湿法制备高铁酸钾是目前最成熟的方法,实验步骤如下:
A.直接用天平称取60.5gFe(NO3)3·9H2O、30.0gNaOH、17.1gKOH。
B.在冰冷却的环境中向NaClO溶液中加入固体NaOH并搅拌,又想其中缓慢少量分批加入Fe(NO3)3·9H2O,并不断搅拌。C.水浴温度控制在20℃,用电磁加热搅拌器搅拌1.5h左右,溶液成紫红色时,即表明有Na2FeO4生成。
D.在继续充分搅拌的情况下,向上述的反应液中加入固体NaOH至饱和。
e.将固体KOH加入到上述溶液中至饱和。保持温度在20℃,并不停的搅拌15min,可见到烧杯壁有黑色沉淀物生成,即K2FeO4.
(1)①步骤b中不断搅拌的目的是_______。②步骤c中发生反应的离子方程式为______。③由以上信息可知:高铁酸钾的溶解度比高铁酸钠_______(填“大”或“小”)。
(2) 高铁酸钾是一种理想的水处理剂,与水反应生成O2、Fe(OH)3(胶体)和KOH。① 该反应的离子方程式为______。②高铁酸钾作为水处理剂发挥的作用是_______。③ 在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用_______。
A.H2O B.稀KOH溶液、异丙醇 C.NH4Cl溶液、异丙醇 D.Fe(NO3)3溶液、异丙醇
(3) 高铁酸钠还可以用电解法制得,其原理可表示为Fe+2NaOH+2H2O![]() 3H2↑+Na2FeO4,则阳极材料是____,电解液为______。
3H2↑+Na2FeO4,则阳极材料是____,电解液为______。
(4)25℃时,Ksp(CaFeO4)=4.536×10-9,若要使100mL1.0×10-3mol/L的K2FeO4溶液中的c(FeO42-)完全沉淀,理论上要加入Ca(OH)2的物质的量为_____mol。
(5)干法制备高铁酸钾的方法是Fe2O3、KNO3、KOH混合加热共熔生成黑色高铁酸钾和KNO2等产物。则该方法中氧化剂与还原剂的物质的量之比为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com