
| A�� | ����ȼ�ϵ�������Խ����е�������Ӧʽ��O2+4H++4e-�T2H2O | |
| B�� | ��������������̼����������ⱥ���Ȼ�����Һ�����ӷ���ʽΪ��2C1-+2H2O$\frac{\underline{\;���\;}}{\;}$H2��+Cl2��+2OH- | |
| C�� | ��ͭ����ʱ�����Դ�����������Ǵ�ͭ���缫��ӦʽΪ��Cuһ2e-=Cu2+ | |
| D�� | ��ӦHCl��aq��+NaOH��aq���TNaCl��aq��+H2O��l����H��0�������������������ԭ��� |
���� A������ȼ�ϵ���������ŵ��һ�����������������Һ�е������ӻ�μӷ�Ӧ��
B�����������ǻ��Ե缫��μӷ�Ӧ����Һ�е������Ӳ���ʧ���ӣ�
C����ͭ����ʱ�������Ǵ�ͭ����ͭ��������
D���Է����е�������ԭ��Ӧ����Ƴ�ԭ��أ�
��� �⣺A������ȼ�ϵ���У����������õ������������ӷ�Ӧ����ˮ�������ĵ缫��ӦΪO2+4H++4e-�T2H2O����A��ȷ��
B����������������̼����������ⱥ���Ȼ�����Һ�����Ե缫���μӷ�Ӧ��������ӦΪFe-2e-=Fe2+��������ӦΪ2H2O+2e-=2OH-+H2�����ܷ�ӦΪFe+2H2O$\frac{\underline{\;���\;}}{\;}$Fe��OH��2+H2����B����
C����ͭ����ʱ���������͵�Դ�ĸ����������Ǵ�ͭ����ͭ���������͵�Դ����������������C����
D��HCl��NaOH���кͷ�Ӧ���ڸ��ֽⷴӦ������������ԭ��Ӧ�������������ԭ��أ���D����
��ѡA��
���� ���⿼��ԭ��غ͵��صĹ���ԭ�����ѶȲ�����ȷ���ԭ����ԭ��ع���ԭ��Ϊ���ؼ���ע�������ǻ��Ե缫ʱ�ķ�Ӧ��B�״�������������ѧ���ķ������������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ�뺤��ʹ�ܱ�������ѹǿ����ƽ��������Ӧ�����ƶ� | |
| B�� | ����X�����ʵ��������������ܶȼ�С | |
| C�� | X������Ӧ������Y���淴Ӧ���ʵ�$\frac{m}{n}$�� | |
| D�� | �����¶ȣ���������ƽ����Է����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ù��Ϊ10mL����Ͳ��ȡ6.20mL��Һ�� | |
| B�� | �����������ƹ��������ʱ���������������ֽ�ϣ�������������ƽ�����̣��������������ƽ������ | |
| C�� | ��������ɳ�ȥҺ̬������зе㲻ͬ���ӷ����ѻӷ��ӷ������� | |
| D�� | �����Ȼ�̼��ȡ��ˮ�еĵ⣬��־��ú��Ϻ�ɫҺ�����ϲ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
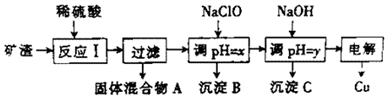
| ������ | Cu��OH��2 | Al��OH��3 | Fe��OH��3 | Fe��OH��2 |
| ��ʼ����pH | 5.4 | 4.0 | 2.2 | 5.8 |
| �������pH | 6.7 | 5.2 | 3.2 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
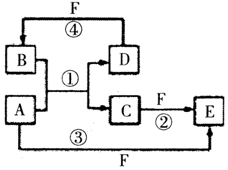 A��B��C��D��E��F�������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ���������ش��������⣺
A��B��C��D��E��F�������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ���������ش��������⣺ ����Ӧ�ܵĻ�ѧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4NO2��+2H2O��
����Ӧ�ܵĻ�ѧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2+4NO2��+2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{14}$ | B�� | 14 | C�� | $\frac{1}{49}$ | D�� | 49 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
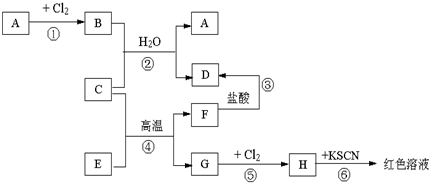
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
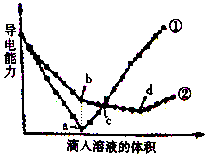 ��������ͬ��Ba��OH��2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ��
��������ͬ��Ba��OH��2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com