
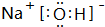 ,故答案为:
,故答案为: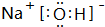 ;
;

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:
某温度下的溶液中c(H+)=1.0×10 x mol/L,c(OH-)=1.0×10 y mol/L.x与y的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合物BmAm分子中所有原子一定共平面 |
| B、一定条件下,元素C、D、E的最高价氧化物对应的水化物之间能发生反应 |
| C、工业上常用电解法制备元素C、D、E的单质 |
| D、化合物BAn与BEn具有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| 浓H2SO4,浓HNO3 |
| △ |
| Br2,Fe |
| 反应Ⅰ |
| 试剂X |
| 反应Ⅱ |
| NaOH溶液 |
| △ |
| Fe,HCl,H2O |
| 反应Ⅲ |
| 试剂Y |

 :
:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题:
A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该复合材料属于新型有机非金属材料 |
| B、Al、K、Ti都属于主族元素 |
| C、原子半径:K>Si>O |
| D、该复合材料能耐强酸和强碱腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com