
【题目】某小组模拟工业上回收分银渣中的银,过程如下:
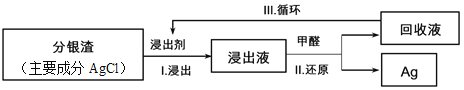
(1)Na2SO3溶液和氨水均可作浸出剂,但由于氨水易______(填物理性质),故用Na2SO3溶液更环保。
(2)Ⅰ中主要反应:AgCl + 2![]()
![]()
![]() + Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
+ Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
(3)研究发现:浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如下图。
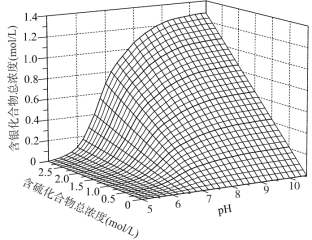
①pH=10时,含银化合物总浓度随含硫化合物总浓度的变化趋势是______。
②解释①中变化趋势的原因:______。
③pH=5时,含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,原因是___。
(4)将Ⅱ中反应的离子方程式补充完整:
□__![]() +□___OH- +□______ = □______ +□______ +□______ + CO32-
+□___OH- +□______ = □______ +□______ +□______ + CO32-
(5)Ⅲ中回收液可直接循环使用,但循环多次后,银的浸出率会降低。从回收液离子浓度变化和反应限度的角度分析原因:______。
【答案】挥发 2![]() 含银化合物总浓度随含硫化合物总浓度的增大而增大 浸出液中c(
含银化合物总浓度随含硫化合物总浓度的增大而增大 浸出液中c(![]() )增大,使浸出反应的平衡正向移动 pH较小时,
)增大,使浸出反应的平衡正向移动 pH较小时,![]() 与H+结合生成
与H+结合生成![]() 或H2SO3,尽管含硫化合物总浓度增大,但c(
或H2SO3,尽管含硫化合物总浓度增大,但c(![]() )均较小 4 6 HCHO 4Ag 8
)均较小 4 6 HCHO 4Ag 8![]() 4H2O 随着循环次数增加,浸出液中c(
4H2O 随着循环次数增加,浸出液中c(![]() )减小、c(Cl-)增大,均使AgCl + 2
)减小、c(Cl-)增大,均使AgCl + 2![]()
![]()
![]() + Cl-的限度减小
+ Cl-的限度减小
【解析】
分银渣中主要成分是AgCl,Ⅰ中用Na2SO3溶液作浸出剂,主要反应:AgCl + 2![]()
![]()
![]() + Cl-;浸出液与甲醛反应,Ⅱ中发生4
+ Cl-;浸出液与甲醛反应,Ⅱ中发生4![]() +6OH-+HCHO=4Ag+8
+6OH-+HCHO=4Ag+8![]() +4H2O+
+4H2O+![]() 反应,生成Ag回收,同时又生成
反应,生成Ag回收,同时又生成![]() ,III中循环使用。
,III中循环使用。
(1)氨水易挥发污染空气,故用Na2SO3溶液更环保;
(2)反应在敞口容器中进行,![]() 很容易被空气中氧气氧化,离子反应方程式为2
很容易被空气中氧气氧化,离子反应方程式为2![]() ;
;
(3)①根据图像可知,当pH=10时,含银化合物总浓度随含硫化合物总浓度的增大而增大;
②①中变化趋势的原因:浸出液中c(![]() )增大,使浸出反应AgCl + 2
)增大,使浸出反应AgCl + 2![]()
![]()
![]() + Cl-的平衡正向移动;
+ Cl-的平衡正向移动;
③ pH=5时,含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,pH较小时,![]() 与H+结合生成
与H+结合生成![]() 或H2SO3,尽管含硫化合物总浓度增大,但c(
或H2SO3,尽管含硫化合物总浓度增大,但c(![]() )均较小;
)均较小;
(4)Ag的化合价由+1价降至0价,HCHO被氧化成CO32-,回收液循环使用,说明有SO32-生成,根据得失电子守恒、电荷守恒和原子守恒配平得:4![]() +6OH-+HCHO=4Ag+8
+6OH-+HCHO=4Ag+8![]() +4H2O+
+4H2O+![]()
(5)随着循环次数增加,浸出液中c(![]() )减小、c(Cl-)增大,均使AgCl + 2
)减小、c(Cl-)增大,均使AgCl + 2![]()
![]()
![]() + Cl-的限度减小
+ Cl-的限度减小


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
A.给溶液加热,Ca(OH)2的溶解度减小
B.向溶液中加入少量CaO充分反应后,恢复到原温度,溶液的pH升高
C.温度不变,向溶液中加入少量Na2CO3固体,充分反应后,Ksp[Ca(OH)2]不变
D.向溶液中加入少量的NaOH固体,Ca(OH)2固体增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g) ![]() S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示,下列说法正确的是
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示,下列说法正确的是
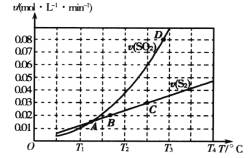
A. 该反应的H>0B. C点时达到平衡状态
C. 增加C的量能够增大SO2的转化率D. T3时增大压强,能增大活化分子百分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容中进行2SO2(g)+ O2(g)![]() 2SO3(g) ΔH < 0 。下列图像及对图像的分析均正确的是
2SO3(g) ΔH < 0 。下列图像及对图像的分析均正确的是
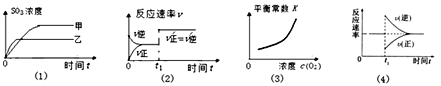
A. 只改变温度时,(1)中甲的温度比乙的温度高
B. (2)表示起始时只加反应物达平衡,在t1时刻使用催化剂对平衡的影响
C. (3)表示容积不变增加氧气的浓度,平衡右移,平衡常数增大
D. 容积可变时,在t1时刻向达平衡的上述反应加入SO3可用图像(4)描述
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量):

根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:ΔH>0,p2>p1B.反应Ⅱ:ΔH>0,T1>T2
C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1D.反应Ⅳ:ΔH<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲池的总反应式为:N2H4+O2=N2+H2O,下列关于该电池工作时的说法正确的是( )
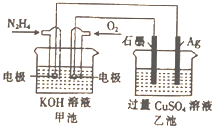
A. 该装置工作时,Ag电极上有气体生成
B. 甲池中负极反应为N2H4-4e-=N2+4H+
C. 甲池和乙池中的溶液的pH均减小
D. 当甲池中消耗0.1molN2H4时,乙池中理论上最多产生6.4g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2(g)+3H2(g)![]() 2NH3 (g) △H<0,在某一时间段中反应速率与反应过程的曲线关系如图,t1、t3、t4时刻外界条件有所改变。下列说法正确的是( )
2NH3 (g) △H<0,在某一时间段中反应速率与反应过程的曲线关系如图,t1、t3、t4时刻外界条件有所改变。下列说法正确的是( )

A. t5~t6时氨气的体积分数最大 B. t3时升高了温度
C. t1时加入催化剂 D. t4时减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________(填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为![]() 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其离子方程式为________。
,其离子方程式为________。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示。下列说法不正确的是

A.电流从右侧电极经过负载后流向左侧电极
B.A电极上发生氧化反应,B为正极
C.电极A极反应式为2NH3-6e-=N2+6H+
D.当有2.24LNO2(标准状况) 被处理时,转移电子为0.4mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com