
【题目】最近,科学家研发了“全氢电池”,其工作原理如图所示。下列说法正确的是

A. 吸附层(a)上的电势比吸附层(b)上的高
B. 负极反应为H2+2e-+2OH-=2H2O
C. 该装置将酸碱中和反应的热能转化为电能
D. 电解质溶液中ClO4-由左往右迁移
【答案】C
【解析】
由电子流向可知,左边吸附层为负极,发生了氧化反应,电极反应是H2-2e-+2OH-=2H2O,右边吸附层为正极,发生了还原反应,电极反应是2H++2e-=H2,结合原电池中阳离子移向正极,阴离子移向负极解答该题。
A.由电子流向可知,左边吸附层为负极,发生了氧化反应,右边吸附层为正极,发生了还原反应,电子总是由电势低的区域向电势高的区域移动,故吸附层(a)上的电势比吸附层(b)上的低,A错误;
B.由电子流向可知,左边吸附层为负极,发生了氧化反应,电极反应是H2-2e-+2OH-=2H2O,B错误;
C.负极电极反应是H2-2e-+2OH-=2H2O,正极电极反应是2H++2e-=H2,电池的总反应为H++OH-=H2O,该反应是放热反应,但反应过程中有电流产生,所以该装置将酸碱中和反应的热能转化为电能,C正确;
D.原电池中阳离子移向正极,阴离子移向负极。若为阳离子交换膜,则电解质溶液中Na+向右移动;若为阴离子交换膜,则ClO4-向左边移动,D错误;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)反应需要在闪电或极高温条件下发生,说明该反应_________。(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)![]() 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:
温度/℃ | 1538 | 1760 | 2404 |
平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
①该反应的△H______0。(填“>”、“=”或“<”)
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如图所示,请 补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。________________

(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g)![]() 2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)_____________
2NO(g)达到平衡时NO的浓度和O2的转化率。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯(C3H6)是重要的有机化工原料。丙烷直接脱氢制丙烯发生的主要反应及能量变化如图:

回答下列问题:
(1)丙烷直接脱氢制丙烯为强吸热过程,该反应必须在高温下进行,但温度越高副反应进行程度越大,同时还会降低催化剂的活性和选择性。
①为提供反应所需热量,恒压时若向原料气中掺入水蒸气,则K(主反应)___(填“增大”、“减小”或“不变”)。
②温度升高,副反应更容易发生的主要原因是_______。
(2)如图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强p1、p2分别为1×104 Pa和1×105 Pa)。

①1×104 Pa时,如图中表示丙烯的曲线是____(填“ⅰ”、“ⅱ”、“ⅲ”或“ⅳ”)。
②1×105Pa、500℃时,若只发生上述主反应和副反应,则达平衡时,丙烷转化为丙烯的转化率为____。
(3)为克服丙烷直接脱氢法的缺点,科学家探索出在无机膜反应器中进行丙烷脱氢制丙烯的技术。在膜反应器中,利用特定功能膜将生成的氢气从反应区一侧有选择性地及时移走。与丙烷直接脱氢法相比,该方法的优点是__________。
(4)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图。

已知:CO和H2的燃烧热分别为△H =-283.0kJ/mol、△H =-285.8kJ/mol。
①反应(ⅰ)的化学方程式为_____。
②25℃时,该工艺总反应的热化学方程式为________。
③该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名的获得诺贝尔奖的狄尔斯—阿德尔反应,是由共轭双烯与烯烃或炔烃反应生成六元环的反应。如:
 (可表示为
(可表示为![]() ),实际是个加成反应。
),实际是个加成反应。
工业上常用下列流程制取重要化学原料![]() (M)。
(M)。

流程中的A为天然橡胶的单体,分子式为C5H8。
(1)A的名称是______,B的结构简式是______。
(2)A的属于炔烃的同分异构体一共有____种,A与B反应生成的另一种含六元环的化合物的结构简式为________。
(3)②反应的类型为_____,③反应的化学方程式为:________。
(4)按下列要求写出B的两种同分异构体的结构简式:__________。
(Ⅰ)能发生银镜反应;(Ⅱ)分子结构中含有两个甲基;(Ⅲ)能发生水解反应
(5)由丙烯制得B经如下流程:

参照流程中的前两步和最后一步的书写方法写出其他中间步骤的流程:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g)![]() 2NO(g)+O2(g)在恒容密闭容器中反应,达到平衡状态的标志是①单位时间内生成n molO2 的同时消耗 2n mol NO;②单位时间内消耗2n molNO2的同时生成n molO2;③混合气体的颜色不再改变的状态;④2v(NO2)正= v(O2)逆;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体的密度不再改变的状态
2NO(g)+O2(g)在恒容密闭容器中反应,达到平衡状态的标志是①单位时间内生成n molO2 的同时消耗 2n mol NO;②单位时间内消耗2n molNO2的同时生成n molO2;③混合气体的颜色不再改变的状态;④2v(NO2)正= v(O2)逆;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体的密度不再改变的状态
A. ①③⑤ B. ②④⑥ C. ①③④⑤ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种用途广泛的无机化工原料,一种以氧化铜矿(CuO,含有Fe2O3、Al2O3、SiO2杂质)为原料制备Cu2O的流程如图所示:

已知氨浸过程中仅发生的反应为:CuO+4NH3·H2O= [Cu(NH3)4]2++2OH-+3H2O
回答下列问题:
(1)氨浸之前需将矿物粉碎、过筛,目的是_______________________________。
(2)氨浸时的温度一般不超过30℃,主要原因是__________________。按此工艺,能否用NaOH溶液代替氨水?__________________(填“能”或“否”)。
(3)蒸馏过程中会生成一种黑色固体,则此过程中发生反应的化学方程式为____________。
(4)电解过程中阳极的电极反应式为_________________。
(5)Cu(OH)2也可与NH3·H2O反应,已知常温下:
Cu(OH)2(s)+4NH3·H2O(aq)![]() [Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
[Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
Cu2+(aq)+4NH3·H2O(aq)![]() [Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
[Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
则常温下Ksp[Cu(OH)2]=________________。
(6)为了尽量减少流程中所用原料的种类,还原过程可用气体A代替气体B,在加热条件下生成两种单质,该反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s) ![]() 2CO(g),达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g),达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

A. 平衡常数:K(Ⅰ) > K (Ⅱ)
B. 在T1K时,在1.0L恒容容器中加入足量碳粉、0.09molCO2、0.05molCO,此时υ正 >υ逆
C. 体系的总压强p:p(Ⅱ) >2p(Ⅰ)
D. 正反应速率:υ正(Ⅰ) >υ正(Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示人体细胞内化学元素所形成的化合物(①~④表示化合物),下列相关说法错误的是( )
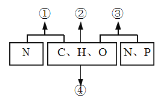
A. ①可以表示蛋白质
B. ②可以表示“生命的燃料”——葡萄糖
C. ③表示的小分子物质可能是核苷酸
D. ④是细胞膜重要的组成成分,可以表示磷脂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:Ca(ClO)2 + 4HCl(浓)= CaCl2 + 2Cl2↑+ 2H2O
(1)浓盐酸在反应中显示出来的性质是 ________(填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3molCl2,则转移的电子的物质的量为 ___________;
(3)该反应中氧化产物与还原产物的质量比为____________;
(4)用双线桥法表示该氧化还原反应中电子转移的方向和数目______
(5)铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:
①Tl3++2Ag=Tl++2Ag+,②Ag++Fe2+=Ag+Fe3+,③Fe+2Fe3+=3Fe2+,下列离子氧化性比较顺序正确的是__________ (填写字母)
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+ C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com