
����Ŀ��Ϊ��֤�����ԣ�Cl2��Fe3����SO2��ijС������ͼ��ʾװ�ý���ʵ��(�г�������A�еļ���װ�����ԣ��������Ѿ��������)ʵ�������ͼ��
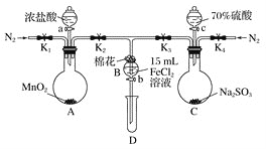
��.���ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�ε��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��
��.����a���μ�һ������Ũ���ᣬ��A���ȡ�
��.��B����Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��.����b��ʹԼ2 mL����Һ����D�Թ��У��������е������ӡ�
��.���ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
��.�����Թ�D���ظ����̢�������B��Һ�е����ӡ�
(1)���̢��Ŀ����________________________��
(2)���н������ҺΪ__________________��������_______________________��
(3)A�з�����Ӧ�Ļ�ѧ����ʽ��______________________________________��
(4)���²��������Һ��Ƶ����ӷ�Ӧ��______________________________����______________(д�Լ���ѧʽ)�����������������___________________________��
(5)��˵��������Fe3����SO2�����ӷ���ʽ��__________________________��
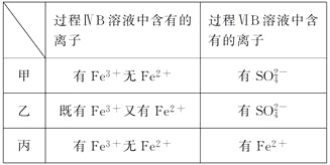
(6)�ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤��������Cl2��Fe3����SO2����________________(��ס����ҡ�����)��
���𰸡� �ų�װ���е����� ����������Һ ����Cl2��SO2����ֹ��Ⱦ���� MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O 2Fe2����Cl2===2Fe3����2Cl���� KSCN�� ��Һ��� 2Fe3����SO2��2H2O===2Fe2����SO
MnCl2��Cl2����2H2O 2Fe2����Cl2===2Fe3����2Cl���� KSCN�� ��Һ��� 2Fe3����SO2��2H2O===2Fe2����SO![]() ��4H�� �ұ�
��4H�� �ұ�
����������1������װ���к��п����ܸ���ʵ���жϣ�
��2�����������Ͷ�����������Ⱦ����������
��3������Aװ���Ʊ��������
��4�����������������������ӷ�����
��5�������������ܰѶ�����������Ϊ���������
��6��������������������ǿ����������������Է����жϡ�
��1�����ɼ�K1��K4��ͨ��һ��ʱ��N2��Ŀ�����ų�װ���е���������ֹ����ʵ�顣
��2�����н����Ϊ����������Һ�����ܹ����շ�Ӧ�ж���������������������壬��ֹ��Ⱦ������
��3��A��Ϊ����������Ũ������ȷ�Ӧ�����������Ȼ��̺�ˮ����Ӧ�Ļ�ѧ����ʽΪMnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
��4����������ǿ�����ԣ��ܹ����Ȼ���������Ϊ�Ȼ�����������������Һ�Ի�ɫ�����ӷ�Ӧ����ʽ�ǣ�2Fe2++Cl2=2Fe3++2Cl-�����������к��������ӣ����������軯����Һ���м��飬�����Һ��ΪѪ��ɫ��֤�������������ɣ�
��5��Fe3+�������������ܰѶ�����������Ϊ��������ӣ�������ԭΪFe2+������˵��������Fe3+��SO2����Ӧ�����ӷ���ʽΪ2Fe3++SO2+2H2O=2Fe2++4H++SO42-��
��6�����е�һ����Fe3+��Fe2+�������������Դ��������ӣ����еڶ��κ���SO42���������ǹ����������Ѷ�����������ΪSO42������һ����Fe3+�Ѷ��������������£��״������е�һ�μ���Fe3+����Fe2+��˵���������㣬���������Դ��������ӣ����еڶ��κ���SO42����˵�������˶��������������ӵķ�Ӧ�������������Ӵ��ڶ���������˿���֤��������Cl2��Fe3+��SO2������ȷ�����е�һ����Fe3+��Fe2+�������������Դ��������ӣ��ڶ�����Fe2+��˵�������˶��������������ӵķ�Ӧ���������������Ӵ��ڶ���������˿���֤��������Cl2��Fe3+��SO2������ȷ����ѡ�ҡ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ӣ�������Һ�д�����������Һ��������( )
A.Mg2+ ��H+ ��Cu2+ ��SO42-B.Ba2+ ��NO3- ��OH- ��CO32--
C.Ag+ ��H+ ��Cl- ��NO3-D.K+ ��H+ ��Cl- ��CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����շ��ֳ�������������(Na2S2O4)�������ڷ�֯��ҵ��Ư������ɫ�������ȼ���Na2S2O4�ǰ�ɫ��ĩ����ζ��������ˮ���������Ҵ������м�ǿ�Ļ�ԭ�����ڿ������ױ��������ڼ��Խ������ȶ���
��.������(HCOONa)���Ʊ�����������

��1������������������Ԫ�صĻ��ϼ�Ϊ______________��
��2��ʵ������Na2SO3 �����ij�ᷴӦ�Ʊ�SO2���壬�Ʊ�SO2ʱ��ѡ�õ��ᣬ����Ϊ����������ѡ�õ���______________��
A.Ũ���� B.Ũ����
C.��������Ϊ70%������ D.��������Ϊ10%������
��3�����������Ʊ������������ƵĻ�ѧ����ʽ�ɱ�ʾΪ____________________________��
��4�������������У����������Ҵ�ˮ��Һ��������______________��
��5���ڰ�װ���桰���շۡ�ʱ����������Na2CO3���壬Ŀ����_________________________��
��6�����ֽ�0.05mol/L Na2S2O4��Һ�ڿ����з��ã�����Һ��pH ��ʱ��(t)�Ĺ�ϵ��ͼ��ʾ��

t1ʱ��Һ��ֻ��NaHSO3һ����������ʱ����Ԫ�ص�����Ũ���ɴ�С��˳��Ϊ_______________��
��t1~t2�η�����ѧ��Ӧ�����ӷ���ʽΪ______________________________��
��.��ⷨ�Ʊ�:��ҵ���ö��Ե缫���NaHSO3��Һ�õ�Na2S2O4��������ͼ��ʾ

��7������Ʒ��_________________����������������������õ���
�������Ӹ�Ĥ���������������Ʋ��ʽ��ͣ���ԭ����__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��ͬѧ��������ʵ��̽���������벻ͬͭ����Һ�ķ�Ӧ��
ʵ�� | ʵ�鷽�� | ���� |
1 | ��5mLlmol/LCuSO4��Һ�м�����ɰֽ��ĥ������Ƭ | ��Ƭ��������������20min����Ƭ�����м������ݣ����к�������ɫ�������� |
2 | ��5mLlmol/LCuCl2��Һ�м�����ɰֽ��ĥ������Ƭ | ��Ƭ���������ݲ�����ͬʱ�к�ɫ����������1min��Ӧ��һ���ӿ죬�ų��������ȣ���������ɫ�������ɡ�һ��ʱ����ձ��ײ����ְ�ɫ���� |
��1����ĥ��Ƭ��Ŀ����_____________________________��
��2��ʵ���г��ֵĺ�ɫ������_______________________________��
��3��ʵ��2����1min��Ӧ��һ���ӿ�����ԭ����________________________________��
��4��������ʵ��1��2�в�������ɫ������H2����ɫ����ΪCuO���������ӷ���ʽ����H2������ԭ��__________________________�������ּ�����ɫ���������ԭ��____________________________��
��5����������ʵ��1��2�����ƲⲢ�жϣ���ɰֽ��ĥ�����Ƭ�ֱ���H+Ũ�Ⱦ�Ϊ0.2molL-1����������ᷴӦ����Ӧ������ǰ�߱Ⱥ���____________��������������������
��6����֤��ʵ��2 �а�ɫ�����Ļ�ѧ�ɷ�ΪCuCl��ijͬѧ�²������Cu��CuCl2��Һ��Ӧ������CuCl����ΪCu����________�ԡ����ݲ²�������������ʵ����ȡCu��������1mol/LCuCl2��Һ��ϣ�һ��ʱ���۲��ް�ɫ������������ͬѧ�ٴη���Al ��CuCl2��Һ��Ӧ��ʵ�����Ľ�ʵ�鷽����֤����Cu��CuCl2��Һ��Ӧ������CuCl�����ĸĽ�����Ϊ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������(��Ҫ�ɷ���Al2O3��������Fe2O3��SiO2)��ȡ������ұ������ԭ��(������Al2O3)����ȡ�����������£�

��ش��������⣺
(1)��д��Ҫ�ɷݵĻ�ѧʽ������A________����Һ���е�������NaCl��________��
(2)��Ӧ����Al3����Ӧ�����ӷ���ʽΪ_________________����Ӧ�۵����ӷ���ʽΪ____________����Ӧ�ܵĻ�ѧ����ʽΪ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������������������Һ������Ӧ���ǣ�������
A.COB.CO2C.CaOD.SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ũ�Ⱦ�Ϊ0.1mol/L.�����ΪV0��NaX��NaY��Һ�ֱ��ˮϡ�������V����֪pOH=-lgc(OH-),pOH ��![]() �ı仯��ϵ��ͼ��ʾ������������ȷ����
�ı仯��ϵ��ͼ��ʾ������������ȷ����
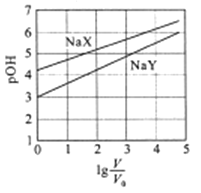
A. HX��HY�������ᣬ��Ka(HX)>Ka(HY)
B. ͼ��pOH��![]() �仯ʼ������ֱ�߹�ϵ
�仯ʼ������ֱ�߹�ϵ
C. ![]() =3ʱ��NaX��Һ��������������С��NaY��Һ
=3ʱ��NaX��Һ��������������С��NaY��Һ
D. �ֱ���ϡ��ǰ��������Һ��������pH=7ʱ��c(X-)=c(Y-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. 1molOH��������Ϊ17gmol��1
B. 0.5mol H2��ռ���ԼΪ11.2L
C. �������Ľ��ʯ�;��������ԭ�Ӹ���֮��Ϊ7��3
D. 1mol NaCl��������0.5Lˮ�У�������Һ�����ʵ���Ũ��Ϊ2molL��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com