
【题目】取某浓度的NaOH溶液10mL,向其中通入一定量的CO2,再向所得溶液中逐滴加入![]() 的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,请回答:
的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,请回答:
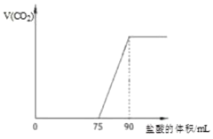
(1)原NaOH溶液的物质的量浓度为__mol·L-1;
(2)原NaOH溶液通入CO2后,所得溶液中的溶质为(写化学式)__;其物质的量之比为__。
【答案】0.9 NaOH和Na2CO3 4:1
【解析】
(1)先向氢氧化钠溶液中通入CO2,后向溶液中滴加盐酸,当CO2完全放出时,溶液的溶质是NaCl,该反应的实质是盐酸和氢氧化钠反应生成NaCl,根据盐酸的物质的量计算氢氧化钠溶液的浓度;
(2)与CO2反应,反应后溶液的溶质可能是NaOH和Na2CO3、Na2CO3、Na2CO3和NaHCO3、或NaHCO3,Na2CO3+HCl= NaHCO3+NaCl,NaHCO3+HCl=NaCl+CO2↑+H2O,消耗的盐酸的体积相等,0-75mL没有气体生成,消耗的盐酸体积大于75-90mL消耗的盐酸的体积,因此可知溶液中的溶质为NaOH和Na2CO3,反应的离子方程式为OH-+H+=H2O,CO32-+H+=HCO3-,HCO3-+H+=H2O+CO2↑, NaHCO3完全反应生成CO2消耗盐酸的体积为90mL-75mL=15mL,那么Na2CO3转化为NaHCO3消耗盐酸的体积也为15mL,因此NaOH完全反应消耗盐酸的体积为75mL-15mL=60mL,结合n=cV计算物质的量之比。
(1)先向氢氧化钠溶液中通入CO2,后向溶液中滴加盐酸,当CO2完全放出时,溶液的溶质是NaCl,该反应的实质是盐酸和氢氧化钠反应生成NaCl,盐酸和氢氧化钠的物质的量之比为1:1,设NaOH的物质的量浓度为xmol/L,加入90mL盐酸时CO2的体积最大,此时溶液为氯化钠溶液,根据Cl-和Na+守恒,可得n(NaOH)=n(NaCl)=n(HCl)=0.09L×0.1mol/L=0.009mol,那么c(NaOH)=![]() =0.9mol/L,溶液具有均一性,因此原NaOH溶液的物质的量浓度为0.9mol/L;
=0.9mol/L,溶液具有均一性,因此原NaOH溶液的物质的量浓度为0.9mol/L;
(2)与CO2反应,反应后溶液的溶质可能是NaOH和Na2CO3、Na2CO3、Na2CO3和NaHCO3、或NaHCO3,Na2CO3+HCl= NaHCO3+NaCl,NaHCO3+HCl=NaCl+CO2↑+H2O,消耗的盐酸的体积相等,0-75mL没有气体生成,消耗的盐酸体积大于75-90mL消耗的盐酸的体积,因此可知溶液中的溶质为NaOH和Na2CO3,反应的离子方程式为OH-+H+=H2O,CO32-+H+=HCO3-,HCO3-+H+=H2O+CO2↑, NaHCO3完全反应生成CO2消耗盐酸的体积为90mL-75mL=15mL,那么Na2CO3转化为NaHCO3消耗盐酸的体积也为15mL,因此NaOH完全反应消耗盐酸的体积为75mL-15mL=60mL,根据n=cV可知NaOH和Na2CO3的物质的量之比为60:15=4:1。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】[实验化学]
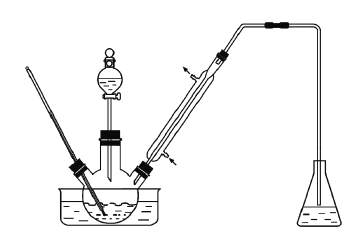
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置中冷凝管的主要作用是________,锥形瓶中的溶液应为________。
(2)步骤1所加入的物质中,有一种物质是催化剂,其化学式为_________。
(3)步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的______(填化学式)。
(4)步骤3中加入无水MgSO4固体的作用是_________。
(5)步骤4中采用减压蒸馏技术,是为了防止_____。
附表 相关物质的沸点(101kPa)
物质 | 沸点/℃ | 物质 | 沸点/℃ |
溴 | 58.8 | 1,2-二氯乙烷 | 83.5 |
苯甲醛 | 179 | 间溴苯甲醛 | 229 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表陈述Ⅰ、Ⅱ均正确,且两者在反应原理上相似的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 将 |
|
B |
|
|
C | 玻璃试剂瓶可用于盛放氢氟酸 | 石英坩埚不能用于熔化NaOH |
D |
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知299 K时,合成氨反应 N2(g ) + 3H2 ( g )![]() 2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
A. 一定大于92.0 kJB. 一定等于92.0 kJ
C. 一定小于92.0 kJD. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molSO2和1molO2充入一固定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H=-197kJ/mol,当达到化学平衡时,下列说法中正确的是
2SO3(g) △H=-197kJ/mol,当达到化学平衡时,下列说法中正确的是
A.SO2和SO3共2mol B.生成 SO32mol
C.放出197kJ热量 D.含氧原子共8mo1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨气可与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置(省略夹持装置及加热装置)可以实现该反应。实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是 ( )
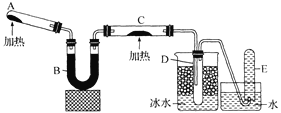
A.试管A中加入的试剂为NH4Cl固体
B.反应中氧化剂和还原剂的物质的量之比为2 : 3
C.装置B中加入的物质可以是碱石灰或无水氯化钙
D.装置D中液体可以使干燥的红色石蕊试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)丙烷(C3H8)是一种价格低廉的常用燃料,其主要成分是碳和氢两种元素,燃烧后只有二氧化碳和气态水,不会对环境造成污染。已知1 g丙烷完全燃烧放出50.45kJ的热量。丙烷在室温下燃烧的热化学方程式为____。
(2)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
则2CH4(g)+ O2(g)=2CO(g)+4H2(g)ΔH=___;
(3)在密闭容器中充入A(g)和B(g),它们的初始浓度均为2mol·L-1,在一定条件下发生反应:A(g)+B(g)![]() 2C(g) ΔH。该T1温度下,此反应的平衡常数为4,
2C(g) ΔH。该T1温度下,此反应的平衡常数为4,
①该反应的平衡常数的表达式为____。
②A的转化率为_____。
③若升温至T2时,此反应的平衡常数为1,判断该反应ΔH___0(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸(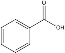 )为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
密度/g·cm-3 | 0.792 | 1.2659 | 1.0888 |
相对分子质量 | 32 | 122 | 136 |
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是______________;写出苯甲酸与甲醇反应的化学方程式:______________。
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。根据有机物的沸点,最好采用__________装置(填“甲”或“乙”)

(3)反应物CH3OH应过量,理由是______________。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请在流程图中方括号内填入操作方法的名称a______________,b______________。
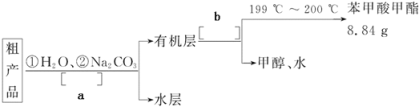
(5)通过计算,苯甲酸甲酯的产率为______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com