
【题目】相同状况下,20mL气体A2和10mL气体B2恰好化合生成20mL气体C,则C的化学式为
A.AB
B.AB2
C.A2B
D.A4B2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用__________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 ___________(“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 ________( “变多”“变少”“不变”),所求中和热_______(“相等、不相等”)
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会_____________(“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)![]() CO2(g)十H2 (g)十Q(Q>0),CO和H2O浓度变化如下图:
CO2(g)十H2 (g)十Q(Q>0),CO和H2O浓度变化如下图:
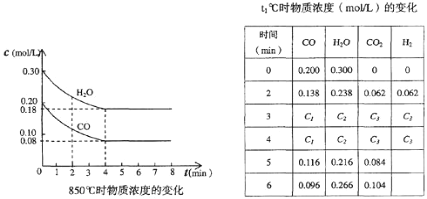
(1)则0~4 min的平均反应速率v(CO)=________mol/(L·min),该反应在850℃的平衡常数K=________
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min~4 min之间反应处于_________状态;C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4 min~5 min间,平衡向逆方向移动,可能的原因是_________(单选),表中5 min~6 min之间数值发生变化,可能的原因是_________(单选)。
A.增加水蒸气 B.降低温度 C.使用催化剂 D.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下2CO(g) + O2(g) = 2CO2(g) △H=-566 kJ·mol—1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ·mol—1,则1molCO和3molCH4组成的混合气体在上述条件下完全燃烧放出的热量为
A.2912 kJ B.2953 kJ C.3236 kJ D.3836 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol ·L-1、0.1 mol ·L-1、0.2 mol ·L-1。当反应达平衡时,可能存在的数据是
2SO3(g)。已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol ·L-1、0.1 mol ·L-1、0.2 mol ·L-1。当反应达平衡时,可能存在的数据是
A. SO2为0.4 mol ·L-1,O2为0.2 mol ·L-1 B. SO2为0.25 mol ·L-1
C. SO2、SO3均为0.15 mol ·L-1 D. SO3为0.4 mol ·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于油脂的理解或说法中,正确的是 ( )
① 油脂在人体内水解,水解产物可在人体内氧化提供能量;
② 油脂为人体合成其他化合物提供了原料;
③ 油脂的主要成分是高级脂肪酸的甘油酯,属于酯类;
④ 油脂能促进脂溶性维生素A、D、E、K等物质的吸收。
A.都正确 B.只有①②
C.只有①②③ D.只有①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,设计如下实验:

(1)写出浓硫酸与木炭粉反应的化学方程式_____________。
(2)B中加入的试剂是_____,现象是______;C的作用是____,E的作用是________。
(3)如果将F放在B、C之间,则一定不能检出的物质是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组欲探究FeCl3溶液、FeCl2溶液的化学性质
试剂清单:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片
请帮助他们完成以下实验报告:
序号 | 实验 目的 | 实验内容 | 实验现象 | 实验结论 | 离子方程式 |
实验1 | ① | 在FeCl2溶液中滴入适量 氯水 | 溶液由浅绿色 变为黄色 | ② | ③ |
实验2 | ④ | 在FeCl2溶液中加入锌片 |
| ⑤ | Zn +Fe2+= Zn2++Fe |
实验3 | ⑥ | 在FeCl3溶液中加入足量 铁粉 | ⑦ | FeCl3(Fe3+)具有氧化性 | ⑧ |
填空:
(1)①_____________③____________ ⑤____________⑧____________
综合以上实验,你能得到的结论是:Fe3+有氧化性;_________________。
(2)亚铁盐溶液易被氧化,短时间保存亚铁盐溶液时为防止亚铁盐被氧化可在溶液中加入少量______________(填试剂名称)。
(3)检验某溶液是Fe2+溶液的方法是(任写一种试剂及其对应的现象即可):________。
(4)某同学向FeCl2溶液中加入Na2O2,产生红褐色沉淀,你认为该反应中产生红褐色沉淀的原因可能是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com