
【题目】(1)按系统命名法命名:
① 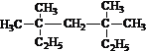 ___________________________;
___________________________;
②(CH3)2CHCH=CHCH3___________________________;
(2)写出下列各有机物的结构简式:
① 2,3-二甲基-4-乙基已烷 :_______________________________;
②支链只有一个乙基且相对分子质量最小的烷烃:___________________。
【答案】(共8分,每空2分)
(1)①3,3,5,5—四甲基庚烷;②4—甲基—2—戊烯
(2)①CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3;②CH3CH2CH(C2H5)CH2CH3
【解析】
试题(1)①烷烃的系统命名法的步骤:a选定分子中最长的C链(含C最多那条)为主链,主链上有几个C原子,就是几烷,b把主链离支链最近一端作为起点,用数字给主链的C原子标出顺序,c把支链作为取代基,把取代基的名称(如甲基-CH4,乙基-CH2-CH4)写在“几烷”前,取代基所连主链C原子对应的数字写在最前面,并和文字用短线“-”隔开。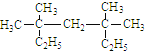 的名称为3,3,5,5—四甲基庚烷;②烯烃的系统命名法是选择含碳碳双键的最长碳链作为主链,根据主链上碳原子的数目称为某烯,然后从碳链上靠近双键的一端开始进行编号,将双键上的第一个碳原子的号码加在烯烃名称的前面以表示双键位置,取代基的名称和位置的表示方法与烷烃相同。(CH3)2CHCH=CHCH3的名称为4—甲基—2—戊烯。
的名称为3,3,5,5—四甲基庚烷;②烯烃的系统命名法是选择含碳碳双键的最长碳链作为主链,根据主链上碳原子的数目称为某烯,然后从碳链上靠近双键的一端开始进行编号,将双键上的第一个碳原子的号码加在烯烃名称的前面以表示双键位置,取代基的名称和位置的表示方法与烷烃相同。(CH3)2CHCH=CHCH3的名称为4—甲基—2—戊烯。
(2)① 2,3-二甲基-4-乙基已烷的结构简式为CH3CH(CH3)CH(CH3)CH(C2H5)CH2CH3;②在烷烃分子中乙基至少连在3号碳上,因此主链至少5个碳原子,结构简式为CH3CH2CH(C2H5)CH2CH3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在BaSO4饱和溶液中,加入Na2SO4(s),达到溶解平衡时,下列关系式正确的是( )
A. c(Ba2+)=c(SO42-)
B. c(Ba2+)≠c(SO42-),c(Ba2+)·c(SO42-)=Ksp(BaSO4)
C. c(Ba2+)=c(SO42-)=[Ksp(BaSO4)]1/2
D. c(Ba2+)≠c(SO42-),c(Ba2+)·c(SO42-)≠Ksp(BaSO4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种强氧化性漂白剂,受热易分解。亚氯酸钠制备及部分性质实验如图:
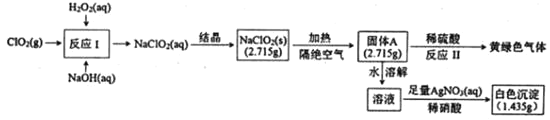
已知:①固体A为两种含氯盐组成的混合物:②AgClO3和AgcClO4都溶于水。
请回答:
(1)双氧水的电子式为___,固体A的成分是___(用化学式表示)。
(2)反应I的离子方程式为___。
(3)反应Ⅱ的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用粗盐水(溶质主要成分为NaCl),制备NaHCO3固体,流程如图:
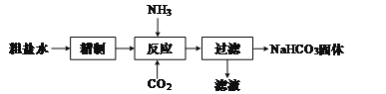
(1)“精制”是为了除去粗盐水中含有的Ca2+、Mg2+、SO![]() 等杂质离子,并获得NaCl饱和溶液,“精制”过程中包含除杂、过滤、蒸发浓缩等操作,需要加入的试剂为稍过量的①Na2CO3、②BaCl2、③盐酸、④NaOH,加入试剂的先后顺序为___(填序号)。
等杂质离子,并获得NaCl饱和溶液,“精制”过程中包含除杂、过滤、蒸发浓缩等操作,需要加入的试剂为稍过量的①Na2CO3、②BaCl2、③盐酸、④NaOH,加入试剂的先后顺序为___(填序号)。
(2)已知“反应”分两步进行。第一步生成NH4HCO3;
第二步的反应方程式为:NH4HCO3+NaCl=NaHCO3↓+NH4Cl。
①第一步反应的化学方程式为___。
②第二步反应能发生的原因是___。
(3)向“过滤”所得滤液中加入NaCl,并通入氨气,过滤,得到固体,该固体可能含有NaCl和NH4Cl,检验该固体中含有NH4Cl的方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B. [实验化学]
次硫酸氢钠甲醛(NaHSO2·HCHO·2H2O)在印染、医药以及原子能工业中应用广泛。以Na2SO3、SO2、HCHO 和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
步骤1:在烧瓶中(装置如图 所示) 加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。步骤2:将装置A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80 ~ 90益下,反应约3h,冷却至室温,抽滤。步骤3:将滤液真空蒸发浓缩,冷却结晶。
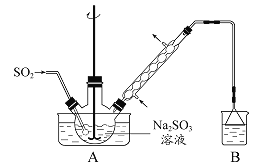
(1)装置B 的烧杯中应加入的溶液是 。
(2)①步骤2 中,反应生成的Zn(OH)2会覆盖在锌粉表面阻止反应进行,防止该现象发生的措施是
。②冷凝管中回流的主要物质除H2O 外还有 (填化学式)。
(3)①抽滤装置所包含的仪器除减压系统外还有 、 (填仪器名称)。②滤渣的主要成分有 、 (填化学式)。
(4)次硫酸氢钠甲醛具有强还原性,且在120益以上发生分解。步骤3 中不在敞口容器中蒸发浓缩的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是海带中提取碘的流程图:
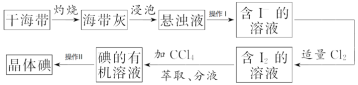
回答下列问题。
(1)干海带在_____________________中灼烧(填仪器名称)
(2)操作I名称为_____________________
(3)分液漏斗在使用前须清洗干净并_____________________,在本实验分离过程中,碘的四氯化碳应该从分液漏斗的_____________________(填“上口倒出”或“下口放出”)
(4)操作II名称为_____________________,该操作中加入碎瓷片的作用是_____________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_____________________(填标号)。
A.立即补加B.冷却后补加C.不需补加D.重新配料
(5)在操作II中,仪器选择及安装都最合理的是_____________________(填标号)。

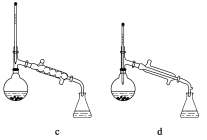
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁磁粉Fe3O4(可能含有Fe2O3或FeO杂质),为确定其纯度,称取23.28g该样品利用图1装置进行实验探究。
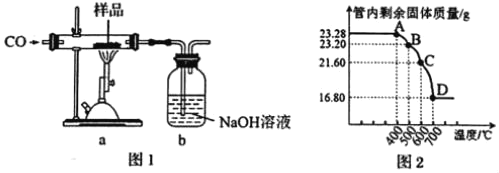
已知:Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe。
请回答:
(1)上述实验装置存在一个明显缺陷是___。
(2)利用仪器测定并绘制出反应过程中a装置中玻璃管内的固体质量随温度的变化曲线(图2),样品中含有的杂质成分是___(填化学式)。
(3)上述实验过程中,CO除作为反应物外,还起到的作用是___。
A.实验开始时,排尽装置中的空气,防止加热时发生爆炸
B.防止b中的溶液倒吸入a中
C.停止加热后,继续通CO气体,防止生成物被氧化
D.将产生的CO2全部赶入装置b中,以提高实验的精确度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,请回答下列问题:
IA | IIA | IIIA | IVA | VA | VI A | VII A | 0 族 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质最不活泼的是___________(填元素符号);
(2)③的气态氢化物的电子式________,②与④形成的气态化合物的结构式_________;
(3)这些元素形成的最高价氧化物的水化物中,碱性最强化合物的电子式:__________; 酸性最强的含氧酸为__________(填物质的化学式);
(4)②的单质可以和③的最高价氧化物的水化物反应,请写出有关化学方程式_______;
(5)⑥的单质和⑤的最高价氧化物对应的水化物反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的化合物有很多,其中Cu2S、Cu2O、CuCl都是用途非常广泛的一价铜的化合物。回答下列问题:
(1)已知:2Cu(s)+O2(g)=2CuO(s) ΔH1=-314 kJmol-1
4CuO(s)=2 Cu2O(s)+ O2(g) ΔH2=+292 kJmol-1
固相法制备Cu2O的反应CuO(s)+ Cu(s)=Cu2O(s)的ΔH=________
(2)辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
① 粗铜应与直流电源的_____ 极(填“正”或 “负”)相连。
② 铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是________ 。
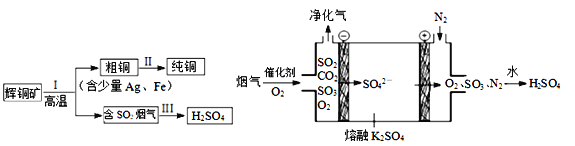
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经上右图所示方法脱除SO2,并制得H2SO4,在阳极生成SO3的电极反应式是____________________________。
(4)反应2CuCl(s) + Hg22+(aq) ![]() Hg2Cl2(s) +2Cu+(aq)达到平衡时,平衡常数K≈_____(保留两位有效数字)。[已知Ksp(CuCl)=1.2×10-6、Ksp (Hg2Cl2)=1.3×10-10]
Hg2Cl2(s) +2Cu+(aq)达到平衡时,平衡常数K≈_____(保留两位有效数字)。[已知Ksp(CuCl)=1.2×10-6、Ksp (Hg2Cl2)=1.3×10-10]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com