
【题目】某固体化合物X由5种元素组成。某学习小组进行了如下实验:
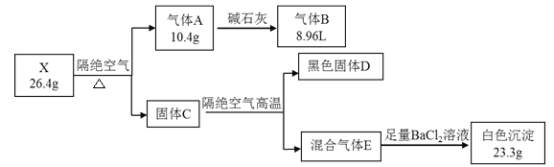
已知气体B能使湿润红色石蕊试纸变蓝。请回答:
(1)X中含有的元素有_____________,X的化学式_____________。
(2)X的水溶液可以与纤维素作用,工业上利用此性质得到产物名称_____________。
(3)写出X隔绝空气强热生成A、D、E的化学方程式_______________。
【答案】Cu、N、S、O、H ![]() 铜氨纤维
铜氨纤维 ![]()
【解析】
碱石灰吸收的应为水蒸气,气体B能使湿润红色石蕊试纸变蓝,黑色固体D应为CuO,白色沉淀应为BaSO4,结合原子守恒和质量守恒分析解题。
气体A用碱石灰吸收后剩余气体B,且气体B能使湿润红色石蕊试纸变蓝,则B为NH3,其物质的量为![]() =0.4mol,质量为0.4mol×17g/mol=6.8g,则气体A中除NH3外的气体总质量为10.4g-6.8g=3.2g,此气体应为水蒸气,物质的量为
=0.4mol,质量为0.4mol×17g/mol=6.8g,则气体A中除NH3外的气体总质量为10.4g-6.8g=3.2g,此气体应为水蒸气,物质的量为![]() =0.2mol;固体C的质量为26.4g-10.4g=16g。加热分解后生成的黑色固体应为CuO,混合气体E通入足量BaCl2溶液生成的白色沉淀23.3g,应为BaSO4,其物质的量为0.1mol,有原子守恒可知,若气体为SO3应为0.1mol,质量为8g,则混合气体应为0.1molSO2和0.05molO2;则黑色固体质量为8g,其物质的量为
=0.2mol;固体C的质量为26.4g-10.4g=16g。加热分解后生成的黑色固体应为CuO,混合气体E通入足量BaCl2溶液生成的白色沉淀23.3g,应为BaSO4,其物质的量为0.1mol,有原子守恒可知,若气体为SO3应为0.1mol,质量为8g,则混合气体应为0.1molSO2和0.05molO2;则黑色固体质量为8g,其物质的量为![]() =0.1mol,故X分解后生成的NH3、H2O、CuO、SO2和O2的物质的量之比为(0.4mol):(0.2mol):(0.1mol):(0.1mol):(0.05mol)=8:4:2:2:1,此化合物中含有Cu、N、S、H、O一共5种元素;
=0.1mol,故X分解后生成的NH3、H2O、CuO、SO2和O2的物质的量之比为(0.4mol):(0.2mol):(0.1mol):(0.1mol):(0.05mol)=8:4:2:2:1,此化合物中含有Cu、N、S、H、O一共5种元素;
(1)由分析知X中含有的元素有Cu、N、S、H、O;此化合物中含有Cu2+:NH4+:SO42-:H2O的物质的量之比为0.1mol:0.4mol:0.1mol:0.2mol=1:4:1:2, X的化学式![]() ;
;
(2) ![]() 的水溶液可以与纤维素作用,工业上利用此性质得到产物名称铜氨纤维;
的水溶液可以与纤维素作用,工业上利用此性质得到产物名称铜氨纤维;
(3) X分解后生成的NH3、H2O、CuO、SO2和O2的物质的量之比为(0.4mol):(0.2mol):(0.1mol):(0.1mol):(0.05)=8:4:2:2:1,则![]() 隔绝空气强热生成A、D、E的化学方程式为
隔绝空气强热生成A、D、E的化学方程式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】常温下0.1molL﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
A. 将溶液稀释到原体积的2倍B. 加入适量的醋酸钠固体
C. 加入等体积0.2 molL﹣1盐酸D. 加少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________,K值大小与温度的关系是:温度升高,K值_________(填一定增大、一定减小、或可能增大也可能减小)。
(2)对于可逆反应CO(g) +H2O(g) ![]() CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示三套实验装置,分别回答下列问题。
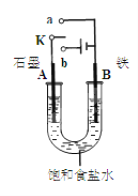
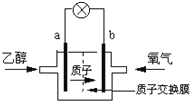
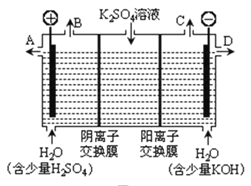
图1图2图3
(1)图1中,① 若开始时开关K与a连接,则该装置为_____(填装置名称),电极A的电极反应式为________________________
②若开始时开关K与b连接,则总反应的离子方程式为 ___________________________
(2)2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200°C左右时供电,电池示意如图2所示:
①______极(填a或b)为电池的正极,电池工作时电流方向为_________(填a→b或b→a)
②写出该电池负极的电极反应式________________________________________
(3)用图3装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾(电解槽内的阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)。
①该电解槽的阴极反应式为_____________________。
②制得的硫酸溶液从出口____(填“A”、“D”)导出,并简述原因__________________________(请用化学用语和文字解释)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将3molA和2molB充入2L一密闭容器中,发生反应:A(g)+B(g)C(g)+D(g),5min后达到平衡。已知该温度下其平衡常数K=1,下列选项正确的是
A. C平衡浓度为1.2mol/L B. 速率v(B)= 0.08 mol/(Lmin)
C. A的转化率为40% D. B的转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核磁共振造影增强剂用于疾病的诊断,还可以作为药物载体用于疾病的治疗。中科院化学研究所在肿瘤鉴别诊断用磁共振造影剂研究方面取得重要进展。为磁性纳米晶体材料在生物医学领域的应用提供了更广泛的前景。制备纳米四氧化三铁过程如图:

下列有关叙述不合理的是( )
A.纳米四氧化三铁具有磁性作为药物载体用于疾病的治疗
B.反应③的化学方程式是:6FeOOH+CO=2Fe3O4+3H2O+CO2
C.在反应②环丙胺的作用可能是促进氯化铁水解
D.纳米四氧化三铁分散在适当溶剂中,它与溶液分散质直径相当
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹 持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.…
(1)A中反应的化学方程式为:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O,则氧化性KMnO4____Cl2(填“>”“<”或“=”)。
(2)验证氯气的氧化性强于碘的实验现象是____。
(3)过程Ⅲ的实验目的是____。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____。
(5)浸有NaOH溶液的棉花团的作用是____。此处发生的化学方 程式是____。
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们单质氧化性强弱为:Cl2>Br2>(CN)2>(SCN)2>I2。试写出:在NaBr和KSCN的混合溶液中加入(CN)2的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酰胺是一种重要的有机合成的中间体。它的球棍模型如图所示:(图中“棍”代表单键或双键或三键,不同颜色球表示不同原子:C、H、O、N)

(1)丙烯酰胺的分子式为___,结构简式为___。
(2)有关丙烯酰胺的说法正确的是___。
A.丙烯酰胺分子内所有原子不可能在同一平面内
B.丙烯酰胺属于烃的含氧衍生物
C.丙烯酰胺能够使酸性高锰酸钾溶液褪色
D.丙烯酰胺能够使溴的四氯化碳溶液褪色
(3)工业上生产丙烯酰胺可以用下面的反应(反应均在一定条件下进行):
CH![]() CH
CH![]() CH2=CHCN
CH2=CHCN![]() 丙烯酰胺
丙烯酰胺
假设反应Ⅰ和反应Ⅱ都是原子利用率100%的反应,反应Ⅰ所需另一反应物的分子式为___,反应Ⅱ的方程式为___。
(4)聚丙烯酰胺(PAM)是一种合成有机高分子絮凝剂,写出由丙烯酰胺合成聚丙烯酰胺的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通足量CO2,溶液变浑浊 | 碳酸的酸性比苯酚的强 |
B | 加热乙醇与浓硫酸的混合溶液,将产生的气体通入少量酸性KMnO4溶液,溶液紫红色褪去 | 有乙烯生成 |
C | 向5 mL 0.1 mol·L1 KI溶液中加入1 mL 0.1 mol·L1 FeCl3溶液,充分反应后,萃取分液,向水层中滴加KSCN溶液,溶液呈血红色 | I-与Fe3+的反应有一定限度 |
D | 向NaHCO3溶液中滴加紫色石蕊试液,溶液变蓝 | Kw<Ka1(H2CO3)×Ka2(H2CO3) |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com