
ЁОЬтФПЁПЯђвЛКуШнУмБеШнЦїжаГфШы2 mol SO2КЭ1mol O2ЃЌдквЛЖЈЬѕМўЯТЗЂЩњЗДгІЃК2SO2ЃЋO2![]() 2SO3ЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ
2SO3ЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ
A. ДяЕНЛЏбЇЦНКтЪБЃЌе§ЗДгІКЭФцЗДгІЕФЫйТЪЖМЮЊСу
B. ЕБO2ЕФХЈЖШВЛБфЪБЃЌЗДгІДяЕНЦНКтзДЬЌ
C. ЕБЕЅЮЛЪБМфЯћКФa mol O2ЃЌЭЌЪБЯћКФ2a mol SO2ЪБЃЌЗДгІДяЕНЦНКтзДЬЌ
D. ЕБSO2ЁЂO2ЁЂSO3ЕФЗжзгЪ§БШЮЊ2ЃК1ЃК2ЃЌЗДгІДяЕНЦНКтзДЬЌ
ЁОД№АИЁПB
ЁОНтЮіЁПЪдЬтЗжЮіЃКAЃЎЛЏбЇЦНКтЪЧвЛИіЖЏЬЌЦНКтЃЌДяЕНЛЏбЇЦНКтЪБЃЌе§ЗДгІКЭФцЗДгІЕФЫйТЪЖМВЛЕШгкСуЃЌДэЮѓЃЛBЃЎИљОнЛЏбЇЦНКтзДЬЌЕФЬиеїЃКИїзщЗжЕФХЈЖШВЛЫцЪБМфЕФБфЛЏЖјБфЛЏЃЌМДДяЕНЛЏбЇЦНКтЪБЃЌSO2ЁЂO2КЭSO3ЕФЮяжЪЕФСПХЈЖШОљБЃГжВЛБфЃЌе§ШЗЃЛCЃЎЛЏбЇЦНКтЪЧвЛИіЖЏЬЌЦНКтЃЌДяЕНЛЏбЇЦНКтЪБЃЌе§ЗДгІКЭФцЗДгІЕФЫйТЪЖМВЛЕШгкСуЃЌЕБЕЅЮЛЪБМфЯћКФa mol O2ЃЌЭЌЪБЯћКФ2a mol SO2ЪБЃЌжЛБэЪОЗДгІе§ЯђНјааЃЌЦНКтХаЖЯЗДгІЪЧЗёДяЕНЦНКтЃЌДэЮѓЃЛDЃЎЕБSO2ЁЂO2ЁЂSO3ЕФЗжзгЪ§БШЮЊ2ЃК1ЃК2ЃЌЗДгІПЩФмДяЕНЦНКтзДЬЌвВПЩФмЮДДяЕНЦНКтЃЌетгыЗДгІЬѕМўМАМгШыЕФЮяжЪЕФЖрЩйгаЙиЃЌДэЮѓЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІдкШЮКЮЮТЖШЯТОљФмздЗЂНјааЕФЪЧ
A. 2N2(g)ЃЋO2(g)===2N2O(g) ІЄHЃНЃЋ163 kJЁЄmolЃ1
B. Ag(s)ЃЋCl2(g)===AgCl(s) ІЄHЃНЃ127 kJЁЄmolЃ1
C. HgO(s)===Hg(l)ЃЋO2(g) ІЄHЃНЃЋ91 kJЁЄmolЃ1
D. H2O2(l)===O2(g)ЃЋH2O(l) ІЄHЃНЃ98 kJЁЄmolЃ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗА(23V)БЛГЦЮЊЁАЯжДњЙЄвЕЮЖОЋЁБЃЌПЩЬэМгдкИжЬњжаЃЌВЂвдюбвЛТСЃЗАКЯН№ЕФаЮЪНгУгкКНЬьСьгђЃЛЗАЕФЛЏКЯЮяБЛЙуЗКгУзїДпЛЏМСЁЂШМСЯМАЕчГиЕШЁЃЮвЙњЗАюбДХЬњПѓДЂСПНЯДѓЃЌЪЧЪРНчЩЯВњЗАДѓЙњЁЃЧыЭъГЩЯТСаЮЪЬтЃК
(1)ЗАЕФЛљЬЌдзгЕФМлЕчзгХХВМЭМЮЊ___________ЁЃ
(2)ЗАЕФФГжжбѕЛЏЮяЕФОЇАћНсЙЙШчЯТЭМ1ЫљЪОЃЌдђИУбѕЛЏЮяЕФЛЏбЇЪНЮЊ___________ЃЌЦфШлЗаЕуБШЯТЭМ3(ЮЊСкБНЖўМзЫсєћЕФНсЙЙ)ЮяжЪЕФШлЗаЕувЊ___________(ЬюЁАИпЁБЁАЕЭЁБЛђЁАВюВЛЖрЁБ)ЁЃ
(3)V2O5ЪЧвЛжжГЃМћЕФДпЛЏМСЃЌдкКЯГЩСђЫсЁЂЯѕЫсЁЂСкБНШ§МзЫсєћЁЂввЯЉЁЂБћЯЉжаЃЌОљЪЙгУЮхбѕЛЏЖўЗАзїДпЛЏМСЁЃ

ЂйЮхбѕЛЏЖўЗАЕФНсЙЙМђЪНШчЩЯЭМ2ЫљЪОЃЌдђИУНсЙЙжаКЌга___________ИіІаМќЁЃ
ЂкдкБћШЉ( CH3CH2CHO)ЗжзгжаЬМдзгЕФдгЛЏЗНЪНЗжБ№ЮЊ___________ЁЃ
ЂлCЁЂNЁЂOЁЂNeЫФдЊЫиЃЌЦфЕквЛЕчРыФмДгДѓЕНаЁЕФЫГађвРДЮЮЊ______________________ЁЃ
ЂмV2O5ШмНтдкNaOHШмвКжаЃЌПЩЕУЕНЗАЫсФЦ(Na3VO4)ЁЃСаОйгыVO43ЃПеМфЙЙаЭЯрЭЌЕФвЛжжвѕРызгЃК___________(ЬюРызгЗћКХ)ЁЃ
(4)вбжЊЕЅжЪЗАЕФОЇЬхВЩгУЬхаФСЂЗНЖбЛ§ЃЌОЇАћШчЩЯЭМ4ЫљЪОЃЌМйЩшЗАдзгжБОЖЮЊdЁС10-7cmЃЌЗАЕФЯрЖддзгжЪСПЮЊMЃЌдђОЇЬхУмЖШЕФБэДяЪНЮЊ___________gЁЄcmЃ3ЁЃ(ЩшАЂЗќМгЕТТоГЃЪ§ЮЊNA)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаБфЛЏЙ§ГЬЃЌашвЊМгШыЛЙдМСВХФмЪЕЯжЕФЪЧ
A. Fe ![]() Fe2+ B. SO2
Fe2+ B. SO2 ![]() S C. NH4+
S C. NH4+ ![]() NH3 D. KMnO4
NH3 D. KMnO4 ![]() O2
O2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаРызгЗНГЬЪНВЛе§ШЗЕФЪЧ
A. ЩйСПSO2ЦјЬхЭЈШыДЮТШЫсФЦШмвКжаЃКSO2+3ClO-+H2O=SO42-+ClЃ+2HClO
B. бѕЛЏЬњШмгкHIШмвКЃКFe2O3+6H+=2Fe3++3H2O
C. ЬМЫсЧтФЦгыЙ§СПBa(OH)2ШмвКЗДгІЃКHCO3-+OH-+Ba2+=BaCO3![]() +H2O
+H2O
D. ЯђЙшЫсФЦЫЎШмвКжаЭЈШыЙ§СПCO2ЦјЬхЃКSiO32-+2H2O+2CO2=2HCO3-+H2SiO3![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгЩКЯГЩЦјжЦБИЖўМзУбЃЌЩцМАШчЯТЗДгІЃК
ЃЈiЃЉ2CH3OH(g)![]() C2H4(g)+2H2O(g) ІЄH1
C2H4(g)+2H2O(g) ІЄH1
ЃЈiiЃЉ2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ІЄH2
CH3OCH3(g)+H2O(g) ІЄH2
ФмСПБфЛЏШчЭМЫљЪОЃК
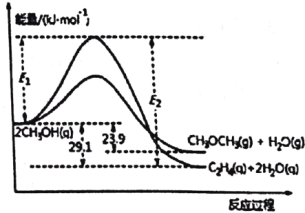
ЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ІЄH1ЃМІЄH2
B. ЗДгІЃЈiiЃЉЮЊЮќШШЗДгІ
C. C2H4(g)+H2O(g)![]() CH3OCH3(g) ІЄH = -5.2 kJЁЄmolЃ1
CH3OCH3(g) ІЄH = -5.2 kJЁЄmolЃ1
D. ШєдкШнЦїжаМгШыДпЛЏМСЃЌдђE2-E1НЋБфаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЛЏКЯЮяжабєРызгКЭвѕРызгЕчзгВуНсЙЙЯрЭЌЕФЪЧ( )
A. NaClB. MgF2C. MgCl2D. K2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЗДгІmAЃЈgЃЉЃЋnBЃЈgЃЉ![]() pCЃЈgЃЉЃЋqDЃЈgЃЉО10 minКѓДяЕНЦНКтЃЌВтЕУДЫЪБAЕФХЈЖШМѕЩйСЫnmol/LЃЌCЕФХЈЖШдіМгСЫ2n/3mol/LЃЌгжжЊЃЌЦНОљЗДгІЫйТЪVC=2VBЃЎДяЕНЦНКтКѓЃЌШєБЃГжЮТЖШВЛБфЃЌЫѕаЁШнЦїЬхЛ§ЃЌAЕФзЊЛЏТЪВЛБфЃЌдђИУЗДгІЕФЛЏбЇЗНГЬЪНгІЮЊ
pCЃЈgЃЉЃЋqDЃЈgЃЉО10 minКѓДяЕНЦНКтЃЌВтЕУДЫЪБAЕФХЈЖШМѕЩйСЫnmol/LЃЌCЕФХЈЖШдіМгСЫ2n/3mol/LЃЌгжжЊЃЌЦНОљЗДгІЫйТЪVC=2VBЃЎДяЕНЦНКтКѓЃЌШєБЃГжЮТЖШВЛБфЃЌЫѕаЁШнЦїЬхЛ§ЃЌAЕФзЊЛЏТЪВЛБфЃЌдђИУЗДгІЕФЛЏбЇЗНГЬЪНгІЮЊ
A. 2AЃЈgЃЉЃЋ6BЃЈgЃЉ![]() 3CЃЈgЃЉЃЋ5DЃЈgЃЉ
3CЃЈgЃЉЃЋ5DЃЈgЃЉ
B. 3AЃЈgЃЉЃЋBЃЈgЃЉ![]() 2CЃЈgЃЉЃЋ2DЃЈgЃЉ
2CЃЈgЃЉЃЋ2DЃЈgЃЉ
C. 3AЃЈgЃЉЃЋBЃЈgЃЉ![]() 2CЃЈgЃЉЃЋDЃЈgЃЉ
2CЃЈgЃЉЃЋDЃЈgЃЉ
D. AЃЈgЃЉЃЋ3BЃЈgЃЉ![]() 3CЃЈgЃЉЃЋ3DЃЈgЃЉ
3CЃЈgЃЉЃЋ3DЃЈgЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЦЋЖўМзыТЃЈC2H8N2ЃЉЪЧвЛжжИпФмШМСЯЃЌШМЩеВњЩњЕФОоДѓФмСППЩзїЮЊКНЬьдЫдиЛ№М§ЕФЭЦЖЏСІЃЎЯТСаа№Ъіе§ШЗЕФЪЧЃЈЃЉ
A. ЦЋЖўМзыТЃЈC2H8N2ЃЉЕФФІЖћжЪСПЮЊ60g
B. 6.02ЁС1023ИіЦЋЖўМзыТЃЈC2H8N2ЃЉЗжзгЕФжЪСПЮЊ60g
C. 1molЦЋЖўМзыТЃЈC2H8N2ЃЉЕФжЪСПЮЊ60g/mol
D. 6gЦЋЖўМзыТЃЈC2H8N2ЃЉКЌгаNAИіЦЋЖўМзыТЃЈC2H8N2ЃЉЗжзг
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com