
| a |
| y+A |
| (A-N+y)×a |
| y+A |
| (A-N+y)×a |
| y+A |
| 10g |
| 20g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
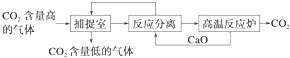
| A、①③ | B、②④ | C、③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)的燃烧热△H=-285.8 kJ?mol-1 |
| B、1molH2O(l)变成1mo1H2O(g),吸收88kJ能量 |
| C、3H2(g)+CO2(g)=CH3OH(l)+H2O(l)△H=+135.9 kJ?mol-1 |
| D、可以寻找特殊催化剂使H2O分解,同时放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Na+ | Al3+ | Cl- | X |
| 个数 | 3a | 2a | a | b |
| A、SO42-、4 a |
| B、NO3-、4 a |
| C、OH-、8 a |
| D、SO42-、8 a |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、21.9% |
| B、11.0% |
| C、13.5mol/L |
| D、5.67mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、.18 | B、.36 |
| C、34.2 | D、.37.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
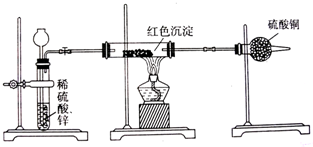
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com